Spektrometria mas sprzężona z wysokosprawną chromatografią cieczową (LC-MS, ang. Liquid chromatography-mass spectrometry) jest coraz bardziej popularną techniką wykorzystywaną w analizie ilościowej. Umożliwia ona pomiar stężenia wielu substancji równocześnie w krótkim czasie, nawet w skomplikowanej matrycy, zapewniając jednocześnie bardzo niskie limity oznaczalności. Jednakże, jak każda technika, ma swoje ograniczenia i wymaga wiedzy, aby skutecznie z niej korzystać. Część wad związana jest z metodą jonizacji, a część z rodzajem stosowanych analizatorów masy. W ostatnich latach można zauważyć coraz większe zainteresowanie spektrometrami mas wysokiej rozdzielczości, co odzwierciedlone jest w ich częstym wykorzystywaniu w analizie ilościowej. W artykule podjęto próbę wyjaśnienia kwestii częstego wykorzystywania potrójnego kwadrupolu w analizie ilościowej oraz zastosowania w tym kontekście spektrometrów mas wysokiej rozdzielczości. Przedstawione zostały wady i zalety obu rozwiązań oraz przewidywania dotyczące najbliższej przyszłości analizy ilościowej za pomocą systemów LC/MS/MS wyposażonych w źródła jonów działające pod ciśnieniem atmosferycznym.
Pierwszym wyzwaniem stojącym przed użytkownikiem systemu LC/MS/MS jest relatywnie niska powtarzalność pomiarów wynikająca z dynamiki procesów zachodzących podczas jonizacji. Najczęściej wykorzystywaną metodą jonizacji działającą pod ciśnieniem atmosferycznym jest elektrosprej (ESI, ang. Electrospray Ionization). Podczas jonizacji naładowane cząsteczki analitu przenoszone są z fazy ciekłej do gazowej. Wydajność tego procesu jest niska (średnio 1:105 cząsteczek ulega jonizacji) i zależy od bardzo wielu parametrów. Kluczową rolę odgrywają: budowa cząsteczki, tzn. rodzaj grup funkcyjnych, skład fazy ruchomej, parametry i geometria źródła jonów oraz obecność pozostałych składników analizowanych próbek. Wszystko to sprawia, że wydajność jonizacji poszczególnych substancji może się bardzo różnić. Ponadto, mierzona intensywność sygnału może się zmieniać w kolejnych pomiarach. Jest to szczególnie istotne dla próbek rzeczywistych. Aby poprawnie wykonywać bezwzględne pomiary ilościowe konieczne jest przygotowanie krzywych kalibracyjnych. W analizie LC/MS zaleca się również stosowanie wzorca wewnętrznego. Szczególnie użyteczna jest pochodna badanej substancji znaczona izotopem. Producenci spektrometrów mas, z większym lub mniejszym sukcesem, starają się tak zaprojektować źródła jonów, aby analiza na ich systemach była jak najbardziej powtarzalna i jak najbardziej przystępna dla użytkownika. Zazwyczaj dany producent stosuje te same źródła jonów w spektrometrach z różnymi rodzajami analizatorów mas.
Bardzo istotne dla uzyskania prawidłowego wyniku w analizie ilościowej jest dobranie odpowiedniego typu spektrometru i stosowanie właściwego trybu pracy. Podczas wykonywania pomiarów na systemach LC/MS/MS zazwyczaj nie jest wymagane rozdzielenie analizowanych związków na kolumnie chromatograficznej. W wielu przypadkach system HPLC i kolumna chromatograficzna wykorzystywane są po to, aby rozłożyć w czasie proces jonizacji, tzn. aby wszystkie analizowane substancje nie trafiały do źródła jednocześnie. Wyjątkiem jest stosowanie analizy wstrzykowej (FIA, ang. Flow Injection Analysis), w której cała próbka dostaje się jednocześnie do źródła jonów. Przeprowadzanie takich pomiarów jest możliwe dzięki wysokiej selektywności spektrometru mas. Z powodu relatywnie niskiej powtarzalności pomiarów jest stosowany w badaniach przesiewowych i daje wynik półilościowy. Co interesujące, w metodzie FIA do wyliczania stężenia związków stosuje się intensywność sygnałów, a nie pole powierzchni pod pikiem. Z drugiej strony, w przypadku analizy związków izomerycznych lub bogatych matryc, rozdzielnie analitów na kolumnie chromatograficznej jest kluczowe do przeprowadzenia wiarygodnej analizy ilościowej.

Niezależnie od analizowanej próbki i metody pomiarowej, to co jest istotne w analizie ilościowej to jak największa wydajność procesu analizowania (rozdzielania jonów). Im większa jest wydajność analizatora masy w danym trybie, tym więcej wytworzonych w źródle jonów trafia do detektora, a co za tym idzie większa jest czułość całego systemu. Kolejnym istotnym parametrem jest selektywność analizatora. Im lepiej możemy rozróżnić od siebie analizowane substancje, tym bardziej selektywny jest spektrometr, a co za tym idzie mniejsze są interferencje w trakcie pomiaru i możliwe jest uzyskanie niższych limitów oznaczalności.
Najprostszym analizatorem masy jest kwadrupol. Może on działać w trybie skanowania lub obserwacji wybranych jonów. Różnica w wydajności tych trybów wynosi kilka rzędów wielkości. Zastosowanie w analizie ilościowej ma tylko tryb obserwacji wybranych jonów. W przypadku analizy pojedynczego związku wydajność tego analizatora jest bliska 100%. Jednakże sam analizator kwadrupolowy jest mało selektywny. Nominalna masa jonu zmierzona z dokładnością do części dziesiętnych jednostki masy atomowej nie jest wystarczająco charakterystyczna dla analitu. Dla przykładu, ogólnodostępna baza danych ChemSpider, gromadząca informacje na temat struktury i właściwości związków chemicznych, wykazuje dla danej masy nominalnej setki tysięcy związków chemicznych (Tabela 1).
Tabela 1. Ilość struktur w bazie Chemspider w zależności od masy nominalnej.
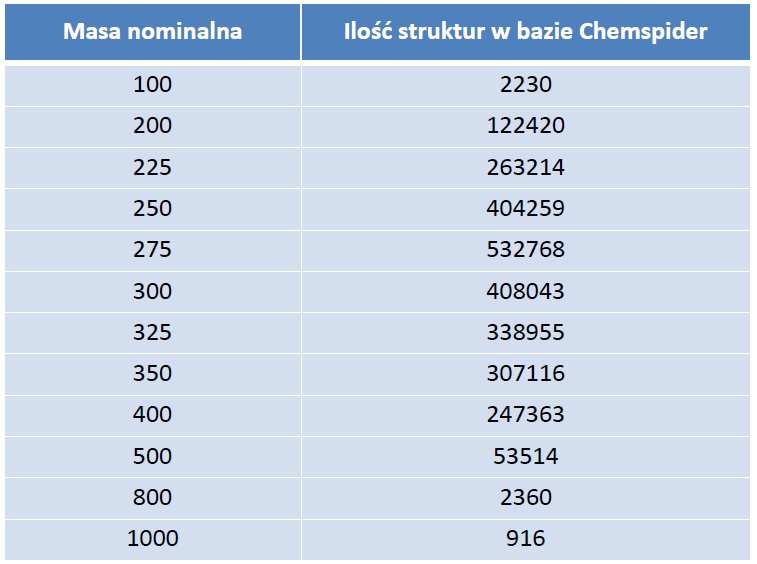
Nie wszystkie jonizują się w technice ESI, niemniej jednak ukazuje to jak duże jest ryzyko interferencji. Dodatkowo widmo komplikuje sama metoda jonizacji. W technice ESI obserwujemy jony pseudomolekularne powstałe poprzez przyłączenie do cząsteczki analitu protonu, kationu metalu takiego jak sód, potas, jonu amonowego i wielu innych kationów powszechnie występujących pierwiastków (Rysunek 1).
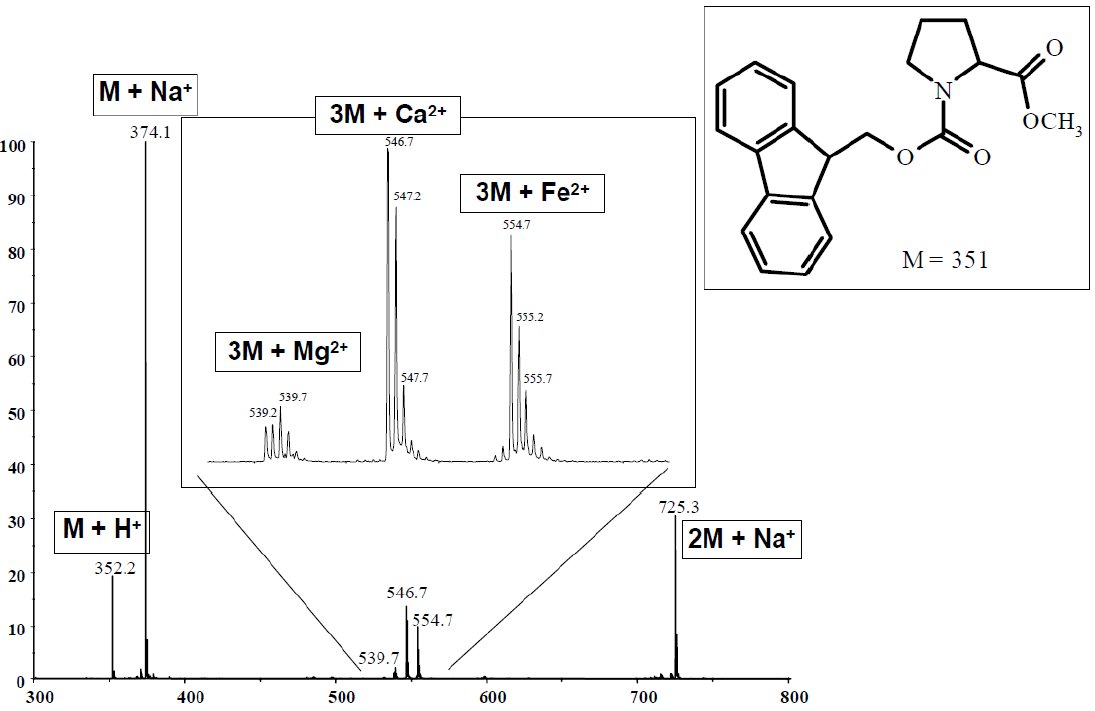
Rysunek 1. Powstawanie adduktów w technice ESI-MS dla związku o masie nominalnej 351 rozpuszczonego w metanolu. Bieńkowski, T., Brodzik-Bieńkowska, A. and Danikiewicz, W. (2002), Complexes of bivalent metal cations in electrospray mass spectra of common organic compounds. J. Mass Spectrom., 37: 617–622.
Dodatkowo, w procesie jonizacji obserwuje się powstawanie różnego rodzaju adduktów z rozpuszczalnikami oraz fragmentów jonizowanych substancji. Podobny efekt obserwowany jest również w trybie jonów ujemnych. Dlatego też, monitorując masę jonu analitu z niską rozdzielczością obserwujemy bardzo wiele interferencji i wysoki sygnał tła.
W związku z powyższym, w analizie ilościowej wykorzystuje się zazwyczaj spektrometry typu potrójny kwadrupol, które wyposażone są w dwa kwadrupolowe analizatory masy rozdzielone komorą zderzeń. Taki układ analizatorów mas pozwala na rozpoznawanie analitu na podstawie produktów reakcji fragmentacji. Pierwszy analizator mas w trybie obserwacji wybranych jonów z wysoką wydajnością przepuszcza do komory zderzeń jony pseudomolekularne analitu. W komorze fragmentacyjnej, na skutek wielu zderzeń z cząsteczkami gazu kolizyjnego, indywidua te rozpadają się na mniejsze jony i cząsteczki obojętne. Następnie drugi analizator przepuszcza tylko wybrany jon fragmentacyjny. Taki tryb nazwany monitorowaniem reakcji fragmentacji (MRM – ang. Multiple reaction monitoring, lub SRM – ang. Selected reaction monitoring; w zależności od producenta sprzętu) jest najczulszym (najbardziej wydajnym) i bardzo selektywnym trybem pracy spektrometru mas. W trybie MRM oba analizatory masy pracują z maksymalną wydajnością. Nie wszystkie jony badanego analitu docierają do detektora, ponieważ w procesie fragmentacji powstaje zazwyczaj więcej niż jeden fragment jonowy. Ilość docierających jonów do detektora jest mniejsza niż w przypadku obserwacji jonu macierzystego (mniejsza bezwzględna intensywność), jednakże dzięki znacznie większej selektywności, możliwe jest uzyskanie znacznie większej czułości niż za pomocą pojedynczego kwadrupola (Rysunek 2).
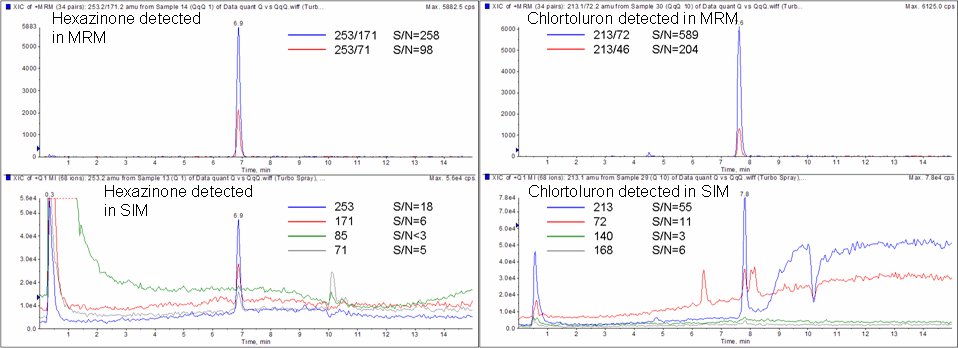
Rysunek 2. Porównanie selektywności trybu pracy SIM i MRM. Materiały AB SCIEX
Zwiększona selektywność umożliwia również zwiększenie zakresu dynamicznego metody analitycznej. Zakres odpowiedzi liniowej detektora w systemach kwadrupolowych przekracza 6 rzędów wielkości. Dzięki temu, że tryb MRM jest bardzo selektywny, możliwe jest wykonywanie pomiarów ilościowych dla sygnałów o intensywności kilkudziesięciu zliczeń na sekundę (cps – ang. Count per second). W sprzyjających warunkach możliwe jest tworzenie metod ilościowych przy zachowaniu liniowości w zakresie 6 rzędów wielkości. Tryb MRM ma jednak poważne ograniczenie. Możemy zarejestrować tylko obecność związków, dla których zostały zdefiniowane reakcje fragmentacji.
Jeżeli w badanej próbce znajdują się inne substancje, nie uzyskamy o nich żadnych informacji.
To jak niskie limity detekcji można uzyskać za pomocą systemu LC/MS/MS działającego w trybie MRM zależy od wielu czynników. Najważniejsze z nich to wydajność jonizacji oraz to, jak bardzo unikalną reakcję fragmentacji obserwujemy. Zazwyczaj tworząc metodykę ilościową staramy się unikać często występujących fragmentacji, takich jak utrata cząsteczki wody w trybie jonów dodatnich lub dwutlenku węgla w trybie jonów ujemnych. Niezwykle istotna jest również matryca, w której mierzymy stężenie interesujących nas związków. Im więcej jest w niej związków podobnych do naszego analitu, tym większe prawdopodobieństwo interferencji i większego tła w czasie pomiarów. Najczęściej jesteśmy w stanie poradzić sobie z sygnałami interferującymi poprzez dobór odpowiednich warunków chromatograficznych. Znacznie trudniejszym wyzwaniem jest wysoki sygnał tła. Jednym ze sposobów jego zmniejszenia jest zmiana sposobu przygotowania próbki, lub zwiększenie selektywności pomiaru, o czym będzie mowa w dalszej części artykułu.

Shimadzu LCMS-8045
Tryb MRM stosowany w spektrometrach typu potrójny kwadrupol jest najczęściej rekomendowany do pomiarów ilościowych. Większość wytycznych (unijne, farmakopealne itp.) zaleca stosowanie tego trybu w analizie ilościowej. Zazwyczaj dla każdego badanego związku stosuje się dwa przejścia MRM. Jedno przejście wykorzystywane jest do wyznaczenia stężenia, a drugie, na podstawie stosunku ich intensywności, do potwierdzenia tożsamości badanej substancji. Stosując tryb MRM trzeba mieć świadomość, że wraz ze wzrostem liczby analitów w pojedynczym pomiarze, spada wydajność pracy spektrometru. W chwili gdy mierzone są jony pochodzące ze zdefiniowanej reakcji fragmentacji wszystkie inne przejścia MRM nie są obserwowane (nie docierają do detektora). Tworząc metodę MRM określa się masy obserwowanych jonów w pierwszym i drugim kwadrupolowym analizatorze masy, czas obserwowania danego przejścia (ang. dwell time), oraz przerwy między obserwowaniem poszczególnych przejść (ang. pause time). Suma tych czasów składa się na całkowity czas cyklu. Wydajność spektrometru można określić poprzez stosunek czasu obserwowanego przejścia do czasu trwania całego cyklu. Większa ilość obserwowanych przejść MRM powoduje spadek wydajności. Takie zjawisko powoduje, że metody ilościowej oparte o przejścia MRM dla bardzo wielu związków przestają być efektywne. Należy pamiętać także, że dla potwierdzenia tożsamości związku obserwuje się dwa przejścia MRM. Aby zwiększyć ilość możliwych do obserwowania par MRM, producenci sprzętu wprowadzili dodatkowe parametry dedykowane do metod ilościowych: czas retencji danego przejścia oraz okno czasowe w jakim może się ono pojawić. Dzięki temu rozwiązaniu w danym przedziale czasu obserwowane są przejścia MRM dla analitów o danym czasie retencji. Kolejnym sposobem na zwiększenie ilości obserwowanych jonów jest wykorzystanie tylko jednego przejścia MRM dla związku, a następnie w momencie gdy sygnał analitu przekroczy zdefiniowaną wartość, zmierzenie kolejnych przejść MRM dla potwierdzenia jego tożsamości lub wykonanie widma fragmentacyjnego na spektrometrach typu QTRAP. Te modyfikacje umożliwiły zwiększenie ilości możliwych do obserwowania analitów do kilkuset. Niestety, dodanie parametru czasu retencji do obserwowanego przejścia MRM spowodowało, że metody te stały się wrażliwe na jego zmiany. Istnieje więc ryzyko, że dany analit nie zostanie zarejestrowany jeżeli zmodyfikowany zostanie skład fazy ruchomej lub kolumna ulegnie zużyciu. Oprócz zmniejszenia wydajności, obserwowanie wielu par MRM wydłuża czas cyklu pomiarowego. W szybkich metodach LC/MS/MS ważne jest to, by dobrać czas trwania całego cyklu tak, aby częstotliwość pomiaru jego intensywności była odpowiednio duża, tzn. aby na obwiedni piku chromatograficznego zostało zarejestrowanych przynajmniej 12 punktów. Takie postępowanie umożliwia właściwą integrację jego powierzchni. Aby zmniejszyć czas trwania cyklu, producenci sprzętu oferują spektrometry, które umożliwiają stosowanie coraz krótszych czasów obserwowania przejść MRM i odstępów między nimi. Należy pamiętać, że skracanie czasu obserwacji wiąże się z pogorszeniem jakości sygnału, co wynika z tego, że do detektora dociera proporcjonalnie mniej jonów. Nie jest możliwe również całkowite wyeliminowanie przerwy pomiędzy obserwowaniem poszczególnych przejść, gdyż niezbędny jest on do tego by anality z obserwowanego przejścia MRM mogły opuścić optykę jonową. Odpowiednio dobrany czas przerwy gwarantuje, że jony docierające do detektora pochodzą z obserwowanej reakcji fragmentacji, a nie z poprzedzającej. Aby zmniejszyć ryzyko powstawania fałszywych sygnałów nie należy umieszczać po sobie przejść MRM, w których dla drugiego analizatora zdefiniowana jest taka sama wartość m/z. W nowoczesnych, potrójnych kwadrupolach ważne jest, aby możliwe było obserwowanie przejścia MRM przez 5 ms lub krócej, oraz aby czas odstępu między kolejnymi przejściami wynosił 1 ms. Dodatkowo, zazwyczaj określane są jeszcze dwa parametry: prędkość skanowania i czas przełączania polaryzacji. O ile pierwszy z parametrów jest absolutnie bez znaczenia dla analizy ilościowej i ogólnie ma małe znaczenie w przypadku tego typu spektrometru, o tyle drugi może być całkiem istotny, szczególnie w metodach wielozwiązkowych, gdzie obserwowane są substancje o bardzo różnych właściwościach. Jonizacja związku zależy od jego budowy i rodzaju grup funkcyjnych. Większość analitów zazwyczaj jonizuje się lepiej w trybie jonów dodatnich, ale istnieje również spora grupa, w której wydajność jonizacji jest większa w trybie jonów ujemnych. W takim wypadku warto jest tworzyć metody, w trakcie których przełączana jest polaryzacja. Wydłuża to czas całego cyklu, ale w bardzo istotny sposób może poprawić limity detekcji. Nowoczesne spektrometry typu potrójny kwadrupol, mogą zmienić polaryzację nawet w 5 ms.
W dalszym ciągu spektrometry typu potrójny kwadrupol są najpopularniejszym rozwiązaniem wykorzystywanym w analizie ilościowej. Przyczyną jest ich wysoka czułość i bardzo dobra selektywność. Jednakże czym więcej związków chcemy analizować, tym większym wyzwaniem staje się stworzenie takiej metody. Należy pamiętać, że dla każdego analizowanego związku musimy dobrać masy w pierwszym i drugim analizatorze masy, oraz zoptymalizować parametry, w szczególności energię zderzeń. Niekorzystnym efektem jest zmniejszenie wydajności i wydłużenie cyklu pomiarowego wraz ze wzrastającą ilością badanych analitów. Wszystko to powoduje, że tworzenie metod, w których obserwowane jest przeszło 1000 par MRM traci sens. W przypadku analizy większej ilości związków należy zastanowić się nad zastosowaniem spektrometru wysokiej rozdzielczości. W obecnej chwili są dwie technologie pozwalające na wykonywanie takich pomiarów: analizatory czasu przelotu (TOF, ang. Time of Flight) i spektrometry z analizatorem typu Orbitrap. Oba typy analizatorów masy charakteryzują się podobną wydajnością, a więc i czułością. Trzy istotne parametry dla tego typu spektrometrów to rozdzielczość, dokładność pomiaru masy i szybkość zbierania widma. Rozdzielczość spektralna oznacza zdolność do rozdzielnia sygnałów w widmie. Czym węższy jest sygnał, tym większą rozdzielczością charakteryzuje się dany analizator masy, co z kolei umożliwia lepszą identyfikację związków. Rozdzielczość dla tego typu spektrometrów wyznacza się dzieląc wartość m/z danego sygnału przez szerokość sygnału w połowie wysokości (FWHM, ang. full width at half maximum). Zagadnienie to zostało przedstawione na rysunku 3.
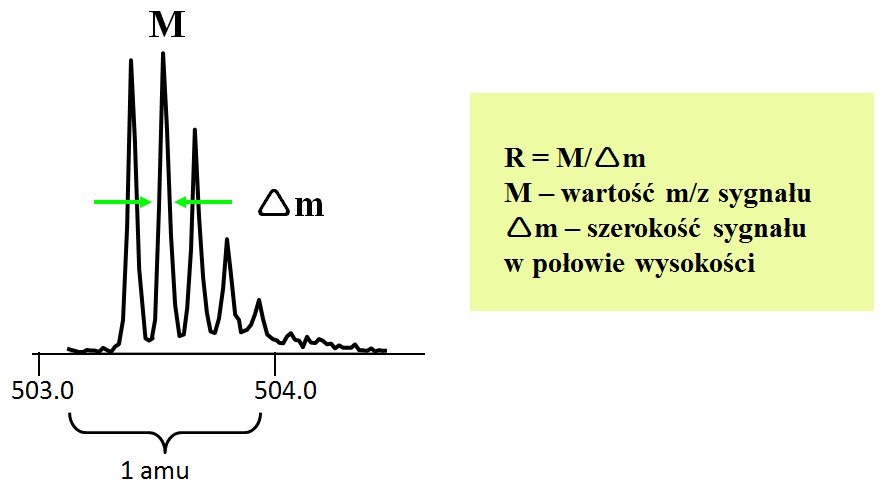
Rysunek 3. Sposób wyznaczania rozdzielczości w spektrometrach wysokiej rozdzielczości.
Analizatory TOF osiągają rozdzielczość do 70 000 i jest ona stała w prawie całym zakresie mas. Dla sygnałów poniżej 100 m/z zaczyna znacząco się zmniejszać. Istotnie, rozdzielczość analizatora TOF jest niezależna od prędkości zbierania danych, która może sięgać nawet 100 Hz. W przypadku analizatora typu Orbitrap jest możliwe uzyskanie wysokiej rozdzielczości, sięgającej kilkuset tysięcy. Wysoka rozdzielczość jest jednak nierozłącznie związana z długim czasem zbierania widma, co jest efektem wykorzystywanej przez ten analizator transformacji Fouriera. Ponadto, dla coraz to wyższych wartość m/z obserwuje się spadek rozdzielczości. Jednakże dokładność pomiaru masy jest zbliżona dla obu typów analizatorów. Technologie te umożliwiają wykonywanie pomiarów z dokładnością do milionowych części m/z mierzonych sygnałów (ppm, ang. parts per milion). Obie technologie niewątpliwie różnią się parametrami, jednak w rutynowej analizie i zastosowaniu w analizie ilościowej mają bardzo zbliżone możliwości.
Najprostsze systemy LC/MS wykorzystujące wysoką rozdzielczość to spektrometry wyposażone w pojedynczy analizator TOF lub analizator typu Orbitrap (spektrometr o nazwie Orbitrap to połączenie liniowej pułapki jonowej i analizatora Orbitrap, jest przeznaczony do analizy jakościowej, np. spektrometr Exactive, firmy Thermo Fisher Scientific). Umożliwiają one zbieranie widm MS wysokiej rozdzielczości. Jednak nie mogą one, tak jak analizator kwadrupolowy, obserwować wybranych jonów. Z drugiej strony, w czasie zbierania danych wykonywane jest zawsze pełne widmo. Pomimo że tryb ten jest mniej wydajny niż obserwowanie wybranych jonów, jest wydajniejszy niż skanowanie za pomocą kwadrupola. Dodatkowo, wysoka rozdzielczość zapewnia większą selektywność. Do analizy ilościowej wykorzystywane są chromatogramy tworzone dla wąskiego wycinka widma (XIC, ang. Extracted Ion Chromatogram). Obejmuje on zazwyczaj 0,02 amu i pokrywają się z wartością m/z charakterystyczną dla badanego analitu. Zastosowanie wysokiej rozdzielczości znacząco zwiększa selektywność, co zostało przedstawione na rysunku 4.
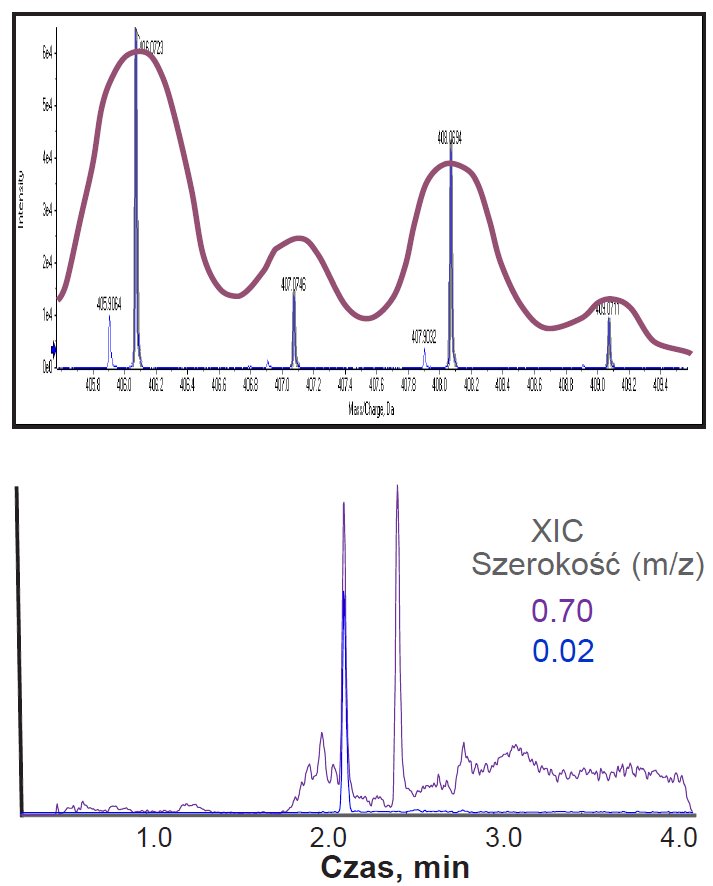
Rysunek 4. Na górze, nałożone na siebie widmo wysokiej i niskiej rozdzielczości. Na dole, Chromatogram dla wybranych jonów wykonany dla różnych szerokości próbkowania.
Taka metoda wykonywania oznaczeń ma kilka bardzo istotnych cech. Całe widmo wykonywane jest równocześnie i zbierane są informacje o wszystkich jonizujących się związkach. Możemy analizować dowolną ilość substancji, a tworzenie metody jest bardzo proste, gdyż definiujemy tylko ogólne parametry – takie same dla wszystkich związków. Ze względu na rejestrowanie całego widma istnieje możliwość powrotu do wcześniejszych wyników i retrospektywnej analizy danych w celu sprawdzenia, czy we wcześniej wykonanych pomiarach była obecna interesująca nas nowa substancja, która wcześniej nie była brana pod uwagę. Skoro zbieranie widma MS wysokiej rozdzielczości ma tak wiele zalet, to dlaczego nadal potrójne kwadrupole są najczęściej wykorzystywane w analizie ilościowej? Niestety, widmo MS nawet wysokiej rozdzielczości zapewnia zbyt niską selektywność. W obecnej chwili, rozdzielczość i stabilność kalibracji pozwalają na tworzenie XIC z rozdzielczością 10 ppm. Nawet gdyby spektrometry wysokiej rozdzielczości zapewniały możliwość tworzenia chromatogramów dla wybranych jonów z rozdzielczością 0,1 ppm, selektywność takiego trybu byłaby znacznie mniejsza niż przejść MRM (Rysunek 5).

Rysunek 5. Porównanie selektywności różnych metod obserwacji jonów. Symulacja została przeprowadzona dla peptydów powstałych w wyniku hydrolizy trypsyną białek drożdży. Po lewej stronie znajduje się wykres pokazujący zależności odsetka wszystkich dwukrotnie naładowanych peptydów posiadających unikalne przejścia MRM w zależności od ich ilości, przedstawione są wykresy dla różnych rozdzielczości ustawionej na pierwszym i drugim analizatorze masy. Z prawej strony pokazany jest odsetek takich peptydów posiadających 3 unikalne przejścia. Pierwsze dwie kolumny odpowiadają selektywności widma MS wysokiej rozdzielczości, trzecia odpowiada przejściu MRM o obniżonej rozdzielczości, kolejna to przejście SWATH, a ostatnia, najczęściej wykorzytywane przejścia MRM o jednostkowej (unit) rozdzielczości.
Do potwierdzenia tożsamości związku, wciąż niezbędne jest wykonanie widma fragmentacyjnego. Dodatkowo niezwykle istotna jest stabilność kalibracji spektrometru w trakcie wykonywania pomiaru. Niewielka zmiana, rzędu kilkudziesięciu ppm, może spowodować brak wykrycia związku lub niepoprawną identyfikację. O ile nowoczesne systemy wysokiej rozdzielczości nie mają z tym problemu przy analizie w trybie jonów dodatnich, lub ujemnych, o tyle zmiana polaryzacji w trakcie wykonywania pomiarów jest znacznie dłuższa niż w przypadku systemów kwadrupolowych. Przy jednoczesnym pomiarze w trybie jonów dodatnich i ujemnych oraz zachowaniu dokładności pomiaru masy do milionowych części wymaganych jest przynajmniej kilkuset milisekund na stabilizację systemu. Na systemach wysokiej rozdzielczości znacznie lepiej jest wykonywać osobno pomiary w każdym z trybów. Kolejna istotna różnica to zakres dynamiczny pomiarów. W spektrometrach typu TOF jaki i Orbitrap, przy sprzyjających warunkach, można uzyskać liniowość metody analitycznej w zakresie około 4 rzędów wielkości. Tryb MRM posiada więc większą selektywność niż widmo MS wysokiej rozdzielczości. Dodatkowo potrójne kwadrupole zapewniają większą czułość. Wynika to z wysokiej wydajności pracy analizatorów. Nie bez znaczenia jest też fakt, że w analizie MRM optymalizowane są parametry spektrometru dla każdego związku, jak zostało to wspomniane wcześniej. Jest to proces pracochłonny, ale zapewnia znacznie większą wydajność w transmisji jonów niż ogólne parametry w spektrometrach wysokiej rozdzielczości. Znacznie większa wydajność i większa selektywność umożliwia uzyskanie niższych limitów detekcji.

Rysunek 5. Porównanie selektywności różnych metod obserwacji jonów. Symulacja została przeprowadzona dla peptydów powstałych w wyniku hydrolizy trypsyną białek drożdży. Po lewej stronie znajduje się wykres pokazujący zależności odsetka wszystkich dwukrotnie naładowanych peptydów posiadających unikalne przejścia MRM w zależności od ich ilości, przedstawione są wykresy dla różnych rozdzielczości ustawionej na pierwszym i drugim analizatorze masy. Z prawej strony pokazany jest odsetek takich peptydów posiadających 3 unikalne przejścia. Pierwsze dwie kolumny odpowiadają selektywności widma MS wysokiej rozdzielczości, trzecia odpowiada przejściu MRM o obniżonej rozdzielczości, kolejna to przejście SWATH, a ostatnia, najczęściej wykorzytywane przejścia MRM o jednostkowej (unit) rozdzielczości.
Do potwierdzenia tożsamości związku, wciąż niezbędne jest wykonanie widma fragmentacyjnego. Dodatkowo niezwykle istotna jest stabilność kalibracji spektrometru w trakcie wykonywania pomiaru. Niewielka zmiana, rzędu kilkudziesięciu ppm, może spowodować brak wykrycia związku lub niepoprawną identyfikację. O ile nowoczesne systemy wysokiej rozdzielczości nie mają z tym problemu przy analizie w trybie jonów dodatnich, lub ujemnych, o tyle zmiana polaryzacji w trakcie wykonywania pomiarów jest znacznie dłuższa niż w przypadku systemów kwadrupolowych. Przy jednoczesnym pomiarze w trybie jonów dodatnich i ujemnych oraz zachowaniu dokładności pomiaru masy do milionowych części wymaganych jest przynajmniej kilkuset milisekund na stabilizację systemu. Na systemach wysokiej rozdzielczości znacznie lepiej jest wykonywać osobno pomiary w każdym z trybów. Kolejna istotna różnica to zakres dynamiczny pomiarów. W spektrometrach typu TOF jaki i Orbitrap, przy sprzyjających warunkach, można uzyskać liniowość metody analitycznej w zakresie około 4 rzędów wielkości. Tryb MRM posiada więc większą selektywność niż widmo MS wysokiej rozdzielczości. Dodatkowo potrójne kwadrupole zapewniają większą czułość. Wynika to z wysokiej wydajności pracy analizatorów. Nie bez znaczenia jest też fakt, że w analizie MRM optymalizowane są parametry spektrometru dla każdego związku, jak zostało to wspomniane wcześniej. Jest to proces pracochłonny, ale zapewnia znacznie większą wydajność w transmisji jonów niż ogólne parametry w spektrometrach wysokiej rozdzielczości. Znacznie większa wydajność i większa selektywność umożliwia uzyskanie niższych limitów detekcji.
W celu uzyskania wysokiej rozdzielczości niezbędne jest więc zastosowanie trybu MS/MS. QqTOF i Q-Exactive są spektrometrami wyposażonymi w kwadrupolowy analizator masy, komorę zderzeń i analizator wysokiej rozdzielczości, odpowiednio TOF i Obritrap. Analizator kwadrupolowy wykorzystywany jest do wydajnej selekcji jonów kierowanych do wysokoenergetycznej fragmentacji. Drugi analizator masy służy do zebrania pełnego widma fragmentacyjnego. Jest to proces mniej wydajny niż transmisja wybranych jonów przez kwadrupol, ale w jego efekcie uzyskujemy pełne widmo fragmentacyjne o wysokiej rozdzielczości. W analizie ilościowej umożliwia to przyjęcie strategii polegającej na wykonywaniu pomiaru w oparciu o widmo MS wysokiej rozdzielczości, a widmo MS/MS służy do potwierdzenia tożsamości analitu. Jest to tak zwane zbieranie danych w zależności od uzyskanych informacji (IDA, ang. information dependent acquisition; lub DDA, ang. data dependent acquisition). Procedura pomiarowa polega na wykonaniu widma MS, a następnie dla najbardziej intensywnych sygnałów wykonywane jest widmo MS/MS. Umożliwia to obserwowanie bardzo dużej ilości związków (tysiące), ale w niezbyt skomplikowanych matrycach. Bardzo dobrym przykładem jest analiza farmaceutyków i środków higieny osobistej w wodzie (PPCP, ang. pharmaceutical, personal care products). Im bardziej skomplikowana jest matryca, tym relatywnie niska selektywność analizatora TOF bardziej utrudnia pomiar ilościowy. W takim wypadku, aby wykonać analizę ilościową wykonuje się widma fragmentacyjne dla zdefiniowanych jonów pseudomolekularnych, a następnie tworzone są chromatogramy dla wąskiego wycinka widma fragmentacyjnego. W ten sposób możemy monitorować wybrane reakcje fragmentacji z wysoką rozdzielczością.
Przejścia MRMHR (ang. high-resolution multiple reaction monitoring) są jeszcze bardziej selektywne niż ich odpowiedniki z potrójnego kwadrupola. Przydatne są w aplikacjach gdzie mamy do czynienia z bardzo skomplikowaną matrycą, np. analiza peptydów w surowicy. Metoda ta jednak jest pracochłonna – dla każdego związku musimy zdefiniować parametry reakcji fragmentacji. Dodatkowo, umożliwia obserwację tylko ograniczonej ilości analitów. Należy również pamiętać, że z powodu mniejszej wydajności analizatorów wysokiej rozdzielczości, charakteryzują się one niższą czułością.
Jak omówione zostało wcześniej, spektrometry wysokiej rozdzielczości z pojedynczym analizatorem mas mają wiele zalet: łatwość tworzenia metody, nieograniczona ilość analitów, retrospektywna analiza danych. Niestety z powodu zbyt niskiej selektywności są mało przydatne do analizy ilościowej. Z drugiej strony, systemy MS/MS są już wystarczająco selektywne, ale wciąż charakteryzują się pewnymi ograniczeniami pod kątem analizy ilościowej. Rozwiązaniem wydaje się być tryb pracy zwany zbieraniem danych niezależnym od informacji (DIA, ang. data indipendent acquisition). Coraz więcej producentów spektrometrów mas stara się wprowadzić to rozwiązanie. Polega ono na wykonywaniu fragmentacji wszystkich jonizujących się analitów. Obecnie wydaje się, że najbardziej zaawansowane rozwiązanie posiada firma SCIEX. Metoda ta została nazwana SWATH (ang. sequential window acquisition of all theoretical fragment-ion spectra) i jest coraz częściej wykorzystywana. Aby możliwe było wykonanie fragmentacji wszystkich jonizujących się analitów i zachowanie niezbyt długiego czas trwania pojedynczego cyklu (sekundy) należy zmodyfikować pracę pierwszego analizatora masy. W metodach opisanych do tej pory do komory zderzeń dostawały się wybrane jony z rozdzielczością jednostkową. W przypadku metody SWATH cały zakres jonów prekursorowych dzielony jest na okna, zazwyczaj o szerokości 25 amu. Fragmentacji nie są poddawane pojedyncze substancje, ale cała grupa analitów o wartościach m/z odpowiadających ustawieniu kwadrupola.
Wszystkie te jony ulegają równocześnie fragmentacji i zbierane jest uwspólnione widmo fragmentacyjne. Ten proces powtarzany jest dla kolejnych okien, tak aby pokryty został cały zakres m/z interesujących nas jonów prekursorowych. W trakcie każdego cyklu zbierane jest również widmo MS wysokiej rozdzielczości. W efekcie pomiaru otrzymujemy bardzo dużą ilość niezwykle skomplikowanych widm fragmentacyjnych.
Należy pamiętać, że pomiar ten nie jest wykonywany w celu identyfikacji związków, lecz ich analizy ilościowej. Aby utworzyć chromatogram dla wybranych związków najpierw odnajdujemy, w którym oknie znajduje się masa jonu pseudomolekularnego analizowanego związku. Następnie z widma fragmentacyjnego z wysoką rozdzielczością (10 ppm) tworzony jest chromatogram dla jonów fragmentacyjnych. W ten sposób, bez definiowana przed pomiarem przejść MRM, jesteśmy w stanie uzyskać przejścia charakterystyczne dla fragmentacji związku z zebranych za pomocą metody SWATH danych. Różnica w stosunku do tradycyjnych MRM-ów jest taka, że pierwszy analizator jest mniej selektywny, natomiast drugi znacznie bardziej selektywny niż w przypadku potrójnego kwadrupola. Z symulacji przeprowadzonych dla bardzo złożonych próbek wynika, że selektywność pomiarów metody SWATH jest bardzo zbliżona do selektywności MRM (Rysunek 5).
Stosowanie metody SWATH, lub ogólnie DIA, ma największy sens wtedy, gdy interesuje nas profilowanie stężeń względnych wielu analitów i śledzenie jak zmienia się to stężenie w różnych próbkach. Nie jest on jednak najlepszym rozwiązaniem do pomiaru bezwzględnej wartości stężenia analitu. SWATH został opracowany z myślą o aplikacjach proteomicznych, lecz obecnie stosowany jest już w profilowaniu metabolitów, toksykologii, kryminalistyce oraz analizie próbek środowiskowych.
Stosowanie metody SWATH, lub ogólnie DIA, ma największy sens wtedy, gdy interesuje nas profilowanie stężeń względnych wielu analitów i śledzenie jak zmienia się to stężenie w różnych próbkach. Nie jest on jednak najlepszym rozwiązaniem do pomiaru bezwzględnej wartości stężenia analitu. SWATH został opracowany z myślą o aplikacjach proteomicznych, lecz obecnie stosowany jest już w profilowaniu metabolitów, toksykologii, kryminalistyce oraz analizie próbek środowiskowych.
Podsumowując tą część artykułu należy stwierdzić, że nadal w przypadku analizy ilościowej nie więcej niż kilkudziesięciu związków, potrójne kwadrupole są najlepszym narzędziem do takich pomiarów. Czym więcej związków chcemy obserwować, tym bardziej przydatne mogą być tandemowe systemy wysokiej rozdzielczości takie jak QqTOF lub Q-Exactive. Jeśli chcemy obserwować więcej niż 1000 analitów, spektrometry wysokiej rozdzielczości są właściwie jedynym rozwiązaniem. Należy jednak pamiętać, że oprócz samej metodyki pomiarowej w przypadku analizy ilościowej należy wykonać walidację metody analitycznej. Jest ona bardzo czasochłonna w przypadku metod opartych o przejścia MRM dla kilkuset związków. Proces walidacji utrudnia również fakt, że przy tak wielu analitach nie stosuje się już wzorca znakowanego izotopem dla każdej badanej substancji. W przypadku większej ilości związków i zastosowania spektrometrów wysokiej rozdzielczości przestaje być to analiza ilościowa, a staje się raczej monitorowaniem obecności związku o stężeniu przekraczającym założoną wartość, lub profilowaniem względnego stężenia związków. W przypadku stosowania spektrometrów wysokiej rozdzielczości w trakcie pomiaru wykonuje się widmo MS. Umożliwia to stwierdzenie obecności wszystkich jonizujących się analitów a nie tylko tych, dla których zdefiniowane są przejścia MRM (tryb MRM).
Nowoczesne spektrometry są coraz bardziej czułe, co powoduje że selektywność trybu MRM jest często zbyt niska. Sygnał interesującego nas analitu, albo pokrywa się z interferującymi sygnałami, albo w ogóle jest niewidoczny z powodu zbyt wysokiego tła. Oprócz wspomnianej wcześniej bardziej selektywnej metody przygotowania próbki, lub zastosowania trybu MRMHR, dostępne są nowe rozwiązania zwiększające selektywność systemu LC/MS/MS.
Spektrometry typu QTRAP są potrójnymi kwadrupolami, w których drugi analizator masy może działać jak kwadrupol lub pułapka jonowa; możliwe jest także zastosowanie trybu MRM3. Pierwszy analizator mas wybiera jon pseudomolekularny analitu z wysoką wydajnością, zaś w komorze zderzeń ulegają one wysokoenergetycznej fragmentacji. stosowanie jej ma sens tylko wtedy, gdy tryb MRM. Wszystkie fragmenty są wyłapywane przez pułapkę jonową, a następnie wybrany jon fragmentacyjny poddawany jest kolejnej fragmentacji. Do analizy ilościowej wykorzystywany jest jeden lub suma kilku fragmentów powstających w drugim stopniu fragmentacji. Dzięki temu w znaczący sposób zwiększymy selektywność pomiaru. Taki sposób prowadzenia pomiaru jest mniej wydajny niż obserwacja przejścia MRM, ale z powodu większej selektywności, w przypadku skomplikowanych matryc, może pomóc w uzyskaniu niższych limitów oznaczalności. Ponieważ przed pułapką jonową znajduje się analizator kwadrupolowy, w przypadku trybu MRM3 na spektrometrach typu QTRAP, jest bardzo niskie prawdopodobieństwo przeładowania pułapki. Metoda ta ma więc dobry zakres dynamiczny i zapewnia bardzo dobrą powtarzalność pomiarów. Należy jednak pamiętać, że jest zbyt mało selektywny.
Druga metoda zwiększenia selektywności to zastosowanie dodatkowego filtra rozdzielającego jony na podstawie ich przekroju czynnego, czyli przystawki wykorzystującej spektrometrię ruchliwości jonów. Technika ta została opisana w osobnym artykule. W analizie ilościowej największe zastosowanie ma różnicowa spektrometria ruchliwości jonów (DMS, ang. differential mobility spectrometry w przypadku firmy SCIEX; lub FAIMS, ang. field asymmetric waveform ion mobility spectrometry w przypadku firmy Thermo i Owlstone, są to dwie nazwy technik wykorzystujące tą samą zasadę działania). Niezależnie od nazwy, urządzenia te działają na zasadzie filtra, który dla zadanych parametrów przepuszcza jony o danym przekroju czynnym. Przystawka ta umieszczona jest między źródłem jonów a próżniową częścią spektrometru mas. Dzięki zastosowaniu spektrometrii ruchliwości jonów zwiększa się selektywność całego zestawu LC/MS/MS. Proces ten poprawia selektywność detekcji wybranych analitów, ale jednocześnie pogarsza wydajność całego systemu. Tak jak w przypadku MRM3, jego zastosowanie ma sens gdy tradycyjne przejścia MRM mają zbyt niską selektywność. Spektrometria ruchliwość jonów może również w niektórych przypadkach, szczególnie gdy matryca nie jest zbyt skomplikowana, zastąpić rozdzielenie chromatograficzne związków i dzięki temu umożliwić znaczące skrócenie czasu analizy.
Zapraszam do zadawania pytań:
tomasz.bienkowski@msekspert.
Zapraszam do zadawania pytań:
tomasz.bienkowski@msekspert.






