Keith A. Porter, E. Keller Barnhardt, Jonathan M. Collins, Michael J. Karney
CEM Corporation
strony wersji drukowanej: 40-42
strony wersji drukowanej: 40-42

Istotnymi problemami występującym podczas syntezy peptydów na nośniku stałym (SPPS, ang. Solid Phase Peptide Synthesis) są agregacja łańcuchów peptydowych oraz słaba ich solwatacja prowadzące do niekompletnej deprotekcji i/lub acylowania. Rezultatem tego jest niski stopień czystości produktów syntezy. [1] Występowanie tego zjawiska nasila się w przypadku długich sekwencji aminokwasów oraz peptydów zawierających wiele reszt hydrofobowych, dla których w wyniku wspomnianej agregacji, wydajności dla etapów deprotekcji oraz kondensacji ulegają drastycznemu obniżeniu. Późniejsze oczyszczanie surowej mieszaniny peptydów staje się zadaniem złożonym i czasochłonnym, często wymagającym kilkukrotnego zastosowania technik chromatograficznych, co prowadzi do redukcji wydajności dla pożądanego peptydu. [2] 

Zastosowanie promieniowania mikrofalowego podczas syntezy peptydów przyczyniło się do obniżenia stopnia agregacji, zwiększenia czystości produktu, oraz skrócenia czasu syntezy. [3] Ostatnimi czasy, ulepszono sposób aplikacji mikrofal oraz zwielokrotniono korzyści płynące z takowego wspomagania, opracowując metodę wysokowydajnej syntezy peptydów na nośniku stałym (HE-SPPS, ang. High Efficiency SPPS). Udoskonalenie pod postacią HE-SPPS, dotyczy aspektu chemicznego oraz aparatury, czego efektem jest zniwelowanie problemu powstających produktów ubocznych, przy jednoczesnej redukcji czasu trwania cyklu syntezy do 4 minut, a także o 90% niższej produkcji odpadów poreakcyjnych. [4] Syntezator peptydów Liberty Blue™, został zaprojektowany by zautomatyzować metodę HE-SPPS, co w efekcie pozwala na zsyntezowanie peptydu złożonego z piętnastu aminokwasów w przeciągu godziny przy zachowaniu wysokiej czystości produktu oraz minimalnym zużyciu rozpuszczalników.
Dobrze znany jest wpływ właściwości żywicy na jakość peptydu otrzymywanego za pomocą SPPS. Z tego powodu poszukiwaliśmy udoskonalonej żywicy opierając się na poprawie efektu końcowego syntezy realizowanej za pomocą automatycznego mikrofalowego syntezatora peptydów Liberty Blue™ przy zastosowaniu metody HE-SPPS. W naszym badaniu skupiliśmy się na żywicach SpheriTide®, które są wyjątkowe w porównaniu do tradycyjnych żywic na bazie polistyrenu i PEG. Składają się one z poli-ε-lizyny niecałkowicie usieciowanej homobifunkcyjnymi kwasami karboksylowymi, co zapewnia występowanie w środowisku reakcji wiązań amidowych podobnych do tych obecnych w łańcuchu peptydowym. W rezultacie otrzymano hydrofilowy, peptydopodobny szkielet, który umożliwia obniżenie tendencji do tworzenia się wewnątrzcząsteczkowych agregatów. Dodatkowo wydłużane łańcuchy peptydowe są związane z grupami α-aminowymi, które ze względu na wysoce wyspecjalizowany charakter żywicy SpheriTide® są rozmieszczone w minimalnej odległości od siebie. Pozwala to na uniknięcie tworzenia się klastrów pomiędzy linkerami, umożliwiając syntezę prowadzącą do produktu o wysokim stopniu czystości nawet przy osadzeniu żywicy większym niż 1 mmol/g.
Końcowym etapem podczas otrzymywania wysokiej czystości peptydu jest jego odszczepienie od nośnika. Zastosowanie rozwiązania oferowanego przez Accent™ Peptide Cleavage System, umożliwia odszczepienie peptydu w skali mikro by kontrolować postęp podczas skomplikowanej syntezy, a także w pełnej skali po jej zakończeniu. W przeciwieństwie do techniki tradycyjnej, dzięki urządzeniu Accent™ można dokonać “mikroodszczepienia” w przeciągu zaledwie 2 minut, zaś w przypadku skali makro czas ten nie przekracza 30 minut.
W celu przetestowania żywicy SpheriTide® i dokładniejszego zbadania metody HE-SPPS przy wykorzystaniu syntezatora Liberty BlueTM, wyselekcjonowano do syntezy dwa peptydy. EGFRvIII i 1-42β-amyloid zostały wybrane ze względu na ich złożoną syntezę, która nastręcza licznych problemów. Peptydy zostały początkowo zsyntezowane na żywicy bazującej na polistyrenie, a następnie na żywicy Rink amide SpheriTide® zarówno o niskim jak i wysokim stopniu osadzenia.
Wyniki
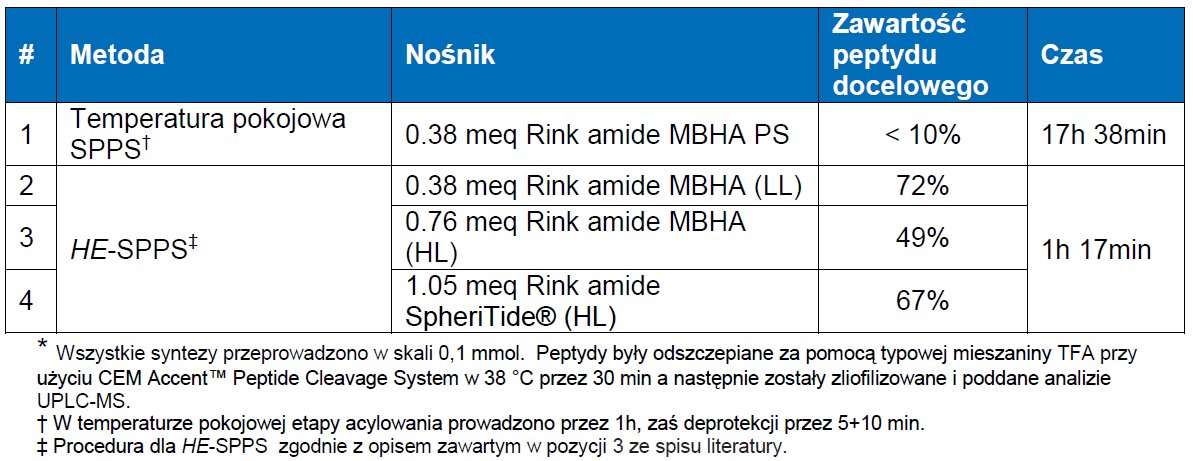
EGFRvIII (LEEKKGNYVVTDHC) został zsyntezowany w celu porównania HE-SPPS z syntezą na nośniku stałym w temperaturze pokojowej. Synteza prowadzona w standardowej temperaturze pokojowej na żywicy Rink amide MBHA PS o niskim stopniu osadzenia (osadzenie 0,38 mmol/g) dała w rezultacie śladowe ilości produktu. Jest to zgodne z uprzednio opublikowanymi wynikami badań, gdzie każdorazowo po etapie sprzęgania wymagana była kilkukrotna deprotekcja (w niektórych przypadkach do ośmiu powtórzeń), zaś czas sprzęgania przekraczał 12 godzin, co w efekcie doprowadziło do uzyskania surowych produktów, których czystość wynosiła od 40 do 70%. [5] Wykorzystanie tej samej żywicy w warunkach HE-SPPS umożliwiło otrzymanie produktu o czystości 72% w nieco ponad godzinę.
Żywica Rink amide SpheriTide® o wyższym stopniu osadzenia (osadzenie 1,05 mmol/g) okazała się najkorzystniejsza, umożliwiła osiągnięcie tych samych rezultatów co uprzednio opisana, a to wskazuje, że unikalne właściwości tej żywicy pozwalają jej konkurować z żywicami słabiej osadzonymi w przypadku pewnych problematycznych sekwencji aminokwasowych. Wysoką czystość surowego produktu otrzymanego na żywicy o znacznym stopniu osadzenia można przypisać (1) hydrofilowemu charakterowi żywicy, co zapobiega agregacji wewnątrz łańcucha syntezowanego peptydu oraz (2) równomiernemu rozmieszczeniu miejsc inicjacji reakcji kondensacji.
Tabela 1. Podsumowanie rezultatów dla przeprowadzonych syntez EGFRvIII *
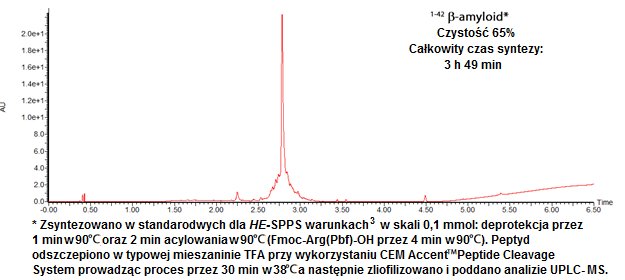
W celu wykazania uniwersalności metody HE-SPPS oraz żywicy SpheriTide®, zsyntezowano szczególnie kłopotliwą i złożoną sekwencję 1-42β-amyloidu (DAEFRHDSGYEVHHQKLVFFAEDVGSNKGAIIGLMVGGVVIA). 1-42β-amyloid jest uważany za wyzwanie zarówno w kontekście syntezy chemicznej jak i analizy. Stosując żywicę Rink amide SpheriTide® (LL) (osadzenie 0,17 mmol/g) otrzymano produkt o czystości 65%, co określono za pomocą UPLC-MS.
Wnioski
Żywica SpheriTide® w połączeniu z techniką HE-SPPS oraz syntezatorem Liberty Blue™ pozwala na otrzymanie wysokiej czystości peptydów w krótkim czasie. Po zakończeniu syntezy peptyd może być z łatwością oraz wysoką wydajnością odszczepiony od żywicy przy użyciu systemu Accent™. Nawet trudne sekwencje aminokwasów mogą być otrzymane efektywnie oraz z zadowalającą czystością surowego produktu.
Literatura:
1. Rovero, P. In Solid Phase Synthesis. A Practical Guide; Kates, S. A.; Albericio, F., Eds.; Marcel Dekker: New York, 2000; Chapters 1-6.
2. Quibell, M.; Johnson, T. In Fmoc Solid Phase Peptide Synthesis. A Practical Approach; W. C. Chan, P. D. White, (Eds.); Oxford University Press: New York, 2000; Chapters 1-2.
3. References include: (a)Yu, H. M.; Chen, S. T.; Wang, K. T.; J. Org. Chem., 1992, 57, 4781. (b) Erdélyi, M.; Gogoll, A.; Synthesis, 2002, 11, 1592. (c) Vanier, G. S. In Microwave Heating as a Tool for Sustainable Chemistry; Leadbeater, N. E., Ed.; CRC Press: Boca Raton, FL, 2010; Chapter 9, p 231. (d) Palasek, S. A.; Cox, Z. J.; Collins, J. M.; J. Pept. Sci., 2007, 13, 143. (e) Collins, J. M. Microwaves in Organic Synthesis, 3rd ed.; Hoz, A., Loupy, A., Eds.; Wiley-VCH: Weinheim, Germany, 2013; Vol. 2, Chapter 20, p 897.
4. Collins, J.M.; Porter, K.A.; Singh, S.K.; Vanier, G.S.; Org. Lett., 2014, 16, 940.
5. Finneman, J.I.; Pozzo, M. J.; J. Pep. Sci. 2012, 8, 511.
SpheriTide® jest zarejestrowanym znakiem towarowym SpheriTech Ltd.
Kontakt:
Michael Karney
Life Science Product Manager
Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript.
www.cempeptides.com





