Laboratorium Masdiag
strony wersji drukowanej: 7-21

W latach 80-tych, gdy powstał pierwszy spektrometr mas typu potrójny kwadrupol, zostały wykonane badania potencjału tej technologii. W powstałym raporcie szacowana ilość sprzedanych urządzeń wynosiła kilkanaście sztuk rocznie na całym świecie. Mimo niezbyt obiecujących perspektyw zdecydowano się na rozpoczęcie produkcji i sprzedaż.  Pierwszymi użytkownikami techniki LC-MS/MS były duże firmy farmaceutyczne. Tylko one miały odpowiednie środki, aby zainwestować w tego rodzaju technologię oraz dostrzegły jej potencjał. Potrójny kwadrupol sprzężony z wysokosprawnym chromatografem cieczowym okazał się idealnym urządzeniem umożliwiającym analizę ilościową polarnych związków organicznych w skomplikowanej matrycy jaką jest krew. Tak rozpoczął się rozwój techniki LC-MS/MS. W obecnej chwili technika ta jest wykorzystywana w bardzo wielu różnorodnych aplikacjach i ciągle się rozwija. Pojawiają się nowe rodzaje spektrometrów mas, są one wciąż udoskonalane. Jedną z najważniejszych aplikacji jest analiza ilościowa. Wszędzie tam, gdzie z dużą pewnością i szybko należy oznaczyć wybrany analit lub cały ich panel, system składający się ze spektrometru typu potrójny kwadrupol i wysokosprawnego chromatografu cieczowego jest najlepszym rozwiązaniem. Dlatego też coraz bardziej powszechne jest wykorzystanie techniki LC-MS/MS w diagnostyce laboratoryjnej, gdzie rutynowo stosuje się ją do analizy ilościowej różnorodnych biomarkerów.
Pierwszymi użytkownikami techniki LC-MS/MS były duże firmy farmaceutyczne. Tylko one miały odpowiednie środki, aby zainwestować w tego rodzaju technologię oraz dostrzegły jej potencjał. Potrójny kwadrupol sprzężony z wysokosprawnym chromatografem cieczowym okazał się idealnym urządzeniem umożliwiającym analizę ilościową polarnych związków organicznych w skomplikowanej matrycy jaką jest krew. Tak rozpoczął się rozwój techniki LC-MS/MS. W obecnej chwili technika ta jest wykorzystywana w bardzo wielu różnorodnych aplikacjach i ciągle się rozwija. Pojawiają się nowe rodzaje spektrometrów mas, są one wciąż udoskonalane. Jedną z najważniejszych aplikacji jest analiza ilościowa. Wszędzie tam, gdzie z dużą pewnością i szybko należy oznaczyć wybrany analit lub cały ich panel, system składający się ze spektrometru typu potrójny kwadrupol i wysokosprawnego chromatografu cieczowego jest najlepszym rozwiązaniem. Dlatego też coraz bardziej powszechne jest wykorzystanie techniki LC-MS/MS w diagnostyce laboratoryjnej, gdzie rutynowo stosuje się ją do analizy ilościowej różnorodnych biomarkerów.
 Pierwszymi użytkownikami techniki LC-MS/MS były duże firmy farmaceutyczne. Tylko one miały odpowiednie środki, aby zainwestować w tego rodzaju technologię oraz dostrzegły jej potencjał. Potrójny kwadrupol sprzężony z wysokosprawnym chromatografem cieczowym okazał się idealnym urządzeniem umożliwiającym analizę ilościową polarnych związków organicznych w skomplikowanej matrycy jaką jest krew. Tak rozpoczął się rozwój techniki LC-MS/MS. W obecnej chwili technika ta jest wykorzystywana w bardzo wielu różnorodnych aplikacjach i ciągle się rozwija. Pojawiają się nowe rodzaje spektrometrów mas, są one wciąż udoskonalane. Jedną z najważniejszych aplikacji jest analiza ilościowa. Wszędzie tam, gdzie z dużą pewnością i szybko należy oznaczyć wybrany analit lub cały ich panel, system składający się ze spektrometru typu potrójny kwadrupol i wysokosprawnego chromatografu cieczowego jest najlepszym rozwiązaniem. Dlatego też coraz bardziej powszechne jest wykorzystanie techniki LC-MS/MS w diagnostyce laboratoryjnej, gdzie rutynowo stosuje się ją do analizy ilościowej różnorodnych biomarkerów.
Pierwszymi użytkownikami techniki LC-MS/MS były duże firmy farmaceutyczne. Tylko one miały odpowiednie środki, aby zainwestować w tego rodzaju technologię oraz dostrzegły jej potencjał. Potrójny kwadrupol sprzężony z wysokosprawnym chromatografem cieczowym okazał się idealnym urządzeniem umożliwiającym analizę ilościową polarnych związków organicznych w skomplikowanej matrycy jaką jest krew. Tak rozpoczął się rozwój techniki LC-MS/MS. W obecnej chwili technika ta jest wykorzystywana w bardzo wielu różnorodnych aplikacjach i ciągle się rozwija. Pojawiają się nowe rodzaje spektrometrów mas, są one wciąż udoskonalane. Jedną z najważniejszych aplikacji jest analiza ilościowa. Wszędzie tam, gdzie z dużą pewnością i szybko należy oznaczyć wybrany analit lub cały ich panel, system składający się ze spektrometru typu potrójny kwadrupol i wysokosprawnego chromatografu cieczowego jest najlepszym rozwiązaniem. Dlatego też coraz bardziej powszechne jest wykorzystanie techniki LC-MS/MS w diagnostyce laboratoryjnej, gdzie rutynowo stosuje się ją do analizy ilościowej różnorodnych biomarkerów.Pojawia się pytanie dlaczego to właśnie spektrometry typu potrójny kwadrupol są najbardziej popularne w diagnostyce i ogólniej w analizie ilościowej? Aby na nie odpowiedzieć trzeba wyjaśnić jak działa spektrometr mas.
Schemat spektrometru mas przedstawiony jest na rysunku 1.
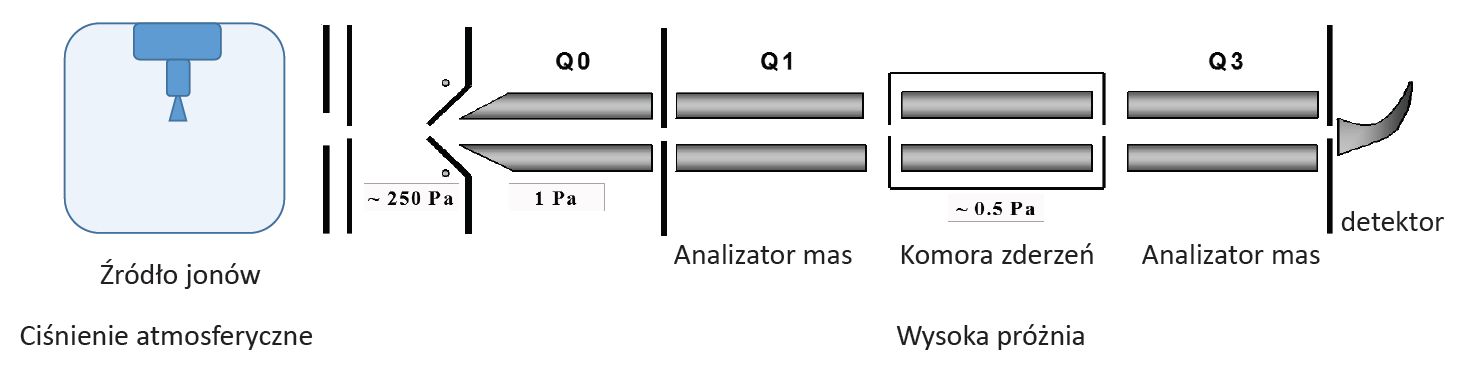
Rys. 1. Budowa spektrometru mas (Na przykładzie potrójnego kwadrupola).
Pierwszym etapem jest zjonizowanie analizowanych substancji pod ciśnieniem atmosferycznym. Następnie jony przenoszone są do części spektrometru znajdującej się pod wysoką próżnią, w której znajdują się analizatory masy. Służą one do analizowania/rozdzielania jonów na podstawie ich stosunku masy do ładunku (m/z - mass to charge ratio). W zależności od trybu pracy spektrometru jony po rozdzieleniu trafiają do detektora lub komory zderzeń. W komorze zderzeń ulegają, wywołanej zderzeniem, fragmentacji (CID – Collision Induced Dissociation). Powstałe fragmenty jonowe są ponownie rozdzielane na podstawie ich stosunku masy do ładunku przez drugi analizator mas i trafiają do detektora. Rodzaj detektora zależy od typu stosowanego analizatora mas.
Najważniejszymi etapami decydującymi o prawidłowym doborze spektrometru mas do aplikacji są metoda jonizacji oraz rodzaj wykorzystanych analizatorów mas.
Metody jonizacji
W komercyjnie dostępnych systemach LC-MS/MS wykorzystywane są trzy metody jonizacji działające pod ciśnieniem atmosferycznym. Najczęstszą metodą jest elektrosprej (ESI - Electrospray). W metodzie tej jony przenoszone są z fazy ciekłej do fazy gazowej. Analizowane związki choć w niewielkim stopniu muszą więc być zjonizowane w fazie ciekłej. Wydajność metody elektrosprej jest tym lepsza im bardziej polarny jest związek. Kolejną metodą jest jonizacja chemiczna pod ciśnieniem atmosferycznym (APCI – Atmosferic Pressure Chemical Ionization). W tej metodzie jony wytwarzane są w fazie gazowej. Umożliwia to wydajne zjonizowanie mniej polarnych związków, takich jak ergokalcyferol i cholekalcyferolu (odpowiednio witamina D2 i D3). Metodą umożliwiającą zjonizowanie najmniej polarnych związków jest fotosprej (APPI - Atmosferic Pressure Photo Ionization). W typ przypadku jony wytwarzane są również w fazie gazowej. Metodę tą można wykorzystywać np. w oznaczaniu paneli hormonów sterydowych. Pierwszym etapem jonizacji w APCI i APPI jest całkowite odparowanie rozpuszczalnika, co powoduje że cząsteczki analitu narażone są na stres termiczny. Ogranicza to możliwość stosowania tych typów jonizacji do związków odpornych na działanie podwyższonej temperatury i maksymalnej masie cząsteczkowej do około 1000 daltonów. Z opisanych powyżej metod najłagodniejszym sposobem jonizacji jest elektrosprej. Umożliwia jonizację termolabilnych i największych cząsteczek. Zakres zastosowania opisanych metod w zależności od polarności i wielkości cząsteczek przedstawia rysunek 2.
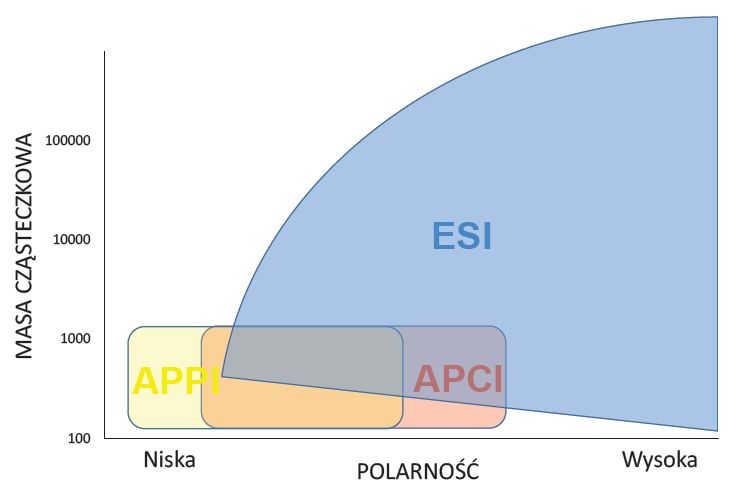
Rys. 2. Zakres optymalnych wydajności jonizacji pod ciśnieniem atmosferycznym.
Należy pamiętać, że większość związków jonizuje się przy wykorzystaniu wszystkich metod. Jednakże w zależności od polarności związku i jego masy cząsteczkowej jedna z tych metod jest najbardziej optymalna. Wydajność jonizacji zależy od bardzo wielu czynników i wprowadza to pewną zmienność wyników. W metodach LC-MS/MS metodę uważa się za bardzo dobrą jeśli współczynnik zmienności jest mniejszy niż 5%.
Rodzaje Analizatorów Mas
Kwadrupol jest najczęściej wykorzystywanym analizatorem w tandemowych spektrometrach mas. Działa w sposób ciągły, przepuszczając jony o danym stosunku masy do ładunku. Może on pracować w dwóch trybach: skanowania, gdy wykonywane jest pełne widmo oraz w trybie obserwacji wybranych jonów, gdy rejestrowana jest intensywność wybranego jonu w czasie. Skanowanie udziela informacji o składzie badanej próbki. Analizator kwadrupolowy w tym trybie działa z bardzo małą wydajnością, mniej niż 0,1% jonów dociera do detektora. Z kolei w trybie obserwacji wybranych jonów kwadrupol działa z maksymalną wydajnością i zapewnia największą czułość wykonywanych pomiarów. Jest to najczulszy tryb pracy spektrometrów mas, który umożliwia największy stopień wykorzystania jonów.
Analizator czasu przelotu (TOF - Time of Flight) działa w sposób okresowy. Stosunek masy do ładunku jest wyliczany na podstawie czasu przelotu jonu przez analizator. Jony przyspieszane są poprzez przyłożenie potencjału. Jony o mniejszej wartości stosunku masy do ładunku uzyskują większą prędkość i dolatują do detektora szybciej. Czas przelotu przez analizator można zmierzyć z bardzo dużą dokładnością i wyznaczyć dokładną masę jonów. W spektrometrach wyposażonych w źródło pracujące pod ciśnieniem atmosferycznym, w którym jony powstają w sposób ciągły analizator TOF umieszczony jest pod kątem prostym w stosunku do pozostałych elementów optyki jonowej (Rysunek 3.).
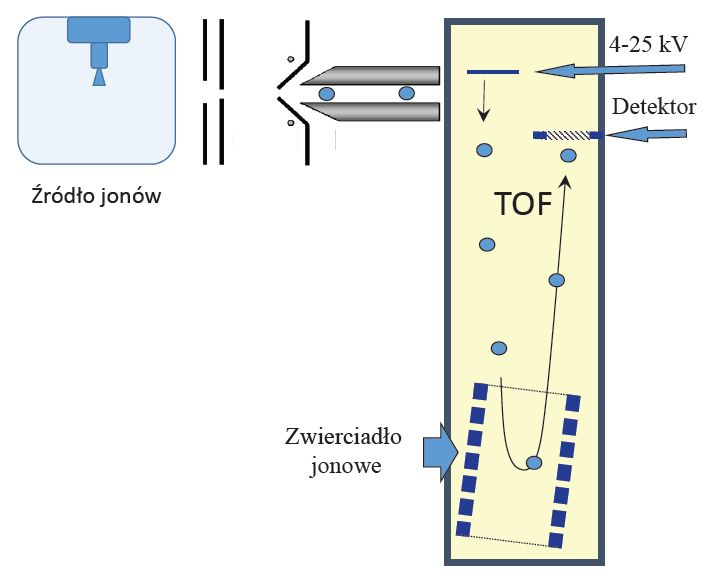
Rys. 3. Budowa spektrometru mas typu API-TOF.
Powstające w źródle jony ogniskowane są w skupioną wiązkę, która jest wysyłana przez przyłożenie potencjału do analizatora TOF pod kątem prostym. Poprzez zastosowanie takiego rozwiązania możliwy jest dokładniejszy pomiar czasu przelotu jonów w analizatorze, ponieważ prędkość jonów w osi źródła jonów nie wpływa na czas przelotu przez analizator TOF. Współczesne analizator TOF umożliwia wykonywania widm z wysoką rozdzielczością spektralną i mierzenie stosunku masy do ładunku z dokładnością do kilku ppm i zapewnia wysoką czułość.
Pułapka jonowa również działa w sposób okresowy. Przez pewien czas wyłapuje powstające w źródle jony, a następnie jest selektywnie opróżniana, tzn. usuwane są z niej po kolei jony o zdefiniowanym stosunku masy do ładunku. Pułapka jonowa umożliwia również wykonywanie fragmentacji. Po wyłapaniu wszystkich powstających w źródle jonów, jest ona selektywnie opróżniana, usuwane są wszystkie jony oprócz tych o wybranym do fragmentacji stosunku masy do ładunku. Następnie pozostające w pułapce naładowane cząsteczki są wzbudzane za pomocą fal o częstotliwości radiowej oraz podnoszone jest ciśnienie w pułapce i następuje fragmentacja, czyli rozpad badanych jonów na cząsteczki obojętne i jony. Ostatnim krokiem jest selektywne opróżnienie pułapki i zebranie widma jonów fragmentacyjnych. Proces ten można powtarzać wielokrotnie. Możliwość wykonywania kolejnych fragmentacji zależy od początkowej ilości jonów jak i wydajności fragmentacji.
Pułapka jonowa zapewnia wysoką czułość w trybie skanowania jak i badania reakcji fragmentacji. Jednakże działanie pułapki jonowej zależy od ilości powstających w źródle jonów. Im więcej różnorodnych substancji się jonizuje, tym łatwiej przeładować pułapkę co powoduje, że pomiary w skomplikowanych matrycach są mało powtarzalne.
Analizator mas wysokiej rozdzielczości z transformacją Fouriera jest kolejnym rodzajem wykorzystywanym w komercyjnie dostępnych spektrometrach mas (Orbitrap, FTICR-MS). Jest to analizator działający w sposób okresowy. Jest to bardzo złożony rodzaj analizatora mas, jego działanie w bardzo uproszczony sposób wygląda następująco. Jony wyłapywane są w pułapce o specjalnej konstrukcji. Dla poruszających się jonów rejestrowana jest funkcja falowa, z której za pomocą transformacji Fouriera uzyskiwane jest widmo masowe. Tego typu analizatory charakteryzują się możliwością uzyskania widma o bardzo wysokiej rozdzielczości. Dzieje się to jednakże kosztem czasu zbierania widma. Im dłuższy czas zbierania widma, tym możliwe jest uzyskanie większej rozdzielczości.
W tandemowym spektrometrze mas występują dwa analizatory mas oraz komora zderzeń. Umożliwia to wykonywanie pomiarów MS jak i MS/MS. W chwili obecnej na rynku dostępnych jest wiele różnorodnych spektrometrów umożliwiających pracę w trybie MS/MS. Najważniejsze z nich to:
- Potrójny Kwadrupol
- Pułapka jonowa
- QTRAP
- Spektrometry wysokiej rozdzielczości (typu QqTOF, Orbitrap, Q-Exactive)
Dostępne są również spektrometry mas z pojedynczym analizatorem mas, ale ze względu na ich małe możliwości aplikacyjne, nie zostaną opisane w tym artykule.
Potrójny kwadrupol
W przypadku potrójnego kwadrupola, dwa kwadrupolowe analizatory mas rozdzielone są komorą zderzeń. Komora zderzeń może mieć różną budowę. W pierwszych spektrometrach tego typu był to również kwadrupol i stąd wzięła się nazwa tego rodzaju spektrometru. Oba analizatory mas mogą pracować w dwóch trybach, zarówno w trybie skanowania jak i transmisji wybranych jonów. Daje to wiele możliwych trybów pracy całego systemu.
Skanowanie służy do wykonywania widma dla zdefiniowanego zakresu mas. Wykorzystywane jest w analizie jakościowej, gdy chcemy zmierzyć co znajduje się w próbce. Współczesne analizatory kwadrupolowe mogą skanować z dużą prędkością, nawet do kilkudziesięciu tysięcy daltonów na sekundę. Jednakże niezależnie jak szybko może skanować kwadrupol to z powodu niskiej czułości tryb skanowania przydatny jest w badaniu w bardzo prostych matrycach i dla analitów o relatywnie wysokich jak na spektrometrię mas stężeniach.
To samo dotyczy również wykonywania widm fragmentacyjnych MS/MS, gdy chcemy identyfikować związki. W trybie skanowania pierwszy kwadrupol działa z wysoką wydajnością wybierając jony o zdefiniowanej wartości m/z. W komorze zderzeń następuje wysokoenergetyczna i wydajna fragmentacja. Drugi analizator działa w trybie skanowania, co bardzo obniża czułość całego procesu.
Tandemowym trybem pracy, w którym potrójny kwadrupol działa z największą wydajnością jest obserwowanie wybranych reakcji fragmentacji (MRM/SRM – Multiple/Selected Reaction Monitoring). W pierwszym kwadrupolu w sposób ciągły wybierane są jony o zdefiniowanej wartości m/z. W komorze zderzeń następuje wysokoenergetyczna i wydajna fragmentacja, a drugi analizator kwadrupolowy przepuszcza tylko fragmenty o zdefiniowanej wartości m/z. Taka konfiguracja obu analizatorów ma dwie podstawowe zalety. Po pierwsze umożliwia rozpoznanie badanego analitu na podstawie reakcji fragmentacji, co bardzo zwiększa selektywność pomiaru. Ponadto oba analizatory mas działają w sposób ciągły i z maksymalną wydajnością filtrują jony. Jest to bardzo istotne przy pracy w skomplikowanych matrycach. Niezależnie od tego jak dużo jonów powstaje w źródle, badane jony są przepuszczane z maksymalną wydajnością, co umożliwia uzyskiwanie bardzo powtarzalnych pomiarów dla niskich stężeń analitu nawet w przypadku skomplikowanych matryc. W przypadku, gdy spektrometr mas działający w trybie MRM jest połączony z systemem HPLC w trakcie analizy uzyskujemy wykres intensywności badanej reakcji fragmentacji w czasie. Gdy badana substancja dostaje się do spektrometru intensywność sygnału pochodzącego od badanej reakcji fragmentacji zwiększa się i jej wartość jest proporcjonalna do stężenia badanej substancji. Pozwala to na wykonywanie pomiarów ilościowych. Dzięki wysokiej wydajności transmisji jonów intensywność sygnału jest duża, a dzięki wysokiej selektywności wartość szumów niska. W trybie MRM możliwe jest uzyskanie najlepszych wartości stosunku sygnału do szumu (S/N - Signal to Noise) na danym spektrometrze, a więc uzyskanie najlepszych limitów detekcji i oznaczalności (LOD - Limit of Detection i LOQ - Limit of Quantitation). Jest to najlepszy tryb do wykonywania pomiarów ilościowych. W większości rutynowych metod ilościowych w trybie MRM, aby zapewnić jak największą powtarzalność pomiaru, stosuje się wzorce znakowane stabilnymi izotopami. Są to związki o właściwościach chemicznych niemal identycznych jak badana substancja, jednakże z powodu zastosowania izotopów ich masa jest inna. Możliwe jest więc śledzenie ich stężenia za pomocą innego przejścia MRM. Wzorce izotopowe dodawane są na początku przygotowywania próbki. Dzięki temu niwelują one błędy wynikające z różnego odzysku analitu w procesie przygotowania próbki oraz ze zmienności efektywności jonizacji związków w źródle jonów.
Potrójny kwadrupol ma jeszcze dwa unikalne tryby skanowania. Jest to obserwowanie utraty cząsteczek obojętnych (neutral loss scan) i obserwowanie jonów macierzystych (precursor ion scan). Służą one do poszukiwania grup związków, które odpowiednio albo tracą charakterystyczną cząsteczkę obojętną lub w przypadku których w wyniku fragmentacji powstaje charakterystyczny fragment. W obu sytuacjach jako wynik pomiaru otrzymujemy wartość m/z jonu macierzystego. W trybach tych jeden lub oba kwadrupole skanują, zapewniają więc wysokoselektywne pomiary, ale o niskiej czułości. Obserwowanie jonów macierzystych było kiedyś bardzo popularne w badaniach przesiewowych noworodków (NBS – Newborn Screening).
Wraz z rozwojem potrójnych kwadrupoli i pojawieniem się szybkich komór zderzeń w chwili obecnej badania te wykonuje się już w trybie MRM. Zapewnia to lepszą jakość sygnału i z powodu wyższej czułości umożliwia pracę z mniejszą ilością materiału.
Pułapka jonowa
Pułapka jonowa nie jest tandemowym spektrometrem mas. Posiada tylko jeden analizator masy jednakże, jak było opisane wcześniej, za jej pomocą można zbierać widma zarówno MS jak i MS/MS. Można więc wykonywać podobne pomiary jak przy wykorzystaniu systemów tandemowych. Ten typ spektrometru charakteryzuje się wysoką czułością skanowania. Nadaje się więc do analizy jakościowej związków na niskim poziomie stężeń. Nie sprawdza się natomiast w analizie ilościowej. Za pomocą pułapki jonowej możliwe jest obserwowanie wybranych reakcji fragmentacji tak jak na spektrometrach typu potrójny kwadrupol. Pułapka jonowa wyposażona jest tylko w jeden analizator mas, proces ten przebiega więc w zupełnie inny sposób. Pierwszym etapem jest wyłapanie wszystkie powstających w źródle jonów. Następnie pułapka jest selektywnie opróżniania i pozostają w niej jony o zdefiniowanej wartości m/z które można poddać procesowi fragmentacji. Proces ten zajmuje znacznie więcej czasu niż w potrójnym kwadrupolu. Dodatkowo czym bardziej skomplikowana matryca i czym mniejsze stężenie analitu, tym mniejsza jest intensywność sygnału badanej substancji w widmie i tym pomiary z pułapki jonowej są mniej powtarzalne.
QTRAP
Jest to potrójny kwadrupol, w którym drugi z analizatorów masy może pracować jak kwadrupol lub jak pułapka jonowa. Posiada więc wszystkie zalety potrójnego kwadrupola. Dostępne są też charakterystyczne dla pułapki tryby skanowania z wysoką czułością. W spektrometrach typu QTRAP przed pułapką jonową znajduje się kwadrupolowy analizator masy i komora zderzeń. Sprawia to, że w pełni można wykorzystać wysoką czułość pułapki przy wykonywaniu widm MS/MS. Niezależnie od tego jak bardzo złożona jest matryca, jony do fragmentacji wybierane są w sposób ciągły i z maksymalną wydajnością, a w komorze zderzeń następuje wysokowydajna fragmentacja. Do pułapki jonowej trafiają więc tylko fragmenty jonów o wybranej wartości m/z. Następnie za pomocą pułapki można zebrać widmo fragmentacyjne lub wykonać kolejną fragmentację. Oba te procesy można wykonywać w bardzo powtarzalny sposób. Unikalnym zastosowaniem spektrometrów typu QTRAP jest możliwość wykorzystania trybu MS3 do analizy ilościowej. Jest to tryb, który polega na dwukrotnej fragmentacji, gdzie w pierwszym etapie wybierane są jony macierzyste, a następnie do fragmentacji wybierany jest jeden z powstałych fragmentów. Tryb ten nazwany MRM3 jest jeszcze bardziej selektywny niż obserwowanie przejść MRM.
Spektrometry wysokiej rozdzielczości
Spektrometry typu Orbitrap są połączeniem pułapki jonowej z analizatorem z transformacją Fouriera. Przeznaczone są głównie do analizy jakościowej i identyfikacji związków i praktycznie nie znajdują zastosowania w analizie ilościowej. Q-Exactive oraz spektrometry typu QqTOF wyposażone są w kwadrupolowy analizator mas, komorę zderzeń oraz analizator umożliwiający uzyskanie widma wysokiej rozdzielczości. Spektrometry te czasami stosuje się w analizie jakościowej. Na spektrometrach typu Q-Exactive prowadzone są próby wykonywania analizy ilościowej. W przypadku badania pojedynczych związków stosuje się obserwowanie wybranych reakcji fragmentacji (SRM - Selected Reaction Monitoring), trybu bardzo zbliżonego do obserwowania przejść MRM na potrójnym kwadrupolu z tą różnicą, że drugi analizator działa z wysoką rozdzielczości. Dzieje się to jednakże kosztem szybkości zbierania danych i wydajności transmisji danych. W przypadku analizy wielu związków na tego typu spektrometrze wykorzystuje się tylko tryb MS. Analizator kwadrupolowy wybiera jony macierzyste analitów, które bez poddawania procesowi fragmentacji trafiają do analizatora wysokiej rozdzielczości. Umożliwia to analizę wielu związków. Tryb MS, nawet z dokładnym pomiarem masy, w wielu wypadkach nie zapewnia jednak wystarczającej selektywności. Na większości spektrometrów typu QqTOF analizę ilościową prowadzi się również tylko w trybie MS. Wyjątkiem są tu spektrometry typu TripleTOF. Wykorzystywany jest w nich tryb MRMHR (High Resolution MRM). Tak jak w przypadku trybu SRM na spektrometrach Q-Exactive również tu obserwujemy wybrane reakcje fragmentacji wykorzystując widma wysokiej rozdzielczości. Różnica polega na tym, że ze względu na wysoką szybkość pracy analizatora TOF możliwe jest obserwowanie nawet 100 analitów w ciągu jednej sekundy. Spektrometry wysokiej rozdzielczości są relatywnie drogie zarówno przy zakupie jak i w eksploatacji. Nie zapewniają również tak wysokiej czułości jak spektrometry typu potrójny kwadrupol. W obecnej chwili nie są powszechnie stosowane w analizie ilościowej w laboratoriach diagnostycznych.
Do rutynowej analizy w laboratoriach diagnostycznych najczęściej wykorzystywane są spektrometry typu potrójny kwadrupol i QTRAP ze względu na tryb pracy MRM. Nie ma czulszego trybu pracy spektrometru mas zapewniającego odpowiednią selektywność i szybkość pomiaru. Jakie cechy są istotne dla tego typu spektrometru oraz na jakie parametry należy zwrócić uwagę wybierając układ LC-MS/MS?
Istotne parametry spektrometru mas w trybie pracy MRM
W obecnej chwili w laboratoriach diagnostycznych rutynowo bada się do kilkudziesięciu różnorodnych analitów w pojedynczym przebiegu analitycznym. Spektrometr przede wszystkim musi charakteryzować się wystarczającą czułością tak, aby możliwe było oznaczanie badanego parametru w całym zakresie występujących stężeń. Im czulszy spektrometr, tym łatwiejsze jest przygotowanie próbki. W wielu przypadkach posiadając odpowiednio czuły spektrometr przygotowanie próbki można ograniczyć do odbiałczania, a w celu zmniejszenia efektu matrycy przed nastrzyknięciem próbkę rozcieńcza się. W większości przypadków producenci specyfikują czułość spektrometru, podając jaką wartość stosunku sygnału do szumu można uzyskać dla nastrzyku określonej ilości rezerpiny. Test ten jest wykonywany dla czystego roztworu standardu. Należy pamiętać, że w zależności od konstrukcji źródła jonów czułość, a co za tym idzie, limity oznaczalności rzeczywistych próbek w skomplikowanych matrycach, takich jak np. surowica, mogą się bardzo różnić od podanych w specyfikacji.
Kolejną istotną cechą spektrometrów typu potrójny kwadrupol jest szybkość ich działania w trybie MRM. Im szybszy spektrometr, tym więcej analitów z większą powtarzalnością można oznaczyć. Szybkość działania spektrometru zależy od czasu przebywania jonów w optyce jonowej. Czas ten opisany jest za pomocą dwóch parametrów. Pierwszy parametr to czas obserwacji (dwell time). Jest to czas poświęcony na obserwowanie przejścia MRM, drugi - to czas przerwy (pause time). Jest to czas pomiędzy kolejnymi przejściami MRM. Tworząc metodę ilościową na systemie LC-MS/MS dobieramy przynajmniej jedno przejście MRM dla każdego analitu. Całkowity czas cyklu pomiarowego to suma czasów obserwacji i czasów przerwy.
Jeśli czas całkowity cyklu jest za długi istnieje niebezpieczeństwo zebrania niewystarczającej ilości punktów pomiarowych i złego odwzorowania piku, a co za tym idzie niskiej powtarzalności metody (rysunek 4).
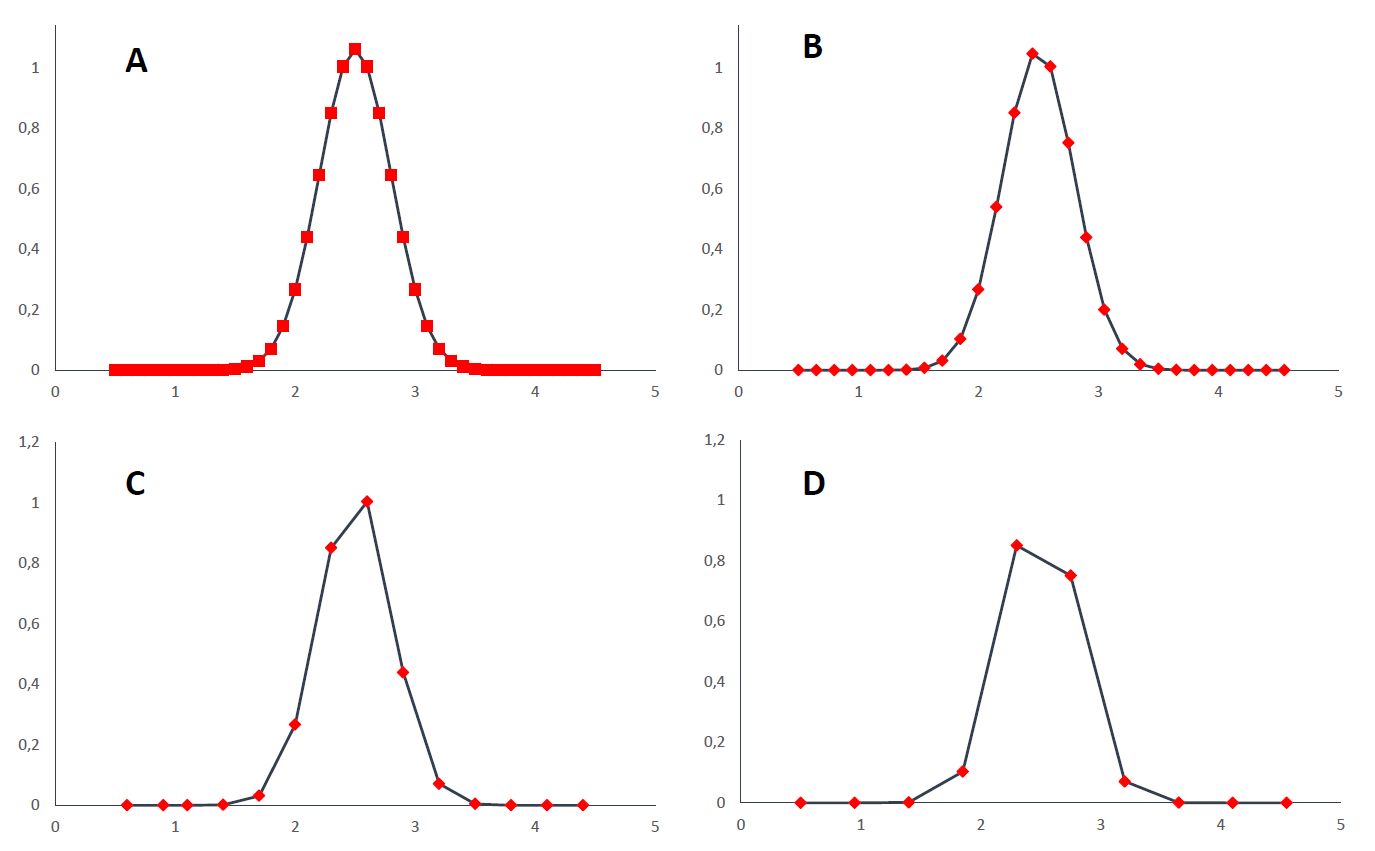
Rys. 4. Odwzorowanie piku w zależności od częstotliwości zbierania danych, ilość punktów na obwiedni piku: A) > 20; B) 14; C) 8; D) 5.
Wydaje się więc, że najlepszym sposobem na skrócenie całkowitego czasu cyklu jest skracanie czasów obserwacji i przerwy. We współczesnych potrójnych kwadrupolach czas obserwacji może być krótszy niż 1 ms, a czas przerwy to 1 ms. Im bardziej skraca się czas obserwacji tym większy udział w czasie cyklu ma czas przerwy, co zmniejsza wydajność transmisji jonów. Dodatkowo im dłużej obserwujemy dane przejście MRM, tym bardziej uśrednia się w czasie sygnał i tym lepszej jakości sygnał uzyskujemy (rysunek 5).
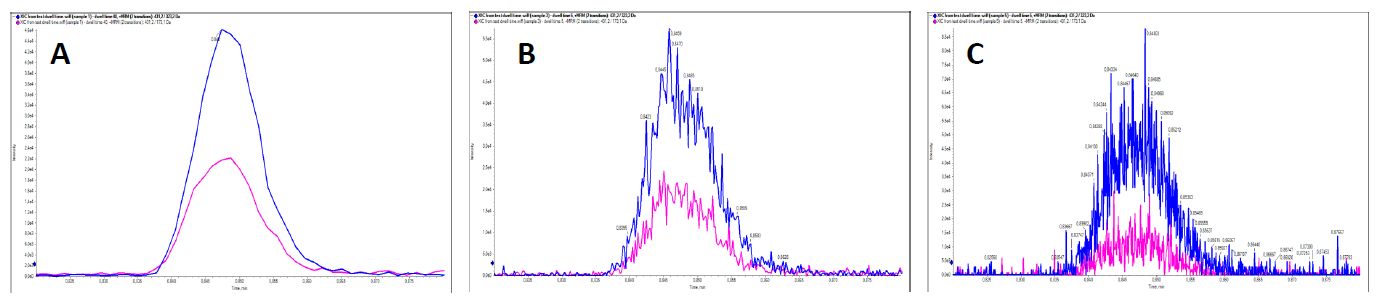
Rys. 5. Zależność stabilności sygnału od czasu dwell time: A) 40 ms, B) 5 ms, c) 1 ms.
W praktyce nie stosuje się czasów obserwacji poniżej 5 ms. Aby umożliwić analizę bardzo wielu związków część producentów wprowadziła oprogramowanie, które umożliwia obserwowanie przejścia MRM dla analitu w oknie czasowym spodziewanego czasu retencji, a nie w czasie całej analizy. Rozwiązanie to znacznie uprościło tworzenie metod ilościowych i umożliwiło tworzenie szybszych metod w przypadku badania więcej niż 10 analitów.
W zależności od struktury i grup funkcyjnych badane anality jonizują się lepiej w polaryzacji dodatniej lub ujemnej. Aby uzyskać jak najlepsze parametry analizy można dla jednej próbki wykonać dwie analizy w różnych polaryzacjach lub wykonać jedną analizę, przełączając polaryzację w trakcie jej trwania. Dostępne na rynku spektrometry mają czas przełączania od kilku do kilkuset milisekund. Nawet w przypadku najszybszych spektrometrów czas przełączania polaryzacji wynoszący kilka milisekund jest porównywalny do najkrótszych stosowanych czasów obserwacji przejść MRM. Stosowanie zmiany polaryzacji w każdym cyklu obniża wydajność transmisji jonów i czułość spektrometru. W przypadku zmiany polaryzacji w trakcie jednej analizy znowu niezwykle istotne jest więc oprogramowanie. Musi ono pozwolić na dostosowanie przełączania polaryzacji do rodzaju analitu i jego czasu retencji. Umożliwia to zminimalizowanie częstotliwości przełączania polaryzacji i zmaksymalizowanie wydajności pracy analizatorów mas. Należy również pamiętać, że w wielu przypadkach, aby uzyskać optymalne warunki analizy, dobiera się tak modyfikatory fazy ruchomej, aby wspomagać jonizację w danej polaryzacji. W przypadku analizy w polaryzacji dodatniej do fazy dodaje się kwas mrówkowy lub octowy. Natomiast, aby wspomóc polaryzację ujemną można dodawać do fazy ruchomej amoniak lub aminę organiczną. Tworząc więc metodę, w trakcie której zmieniana jest polaryzacja, analizę prowadzi się w nieoptymalnych warunkach.
Parametrem często podawanym w specyfikacjach potrójnych kwadrupoli jest prędkość skanowania. W trybie MRM oba analizatory mas pracują w trybie obserwowania wybranych jonów dlatego też parametr ten nie ma znaczenia znaczenia w analizie ilościowej. Dodatkowo, ponieważ skanowanie jest bardzo mało wydajne na analizatorze kwadrupolowym, co za tym idzie jest rzadko wykorzystywane wartość tego parametru nie przekłada się na możliwości zastosowania potrójnych kwadrupoli.
Bardzo istotną dla rutynowych analiz w laboratorium diagnostycznym cechą systemu LC-MS/MS jest stabilność pracy spektrometru i związana z tym powtarzalność wyników. W specyfikacjach spektrometrów nie ma parametru bezpośrednio ją opisującego. Zależy ona od wielu czynników. Najważniejsze to odporność spektrometru mas na zanieczyszczenia, co determinuje częstotliwość czyszczenia optyki jonowej oraz budowa źródła jo-nów i jego odporność na efekt matrycy. Oczywiście spektrometr sprzężony jest z chromatografem cieczowym, więc optymalizacja warunków chromatograficznych i właściwe przygotowanie próbki wpływają na bezproblemowości pracy całego systemu. Należy również pamiętać, że im czulszy jest spektrometr, tym więcej jonów dostaje się do jego wnętrza i tym ważniejsze jest stosowanie ultra czystych rozpuszczalników i dbanie o otocznie spektrometru. Dlatego pomimo, że czulszy spektrometr daje większe możliwości analityczne i często umożliwia uproszczenie przygotowania próbki do analizy nie zawsze jest najlepszym rozwiązaniem dla laboratorium wykonującego rutynowe analizy diagnostyczne.
Najpopularniejsze zastosowania LC-MS/MS w diagnostyce laboratoryjnej
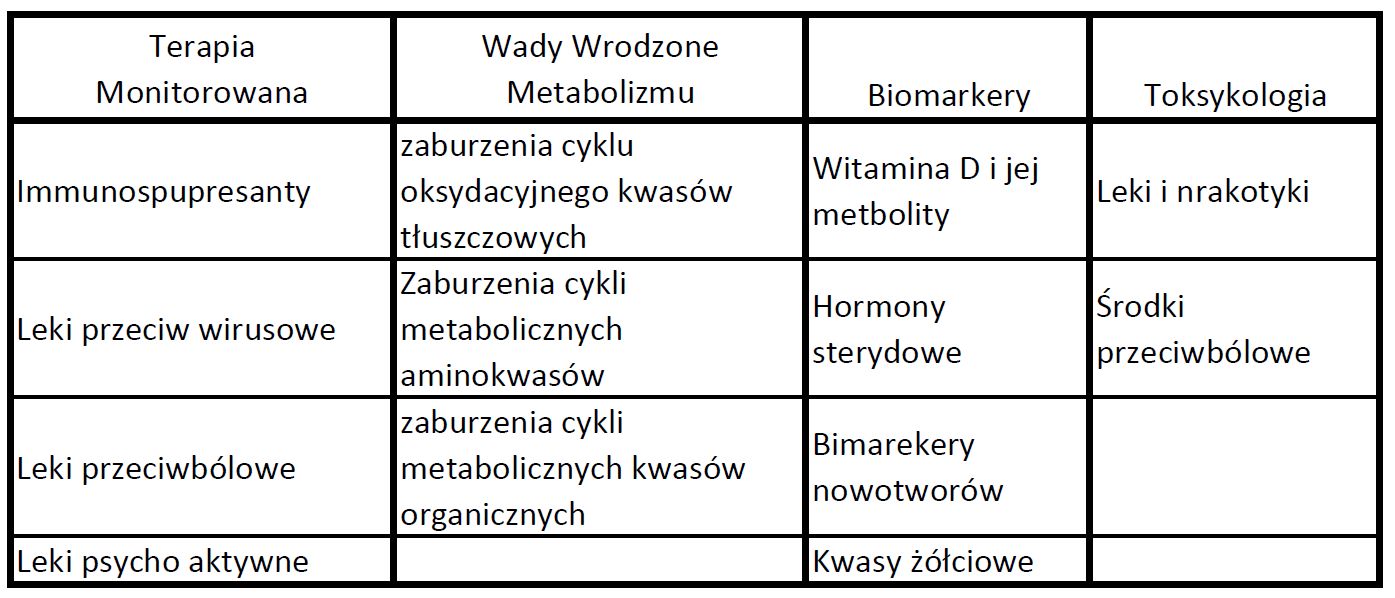
Technika LC-MS/MS jest wykorzystywana w wielu laboratoriach diagnostycznych do oznaczania różnorodnych parametrów. Jej największą zaletą jest możliwość oznaczania wielu parametrów w czasie jednej analizy, niski koszt pojedynczej analizy i możliwość dodawania nowych analitów. Wadą natomiast jest wysoki koszt aparatury oraz potrzeba eksperckiej wiedzy do efektywnego wykorzystywania możliwości techniki LC-MS/MS. Dlatego też spektrometrię mas sprzężoną z chromatografią cieczową rutynowo wykorzystuje się tylko w niektórych, opisanych w dalszej części, metodach. Są one na tyle popularne, że dostępne są komercyjnie zestawy odczynników ułatwiających prowadzenie pomiarów.
Tabela 1. Zastsowanie LC-MS/MS w diagnostyce medycznej.
Badania przesiewowe noworodków
Jedną z najpopularniejszych aplikacji wykorzystujących LC-MS/MS w diagnostyce laboratoryjnej są badania przesiewowe noworodków w kierunku wrodzonych wad metabolizmu. Zastosowanie w tym przypadku wstrzykowej analizy przepływowej (FIA – Flow Injection Analysis ) umożliwia jednoczesne oznaczenie profilu aminokwasów i acylokarnityn bez konieczności ich wcześniejszego rozdzielania na kolumnie analitycznej. Pozwala to na stosowanie bardzo krótkiego czasu analizy (w zależność od konfiguracji systemu nawet poniżej 1 minuty) pomimo, że monitoruje się stężenie kilkudziesięciu parametrów. Ponieważ wszystkie anality i matryca trafiają równocześnie do źródła jonów, występuje efekt matrycy w różnym stopniu zaburzający jonizację w źródle jonów. Aby możliwe było wykonywanie pomiaru z wystarczającą powtarzalnością dla większości analitów stosuje się wzorce znakowane izotopowo. Wykorzystanie metody MS/MS w badaniach przesiewowych wynika również z tego, że do wykonania badania potrzebna jest bardzo mała ilość próbki. Wykorzystuje się suchą kroplę krwi ( DBS – Dry Blood Spot ). W trzeciej lub czwartej dobie życia noworodka pobiera się z pięty około 30 – 50 l krwi ( kilka kropli) na specjalną bibułę, która po wysuszeniu wysyłana jest do laboratorium, gdzie wykonywane są specjalistyczne badania. Badania powinny być wykonane w ciągu tygodnia od urodzenia dziecka.
Metoda MS/MS zyskała popularność dzięki możliwości oznaczania parametrów w kierunku wielu wad wrodzonych równocześnie. Najczęstszą wykrywaną tą metodą chorobą jest fenyloketonuria, w przypadku której oznacza się stężenie fenyloalaniny i tyrozyny. W Polsce częstość jej występownia to około 1 na 8000 urodzonych dzieci. Analiza dodatkowych analitów w próbce tylko nieznacznie zwiększa koszt pomiaru, dlatego możliwe jest wykonywania badania przesiewowego w kierunku nawet bardzo rzadko występujących wad. W obecnej chwili wszystkie dzieci w Polsce objęte są tym badaniem. Jest to badanie przesiewowe, więc o jego wyniku informowani są rodzice tylko w wypadku uzyskania nieprawidłowego wyniku.
Terapia monitorowana
W większości przypadków dawkę leku dla pacjenta dobiera się na podstawie jego wagi, płci i wieku. Metabolizm substancji czynnych u różnych osób może bardzo się różnić. Efektem tego jest różne stężenie substancji czynnej i jej aktywnych metabolitów we krwi, a co za tym idzie dalekie od optymalnego działanie podanego leku. Jest to szczególnie istotne np. w przypadku immunosupresantów podawanych po przeszczepie. Za mała dawka może spowodować, że przeszczep zostanie odrzucony, a za duża może zniszczyć układ odpornościowy pacjenta i w rezultacie doprowadzić do jego śmierci. W obecnej chwili stosuje się 4 substancje czynne: Cyklosporynę A, Ewerolimus, Syrolimus i Takrolimus. Technika LC-MS/MS zapewnia największą selektywność (czyli brak interferencji, będący największym problemem w metodach immunoenzymatycznych), wymaganą czułość i krótki czas analizy, Do oznaczania wszystkich substancji służy jedna metoda LC-MS/MS, w której czas analizy jest poniżej 5 minut.
Coraz częściej stosuje się terapię monitorowaną i oznaczanie stężenia substancji czynnej za pomocą LC-MS/MS również w przypadków leków przeciwwirusowych, antynowotworowych oraz substancji psychoaktywnych.
Witamina D
Witamina D stała się ostatnio bardzo popularna. Okazuje się, że bierze ona udział w bardzo wielu procesach w organizmie i wpływa nie tylko na procesy związane z metabolizmem układu kostnego i gospodarką wapnia, ale również na układ odpornościowy (między innymi wpływa na syntezę peptydów antybakteryjnych), a jej niedobór może wpływać na obniżenie nastroju. Z powodu wielu istotnych funkcji jakie witamina D pełni w organizmie proponuje się nazywać ją hormonem. Ponieważ nadmiar witaminy D może mieć również niekorzystny wpływ na organizm istotne jest oznaczanie jej poziomu w organizmie.
Witamina D3 (cholekalcyferol) powstaje w skórze pod wpływem promieniowania słonecznego, natomiast Witamina D2 (ergokalcyferol), którą zazwyczaj się suplementuje, jest pochodzenia roślinnego. Aktywną formą Witaminy D są jej metabolity 25-Hydroksy, czyli odpowiednio 25-OH-cholekalcyferol i 25-OH-ergokalcyferol. W obecnej chwili większość oznaczeń poziomu witaminy wykonuje się za pomocą zautomatyzowanych metod immunoenzymatycznych. W zależności od producenta oznaczają one poziom całkowity 25-hydroksy metabolitów lub tylko formy D3. Za złoty standard uważa się metodę LC-MS/MS. Zapewnia ona największą precyzję pomiarów oraz umożliwia oznaczenie poziomu obu form niezależnie. Stężenie metabolitów jest na poziomie ng/ml i oznaczenie to może być wykonywane na większości dostępnych potrójnych kwadrupoli. Dodatkowo badania z ostatnich lat wskazują na obecność w organizmie jeszcze jednego metabolitu 3-epi-25-OH-witaminy D3. Jest to forma nieaktywna. Oznaczenie jej poziomu jest szczególnie istotne u dzieci poniżej 1 roku życia, choć i u dorosłych ta forma może stanowić nawet 17% całkowitego poziomu Witaminy D. W obecnej chwili dostępne są tylko metody LC-MS/MS pozwalające na rutynowe oznaczanie tego epimeru.
Innym istotnym metabolitem jest 1,25–dihydroksy-Witamina D3. Jest to aktywny metabolit powstający w nerkach, którego prawidłowy poziom jest uzależniony od pracy tego narządu. Jego stężenie jest około 1000 razy niższe od stężenia wspomnianych wcześniej metabolitów i jest na poziomie kilkudziesięciu pg/ml. Oznaczenie tego parametru możliwe jest jednak głównie przy wykorzystaniu najczulszych dostępnych obecnie systemów LC-MS/MS.
Toksykologia
W toksykologii celem jest stwierdzenie jaką substancją zatruł się pacjent. Nie jest tu istotna dokładana analiza ilościowa, lecz znalezienie jakie substancje toksyczne są obecne w organizmie. Pomiary można wykonywać na różnego rodzaju spektrometrach. Wykorzystując potrójny kwadrupol pracujący w trybie MRM można badać próbki pod kątem kilkuset (około 300) różnorodnych spodziewanych substancji (MTS - Multi Target Screening). Takie pomiary charakteryzują się bardzo dużą czułością, ale możliwe jest stwierdzenie obecności tylko monitorowanych substancji. Jeśli badana osoba zatruła się substancją dla której nie ma zdefiniowanego przejścia MRM, w tym trybie pracy nie zostanie ona znaleziona. Dlatego identyfikacja za pomocą samego przejścia MRM, lub nawet kilku przejść, może prowadzić do fałszywie pozytywnych wyników.
Z kolei za pomocą spektrometrów charakteryzujących się wysoką czułością w trybie skanowania (pułapka jonowa, QTRAP) można sprawdzać obecność niespodziewanych substancji (GUS - General Unknown Screening). Aby możliwa była identyfikacja substancji niezbędne jest wykonanie widma fragmentacyjnego i potwierdzenie tożsamości substancji za pomocą porównania z widmem z biblioteki. Ograniczeniem stosowania tej metody jest konieczność posiadania odpowiednio rozbudowanej biblioteki widm oraz jej niższa czułość, znacznie gorsza niż w przypadku trybu MRM potrójnego kwadrupola. Jest to szczególnie istotne dla substancji jonizujących się z niską wydajnością. Jeśli znaleziona substancja nie znajduje się w bibliotece jej identyfikacja za pomocą spektrometru mas wymaga eksperckiej wiedzy i nie zawsze jest możliwa. Na spektrometrach typu QTRAP możliwe jest połączenie MTS i GUS. W trybie MRM obserwuje się za pomocą przejść MRM listę substancji, dla których wymagana jest duża czułość, a następnie w tym samym cyklu wykonywany jest pełen skan w celu sprawdzenia jakie jeszcze substancje mogą występować w badanej próbce. Dodatkowo w przypadku znalezienia substancji za pomocą przejścia MRM możliwe jest wykonanie z wysoką czułością widma fragmentacyjnego, które pozwala z dużą pewnością potwierdzić tożsamość badanej substancji.
Równie dużą pewność otrzymanych wyników można uzyskać wykonując pomiary na tandemowych spektrometrach wysokiej rozdzielczości. Jako wstępny skan stosuje się widmo wysokiej rozdzielczości, a następnie potwierdza się tożsamość związku za pomocą widma fragmentacyjnego. Czułość takich pomiarów jest niższa niż w trybie MRM, natomiast dodatkowo uzyskiwana jest dokładna masa związków, co może ułatwić identyfikację substancji nie znajdujących się w posiadanej bibliotece.
Przyszłość spektrometrii mas w diagnostyce laboratoryjnej
Świętym Graalem techniki LC-MS/MS w diagnostyce jest w pełni zautomatyzowany analizator, do którego wkładać się będzie próbki, odczynniki i ewentualne elementy zużywalne, i który po naciśnięciu komendy „start” w krótkim czasie dostarczać będzie informacji o wybranych parametrach w wielu próbkach. Do takiego rozwiązania jeszcze daleka droga i na razie do prawidłowej pracy systemu potrzebny jest operator z dużym doświadczeniem. W obecnej chwili trwają prace, które mają uprościć i przyspieszyć wykonywanie analizy, przy zapewnieniu właściwej czułości i specyficzności. Najprostszą metodą przyspieszenia analizy jest usunięcie kolumny chromatograficznej z układu tak jak w przypadku analizy wstrzykowej. Niestety takie rozwiązanie zwiększa efekt matrycy w źródle jonów i uniemożliwia oznaczenie związków izobarycznych. Aby zmniejszyć ten efekt należy stosować bardziej wydajne metody przygotowania próbek. Natomiast, aby oznaczać związki izobaryczne bez zastosowania chromatografii i zachować specyficzność metody można stosować spektrometrię ruchliwości jonów (IMS – Ion Mobility Spectrometry). W technice tej jony nie są rozdzielane na podstawie ich stosunku masy do ładunku, ale na podstawie ich przekroju czynnego, czyli kształtu cząsteczki. Coraz więcej firm wprowadza takie rozwiązania w komercyjnie dostępnych spektrometrach mas.
Skrócenie czasu analizy można uzyskać stosując nowe metody jonizacji próbek takie jak np. laserowa desorpcja termiczna (LDTD – Laser Diode Thermal Desorption) połączona z jonizacją APCI. Przygotowaną próbkę o objętości kilku mikrolitrów nanosi się na specjalną płytkę wielodołkową, w której jest metalowe dno. Promień lasera uderzając od spodu w dno dołka powoduje termiczną desorpcję cząsteczek analitu, które następnie są jonizowane w wyładowaniu koronowym. Przy zastosowaniu tej metody czas analizy pojedynczej próbki to mniej niż 10s.
Innym sposobem skrócenia czasu analizy próbek jest połączenie przygotowania próbki z pomiarem. Jednym z rozwiązań jest tu zastosowanie metody jonizacji Paper Spray. Mechanizm jonizacji jest podobny jak w technice elektrosprej. Odmierzoną objętość krwi nanosi się na bibułę chromatograficzną o specjalnym kształcie. Po wysuszeniu bibułę nawilża się rozpuszczalnikiem organicznym, umieszcza przed wlotem do spektrometru mas i przykłada się do niej wysokie napięcie. Z czubka bibuły pod wpływem wysokiego napięcia emitowany jest sprej, który umożliwia zjonizowanie cząsteczek analitu. Odpowiedź systemu jest proporcjonalna do stężenia analitu. W obecnej chwili prowadzi się badania nad możliwością zastosowania tej metody w analizie rutynowej. Jej zalety to szybkość oraz łatwość pobierania próbek i ich transportu. Wyzwaniem w dalszym ciągu jest uzyskanie odpowiedniej powtarzalności pomiarów.
Oprócz zmian w samej technice pomiarów obserwuje się również coraz większą ilość nowych parametrów oznaczanych za pomocą techniki LC-MS/MS. Największy rozwój obserwuje się w analizie ilościowej biomarkerów białkowych i w metabolomice.
W przypadku oznaczania białka za pomocą spektrometru mas pomiar wykonuje się po przeprowadzeniu hydrolizy enzymatycznej (zazwyczaj za pomocą trypsyny). Wybrany peptyd o charakterystycznej dla białka sekwencji oznacza się w trybie MRM lub MRM3. Praca na poziomie peptydów zdecydowanie zwiększa czułość pomiaru oraz jego powtarzalność. Dodatkowo ułatwia opracowanie metody chromatograficznej.
W podejściu metabolomicznym w czasie jednego pomiaru oznacza się wiele parametrów równocześnie. Są to anality charakterystyczne dla wybranego cyklu metabolicznego. W tego rodzaju oznaczeniach najważniejsza nie jest bezwzględna wartość stężeń ale profil badanych związków, ich wzajemna relacja stężeń. Do opracowania wyników potrzebne są narzędzia chemometryczne, pozwalające na postawienie prawidłowej diagnozy.






