Polpharma SA, Badania i Rozwój
strony wersji drukowanej: 8-14
W niniejszej publikacji zostaną zaprezentowane najnowsze trendy w rozwoju chromatografii cieczowej. Porównana zostanie klasyczna HPLC z jej najnowszym wariantem - ultra wysokosprawną chromatografią cieczową (UHPLC). Poniższe opracowanie poświęcone jest przede wszystkim sposobom postępowania podczas transferu metod HPLC do nowego wymiaru jakim jest UHPLC.
 Historia UHPLC
Historia UHPLC
Przez ponad 30 lat technika HPLC zyskała ogromną popularność w większości laboratoriów analitycznych. Twierdzi się, że chromatograf cieczowy jest trzecim co do popularności sprzętem w laboratorium – zaraz po wadze i pH-metrze. Oczywiście, jak każda technika i ona ulega ciągłemu doskonaleniu. Z roku na rok pojawiają się nowsze modele, tak samych aparatów, jak i kolumn chromatograficznych.
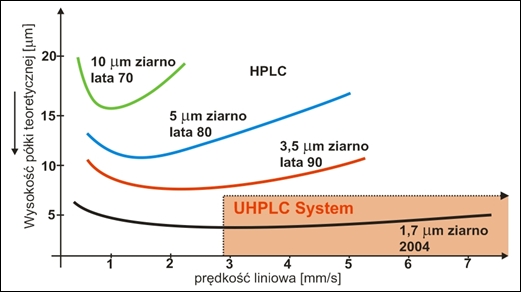
We wczesnych latach 70-tych komercyjnie dostępne były kolumny wypełnione nieporowatym, o nieregularnych kształtach żelem krzemianowym o wymiarach około 40 µm. Ich sprawność była delikatnie mówiąc niska – przy 1 metrze złoża liczba półek teoretycznych wynosiła około 1000. W późnych latach 70-tych na rynku pojawiały się kolumny z ziarnem o średnicy 10 µm, a w latach 80-tych znane już były popularne obecnie kolumny z żelem krzemionkowym ze sferycznym, porowatym ziarnem, o średnicy 5 µm. Charakteryzuje się ono przyzwoitą sprawnością wynoszącą około 12.000 półek teoretycznych przy długości kolumny 150 mm.
Szczęśliwie, na rynku panuje ostra konkurencja, która owocuje coraz lepszym sprzętem - dotyczy to oczywiście również samych kolumn. Po upowszechnieniu w latach 90-tych ziaren o średnicy 3 µm, uważano, że dalsze zmniejszanie ziarna nie ma uzasadnienia, ze względu na koszty związane z ich produkcją oraz problemy związane z ich stosowaniem.
Przełom nastąpił w roku 2004 kiedy na rynku pojawił się zupełnie nowy model chromatografu cieczowego – ACQUITY UPLC oraz kolumny z ziarnem o średnicy 1,7 µm, wyprodukowane przez firmę Waters. Co ciekawe, minęło kilka lat, zanim konkurencja była w stanie dostarczyć sprzęt o zbliżonych osiągach.
Obecnie praktycznie każdy liczący się gracz na rynku chromatograficznym posiada w ofercie sprzęt zdolny do pokonania ciśnienia stawianego przez kolumny z ziarnem o średnicy poniżej 2,1 µm. Są to poza firmą Waters m.in.: Agilent, Shimadzu, Thermo, Dionex, PerkinElmer, Hitachi, Jasco. Warto wspomnieć, że skrót UPLC jest zastrzeżonym znakiem towarowym firmy Waters, dlatego pozostałe firmy stosują różne synonimy m.in. RRLC (Rapid Resolution LC), RSLC (Rapid Separation LC), czy FPLC (Fast Performance LC) lub UFLC (Ultrafast LC). W czasie tegorocznych targów Pittcon firma Waters zaprezentowała nowy model chromatografu przystosowanego do pracy w warunkach wysokich ciśnień – ACQUITY UPLC H-Class, zdolny do pracy zarówno ze standardowymi kolumnami jak i z kolumnami sub-2,1 µm.
Prognozuje się, że w roku 2013 systemy UHPLC będą stanowiły 50% rynku, co wydaje się bardzo prawdopodobne, gdyż cena nowych systemów jest niewiele wyższa, niż systemów standardowych.
Podobny rozwój nastąpił na rynku kolumn chromatograficznych. Gdy Henry Ford prezentował pierwsze modele Forda T, mówił, „możesz otrzymać samochód w każdym kolorze, pod warunkiem, że będzie to kolor czarny”, podobnie w roku 2004 można było zastosować, każde wypełnienie, pod warunkiem, że było to C18. Dzisiaj sytuacja wygląda o wiele lepiej, nie tylko dostępne są niemal wszystkie popularne modyfikacje krzemionki (w tym poza C18, również C8, Phenyl, HILIC, Silica, Amide, Fluoro-Phenyl, Phenyl-Hexyl), ale wybierać można także pomiędzy różnymi technologiami, co ułatwia dobór kolumny o odpowiedniej selektywności.
Pierwszą dostępną technologią była znana jeszcze przed 2004 rokiem technologia BEH (Ethylene Bridged Hybrid, kolumny z wypełnieniem krzemionkowym wzmocnionym mostkami etylenowymi), dzięki której kolumny są zdolne znieść ciśnienie rzędu 15000 Psi (około 1000 bar). Inna technologia to złoża czysto krzemionkowe o wysokiej odporności na kruszenie (High Strength Silica, HSS). Ich wadą, w stosunku do złóż BEH, jest mniejsza odporność na wysokie pH, ale za to wykazują znacznie wyższą retencyjność, przydatną w oznaczaniu polarnych analitów. CSH (Charged Surface Hybrid) to najnowszy typ wypełnienia, który jest modyfikacją kolumn BEH. W tym przypadku powierzchnia dodatkowo została obdarzona ładunkiem, dzięki czemu kolumny wypełnione tymi złożami (C18, Fluoro-Phenyl, Phenyl-Hexyl) oferują szeroki zakres selektywności oraz poprawioną symetrię pików związków zasadowych badanych w kwaśnych fazach o niskiej sile jonowej (np. 0,1% kwas mrówkowy).
Powyższe złoża zostały opracowane przez firmę Waters, ale na rynku pojawiają się również kolumny firm konkurencyjnych, m.in. Agilent (Rapid Resolution HD 1,8 µm), Grace (VisionHT 1,5 µm), Phenomenex (Kinetex 1,7 µm), GLSciences (Inertsil ODS-4 2 µm), Thermo (Hypersil GOLD, 1,9 µm).
Teoretyczne podstawy UHPLC
Od dawna wiadomym było, że zgodnie z równaniem van Deemter’a, im mniejsza średnica ziarna wypełnienia kolumny, tym niższa będzie wysokość półki teoretycznej (HEPT), czyli tym wyższa będzie sprawność kolumny (N).
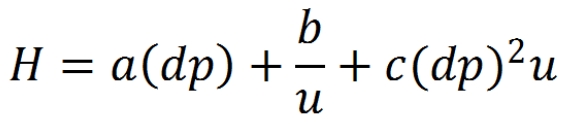
gdzie:
- a(dp) - parametr A związany jest z wypełnieniem kolumny (wielkością ziarna), z dystrybucją wielkości ziaren oraz z jakości ich upakowania. Wartość A nie zależy od szybkości przepływu. Im mniejsze ziarno, mniejsza dystrybucja wielkości oraz lepsze upakowanie tym mniejsza jest wartość A i większa sprawność kolumny.
- b/u - parametr B związany jest z dyfuzja pasma podczas przesuwania się w kolumnie. Wolniejszy przepływ to dłuższe przebywanie na kolumnie i większe poszerzenie pasma.
- c(dp)2u - parametr C związany z transportem masy, na który wpływ mają trzy składowe:
• transport masy przez przepływającą fazę ruchomą – faza ruchoma płynie szybciej środkiem między dwoma ziarnami, a wolniej przy ziarnie, co powoduje rozmycie pasma,
• transport masy przez stojącą fazę ruchomą – faza ruchoma wewnątrz porów nie porusza się, analit migruje do i z wnętrza pora na drodze dyfuzji. Im krótsza droga cząsteczki w ziarnie tym mniejsze rozmycie,
• transport masy przez fazę stacjonarną – kinetyka adsorpcji/desorpcji.
- u - prędkość liniowa – L/t [mm/s]
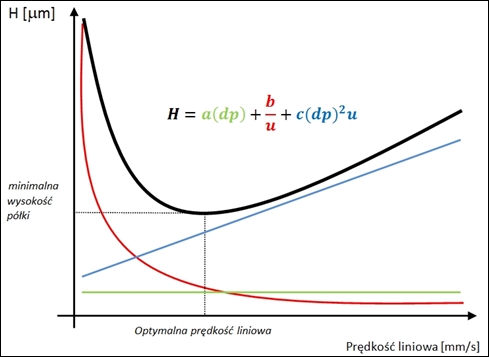
Minimum krzywej van Deemter’a odpowiada idealnej prędkości przepływu, przy której uzyskuje się najwyższą sprawność kolumny. Jest to kompromis między składowymi B i C.
Składowe A i C są zależne od wielkości ziaren. Mniejsze ziarna powodują zmniejszenie wysokości H, co oznacza, że kolumna jest bardziej sprawna, tj. posiada więcej półek teoretycznych na jednostkę długości. Małe ziarna pozwalają analitowi na szybszą migrację do i z ziarna, ponieważ jego droga dyfuzji jest krótsza. To powoduje, że analit eluuje jako wąski pik, ponieważ spędza mniej czasu w fazie stacjonarnej, gdzie następuje poszerzanie pasma.
Z powyższego wynika, że sprawność (N) kolumny jest odwrotnie proporcjonalna do wielkości ziarna (dp):
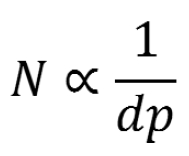
a przy założeniu, że sprawność (N) kolumny jest odwrotnie proporcjonalna do szerokości piku (w):
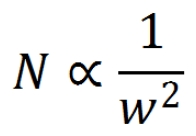
z kolei wysokość piku jest odwrotnie proporcjonalna do szerokości piku (w):
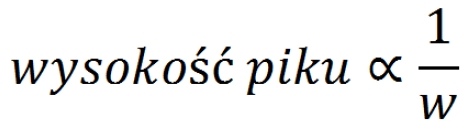
Dlatego teoretycznie, przy założeniu, że wielkość ziarna zmniejszona zostanie z 5 µm do 1,7 µm, a długość kolumny nie ulegnie zmianie to:
• rozdzielczość poprawi się 1,7-krotnie,
• analiza skróci się 3-krotnie,
• czułość podniesie się 1,7-krotnie,
• ciśnienie podniesie się 27-krotnie!
Natomiast, jeśli założy się stały współczynnik długości kolumny (L) do wielkości ziarna (dp) to:
• rozdzielczość nie ulegnie zmianie,
• analiza skróci się 9-krotnie,
• czułość podniesie się 3-krotnie,
• ciśnienie podniesie się 9-krotnie.
Jest to powód dlaczego producenci od lat dążyli do zmniejszenia wielkości ziarna.
Zalety i wady techniki UHPLC
Zasadniczymi zaletami techniki UHPLC są: skrócenie czasu analizy, podniesienie czułości oraz rozdzielczości. Oczywiście, aby uzyskać wartości zbliżone do teoretycznych należy pamiętać, że wpływ na nie mają również efekty pozakolumnowe i decydująca będzie konstrukcja chromatografu. Producenci sprzętu dokonali zasadniczych zmian praktycznie w każdym elemencie systemu chromatograficznego. Zaczynając od konstrukcji pomp, przez dozownik, a kończąc na detektorach, w których obniżono objętość cel pomiarowych oraz zwiększono częstotliwość próbkowania. Wszystkie zmiany podporządkowane były dwóm celom: obniżeniu do maksimum objętości martwej oraz przystosowaniu do pracy pod kilkukrotnie wyższymi ciśnieniami niż w standardowym systemie HPLC.
Jeśli mowa o zaletach, należy zauważyć, że skracając czas analizy zasadniczo zmniejsza się koszty analiz, poprzez efektywniejsze wykorzystanie sprzętu oraz zmniejszenie zużycia odczynników. Dodatkowy wpływ na to ma skrócenie czasu stabilizacji układu, gdyż objętość martwa uległa zmniejszeniu z około 1-2 ml do około 120 µl. Poza tym należy pamiętać, że nowe metody niosą często więcej informacji, a dzięki podniesionej sprawności pojawiają się nowe piki, z których istnienia wcześniej nie zdawano sobie sprawy.
Oczywiście systemy UHPLC nie są pozbawione wad - jedną z zasadniczych jest fakt, że nie są one jeszcze dostępne we wszystkich laboratoriach, więc może zdarzyć się, że opracowana metoda nie będzie mogła zostać odtworzona w innym laboratorium. Dodatkowo, pomimo, że dostępny jest stosunkowo szeroki wybór kolumn UHPLC, aby uniknąć większych problemów z selektywnością podczas transferu metody z HPLC do UHLC wskazane jest zastosowanie tego samego rodzaju wypełnienia, obecnie nie jest to możliwe, gdyż wiele aktualnie produkowanych złóż nigdy nie będzie dostępne w wersji UHPLC.
Inny problem polega na fakcie, że zmiana istniejącej metody z HPLC do UHPLC związana jest z jej ponowną walidacją, co generuje dodatkowe koszty. Z drugiej strony należy pamiętać, że, w niektórych przypadkach, zyski z transferu będą znacznie wyższe niż wspomniane koszty, ponieważ, zakładając, że np. uda się skrócić metodę z 60 minut do 10 minut, a przeciętna walidacja to około 120 nastrzyków, to wszystkie analizy można wykonać w czasie poniżej 24 godzin.
Transfer metod HPLC do UHPLC
Każdy analityk który stanie przed zadaniem przetransferowania metody HPLC do UHPLC powinien pamiętać, że nowa metoda musi zapewniać:
• odpowiedni rozdział wszystkich istotnych zanieczyszczeń,
• homogeniczność/czystość pików,
• pewność identyfikacji pików,
• odpowiednią dokładność i precyzję.
Transferując metodę HPLC do UHPLC nie da się uniknąć pewnych modyfikacji, spowodowanych różnicami w konstrukcji i parametrach nowego systemu, należy więc założyć potrzebę jej optymalizacji.
Pierwszym etapem transferu jest odpowiedni dobór kolumny, czyli jej chemizmu i wymiarów. Niestety jak już wcześniej wspomniano, dla niewielu kolumn istnieją ich odpowiedniki UHPLC, a obecnie dostępne systemy służące do porównywania złóż w ograniczony sposób pokrywają dostępne na rynku kolumny UHPLC. Jeśli chodzi o wymiary to:
• preferowana średnica wynosi 2,1 mm,
• długość 50 mm, gdy istotna jest szybkość analizy,
• długość 100 mm, gdy najważniejsza jest rozdzielczość.
Następnym etapem jest porównanie objętości obu układów. W przypadku transferu metod gradientowych z HPLC do UHPLC najczęściej spotykaną sytuacją jest fakt, że docelowy system posiada mniejszą objętość martwą, więc aby dokładnie odtworzyć warunki, należy wstawić dodatkowy czas opóźnienia gradientu.
Kolejnym krokiem jest zmniejszenie objętości nastrzyku. Kolumny UHPLC posiadają znacznie mniejszą objętość niż klasyczne kolumny, dlatego należy zmniejszyć objętość nastrzyku proporcjonalnie do
zmniejszenia wymiarów kolumny. Do obliczenia można posłużyć się wzorem:
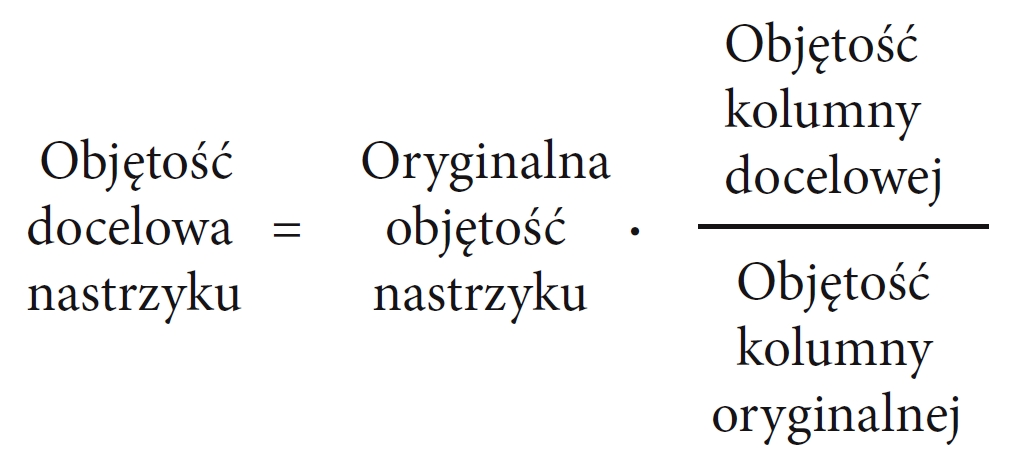
Przyjmuje się, że minimalna objętość (zależnie od konstrukcji nastrzykiwacza) wynosi od 0,5 do 1 µl. Natomiast największa objętość dla kolumny 2,1 x 50 mm to 5 µl.
Następnie należy wyznaczyć ekwiwalent przepływu fazy ruchomej dla zmienionych wymiarów kolumny. W przybliżeniu posłużyć można się wzorem:
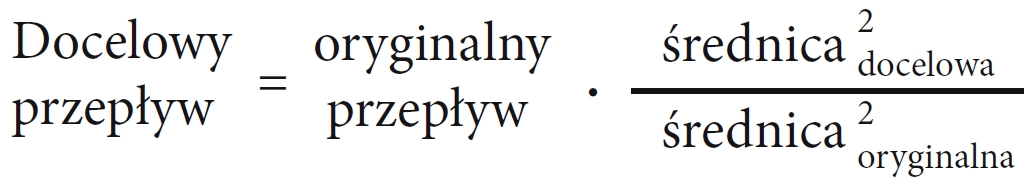
Jak wynika z krzywej van Deemter’a w przypadku małych ziaren zakres optymalnej prędkości liniowej jest o wiele szerszy niż w przypadku ziaren o większej średnicy, dlatego bez uszczerbku dla jakości rozdziału można podnieść przepływ, przy czym należy pamiętać o ograniczeniu jakim będzie wzrost ciśnienia.
O wiele bardziej skomplikowanie sprawa wygląda w przypadku przepływu gradientowego. Pierwszym krokiem jest przeliczenie poszczególnych etapów gradientu jako procentu zmiany do objętości kolumny. W tym celu należy policzyć:

a następnie należy wyznaczyć trwanie każdego segmentu gradientu wyrażone jako objętość kolumny (cυ):
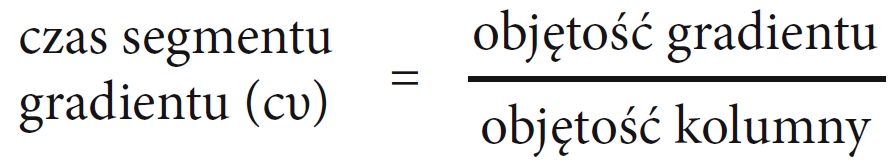
Ostatecznie należy proporcjonalnie obliczyć czas trwania poszczególnych segmentów uwzględniając przepływ i objętość docelowej kolumny.

a następnie:
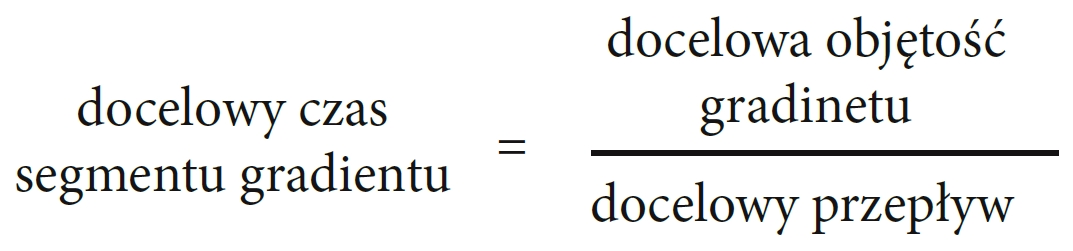
Jak widać jest to dość czasochłonne, dlatego producenci udostępnili odpowiednie kalkulatory umożliwiające przeliczenie wszystkich parametrów w sposób automatyczny. Co więcej, oprogramowanie to pozwala nie tylko na geometryczne skalowanie, ale również na optymalizację pod kątem czasu analizy lub maksymalnej efektywności.
Transferując metodę HPLC do UHPLC nie można zapomnieć o minimalizacji objętości martwych. Należy ograniczyć do minimum długość połączeń komponentów systemu chromatograficznego, nie dopuszczalne jest np. zastępowanie kapilar oryginalnych, kapilarami o większej średnicy wewnętrznej.
Poniżej przedstawiono wynik transferu przykładowej metody HPLC (służącej do testowania kolumn) do warunków UPLC.
Chromatogram 1
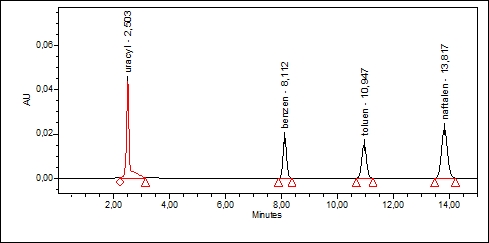
Waters Alliance 2695
kolumna: Atlantis T3
250x4,6 mm 5 µm
faza: H2O:ACN (40:60)
przepływ: 1,0 ml/min
temperatura kolumny: 25°C
detekcja: 254 nm
objętość nastrzyku: 10 µl
Nnaftalen= 19553
Rtoluen-naftalen= 8,1
Chromatogram 2
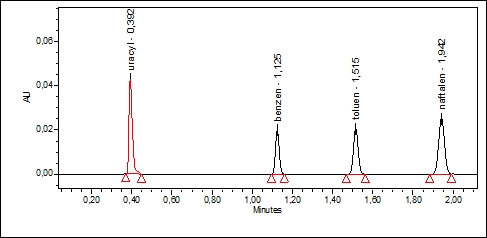
Waters ACQUITY UPLC
kolumna: Acquity HSS T3
100x2,1 mm 1,8 µm
faza: H2O:ACN (40:60)
przepływ: 0,525 ml/min
temperatura kolumny: 25°C
detekcja: 254 nm
objętość nastrzyku: 0,8 µl
Nnaftalen= 19950
Rtoluen-naftalen= 8,7
Chromatorgam 3
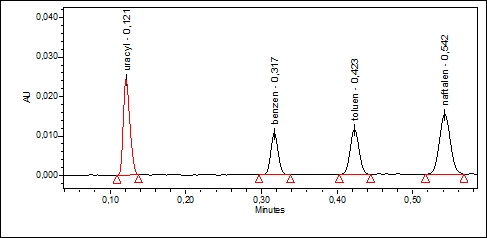
Waters ACQUITY UPLC
kolumna: Acquity HSS T3
50x2,1 mm 1,8 µm
faza: H2O:ACN (40:60)
przepływ: 1,024 ml/min
temperatura kolumny: 25°C
detekcja: 254 nm
objętość nastrzyku: 0,4 µl
Nnaftalen= 7240
Rtoluen-naftalen= 5,2
Chromatogram 4
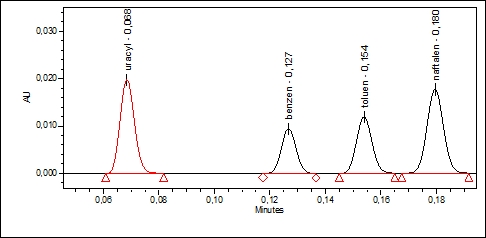
Waters ACQUITY UPLC
kolumna: Acquity HSS T3
50x2,1 mm 1,8 µm
faza: H2O:ACN (40:60)
przepływ: 2,0 ml/min
temperatura kolumny: 90°C
detekcja: 254 nm
objętość nastrzyku: 0,4 µl
Nnaftalen= 4297
Rtoluen-naftalen= 2,4
Jak widać na chromatogramie 1, ostatni pik (naftalen) posiada czas retencji około 14 minut z liczbą półek około 20 000. Korzystając z pomocy kalkulatora dołączonego do oprogramowania systemu UPLC firmy Waters obliczono, że ekwiwalentem sprawności, dla kolumny o wymiarach 100 x 2,1 mm będzie przepływ 0,525 ml/min. Zostało to potwierdzone eksperymentalnie – chromatogram 2. Kalkulator zaproponował również warunki, w którym priorytetem jest czas analizy – chromatogram 3. W tym celu użyto krótszej kolumny (50 mm) oraz zwiększono przepływ (1,024 ml/min). W wyniku tej zmiany skrócono czas czterokrotnie – z dwóch minut do 33 sekund, przy zachowaniu akceptowalnej sprawności układu (ponad 7000 półek). Chromatogram 4 przedstawia graniczne możliwości tego układu – czas retencji poniżej 11 sekund! W tym celu podniesiono temperaturę kolumny do 90°C i przepływ do 2 ml/min. Jak widać na załączonym chromatogramie piki są nadal rozdzielone do podstawy ze sprawnością około 4300 półek.
Podsumowanie i przyszłość UHPLC
Na podstawie analizy bieżących publikacji w dziedzinie chromatografii cieczowej można zauważyć, że systemy UHPLC zaczynają powoli wypierać standardowe systemy HPLC. Dzisiaj powszechnie są obecne w przemyśle, w szczególności farmaceutycznym. Obecnie, większość nowych systemów LC/MS wyposażone jest w system UHPLC ze względu na możliwość pracy z małymi przepływami (szczególnie na kolumnach o średnicy 1,0 mm) i możliwość uniknięcia dzielenia strumienia.
Aktualnie na rynku dostępnych jest kilkaset kolumn C18, charakteryzujących się różną retencyjnością, selektywnością, aktywnością grup silanolowych itd., pozwala to wybrać kolumnę odpowiednią do danego zastosowania. Wypełnień C18 o ziarnie poniżej 2,1 µm istnieje natomiast najwyżej kilkanaście, lecz w praktyce nie stanowi to problemu, gdyż znaczący wzrost ich efektywności sprawia, że przy niewielkim nakładzie pracy możliwy jest na nich rozdział nawet trudnych par pików. Warto zauważyć, że system UHPLC pozwala na znaczne skrócenie czasu nie tylko pojedynczej analizy, ale również czasu potrzebnego na stabilizację układu do kilku minut. Dzięki temu rozwój i walidację metody można przeprowadzić w zaledwie kilkanaście godzin!
Jaka będzie przyszłość chromatografii cieczowej?
Wydaje się, że należy spodziewać się dalszego doskonalenia sprzętu, podnoszenia jego precyzji i niezawodności. Natomiast gorzej wygląda sprawa dalszego obniżania wielkości ziarna. Należy pamiętać, że przy obniżeniu jego wielkości do 1,0 µm, owszem, podniesie się sprawność o 70%, ale równocześnie ciśnienie wzrośnie o niewyobrażalne 790%...
Dostępne w Internecie bezpłatne kalkulatory umożliwiające przeliczenie warunków dla transferu metod HPLC do UHPLC:
- HPLC Calculator v3.0
- Developed by J.-L. VEUTHEY, D. GUILLARME,
- Laboratory of Analytical Pharmaceutical Chemistry, University of Geneva
- http://www.unige.ch/sciences/pharm/fanal/lcap/telechargement-en.htm
- Thermo Scientific HPLC Method Development Calculator
- http://www.hplctransfer.com/
- Dionex method transfer calculator
- http://www.dionex.com/en-us/products/liquid-chromatography/lc-systems/rslc/lp-72455.html





