Rajmund Michalski, Magdalena Jabłońska-Czapla, Sebastian Szopa, Aleksandra Łyko
Instytut Podstaw Inżynierii Środowiska PAN, Zabrze
strony wersji drukowanej: 46-51
strony wersji drukowanej: 46-51

Analiza specjacyjna znajduje zastosowania m. in. w ochronie środowiska, biochemii, geologii, medycynie, farmacji oraz kontroli jakości produktów żywnościowych. Związane jest to z tym, że często nie całkowita zawartość danego pierwiastka lub związku, lecz obecność różnych jego form decyduje o ich właściwościach toksykologicznych. Badania różnych form specjacyjnych wybranych pierwiastków, szczególnie w próbkach o obciążonej matrycy wymaga stosowania różnych metod i technik analitycznych. Najnowsze trendy w tym zakresie dotyczą tzw. technik łączonych, w których metody separacyjne łączone są z różnymi metodami detekcji. W pracy przedstawiono możliwości zastosowań technik łączonych IC-ICP-MS i IC-MS w analizie specjacyjnej wybranych pierwiastków.
Określenie „specjacja” zostało zapożyczone z nauk biologicznych z łacińskiego słowa „species” oznaczającego „gatunek”, „ewolucja gatunku”. Z kolei termin „analiza specjacyjna” pojawił się w literaturze w 1993 roku i był początkowo określany jako „przemieszczanie i przekształcanie się form pierwiastka w środowisku” [1]. Zgodnie z definicją zaproponowaną przez Międzynarodową Unię Chemii Czystej i Stosowanej (ang. International Union of Pure and Applied Chemistry, IUPAC) specjacja to „występowanie pierwiastka w postaci różnych chemicznych indywiduów określonych składem izotopowym, strukturą elektronową lub stopniem utlenienia, strukturą kompleksową lub cząsteczkową” [2].
Specjacja w chemii rozumiana jest jako występowanie danego pierwiastka w różnych postaciach takich jak: jony lub związki chemiczne na różnych stopniach utlenienia oraz w połączeniu z różnymi ligandami. W zależności od celu analizy specjacyjnej i możliwości wydzielania poszczególnych indywiduów chemicznych lub ich grup stosowane są różne terminy związane ze specjacją chemiczną, takie jak specjacja: szczegółowa, grupowa, funkcjonalna, operacyjna, fizyczna i cytologiczna. Inny podział to specjacja: przesiewowa, grupowa, dystrybucyjna i indywidualna [3]. Typ specjacji przesiewowej określa tylko jeden analit najbardziej niebezpieczny w badanej matrycy. Przykładem może być oznaczanie tributylocyny w wodzie morskiej lub oznaczanie metylortęci w tkankach zwierząt. W specjacji grupowej dąży się do określenia poziomu stężenia danej grupy związków lub badanego pierwiastka na różnych stopniach utlenienia np.: jednoczesne oznaczanie Cr(III) i Cr(VI); Fe(II) i Fe(III); Mn(II), Mn(IV) i Mn(VII) lub biochemiczne zapotrzebowanie tlenu (BZT) obok chemicznego zapotrzebowania tlenu (ChZT), czy rtęci elementarnej oraz nieorganicznej i organicznej. Z kolei specjacja dystrybucyjna wiąże się z oznaczaniem różnych form analitów w próbkach biologicznych, np. w płynach fizjologicznych czy w surowicy krwi. Ostatni typ specjacji to specjacja indywidualna, która polega na identyfikacji i oznaczeniu w próbce wszystkich indywiduów chemicznych, które zawierają w swoim składzie dany pierwiastek.
Substancje badane w ramach analizy specjacyjnej można podzielić na wytwarzane przez ludzi i przez nich wprowadzane do środowiska, oraz naturalne związki chemiczne, które powstają w wyniku przemian biochemicznych w organizmach żywych lub w środowisku. Pierwsza grupa znajduje się przede wszystkim w obszarze zainteresowań analizy środowiskowej, a druga jest obiektem badań biochemików i ekotoksykologów. Analiza specjacyjna pomimo znacznych kosztów odgrywa coraz większe znaczenie w rozwiązywaniu zagadnień wymagających nie tylko oznaczenia całkowitej zawartości pierwiastków, lecz również uwzględnienia roli poszczególnych form, w których one występują. Analiza specjacyjna jest wykorzystywana między innymi w: badaniach cyklów biochemicznych wybranych związków chemicznych, oznaczaniu toksyczności i ekotoksyczności pierwiastków, kontroli jakości produktów żywnościowych, oraz farmaceutyków, kontroli procesów technologicznych oraz w analityce klinicznej. Nawet najbardziej wyrafinowana technika czy metoda analityczna oraz najbardziej doświadczony i rzetelny analityk nie jest w stanie uzyskać wiarygodnych wyników analizy, jeżeli próbka zostanie źle pobrana, przechowywana lub przygotowana do analizy. Przygotowanie próbki stanowi zazwyczaj najbardziej żmudny etap analizy i jest najpoważniejszym źródłem błędów. Jest to szczególnie ważny etap w analizie specjacyjnej.
Techniki łączone w analizie specjacyjnej
Wraz z rozwojem metod i technik analitycznych zmienia się pojęcia analizy śladowej [4]. Konieczność ciągłego obniżania granic wykrywalności do ekstremalnie niskich poziomów stężeń spowodowało, że dotychczas stosowane metody analityczne nie zawsze są odpowiednie do obecnych wymagań. W związku z tym łączy się różne metody separacyjne i metody detekcji, co określane jest ogólną nazwą techniki łączone. Jako metody separacyjne wykorzystuje się przede wszystkim metody chromatograficzne, a jako metody detekcji – metody spektroskopowe [5]. Do technik łączonych zaliczyć można także połączenia kliku metod chromatograficznych. Technika łączona powinna być selektywna wobec oznaczanych analitów, czuła w szerokim zakresie stężeń i powinna umożliwiać możliwie jak najlepszą identyfikację oznaczanych substancji. Wybór odpowiedniej techniki łączonej powinien być uwarunkowany naturą analitu, łatwością połączenia różnych metod, wymaganą czułością oznaczeń oraz dostępnością urządzeń.
Metody chromatograficzne takie jak przede wszystkim: chromatografia gazowa (ang. Gas Chromatography, GC), wysokosprawna chromatografia cieczowa (ang. High Performance Liquid Chromatography, HPLC) oraz będąca jej częścią chromatografia jonowa (ang. Ion Chromatography, IC) względu na możliwość szybkiego rozdzielania i oznaczania substancji w próbkach o złożonych matrycach należą do najbardziej rozpowszechnionych metod instrumentalnych w chemii analitycznej. Poza nimi ważną grupą metod separacyjnych są metody oparte na zjawisku elektroforezy takie jak m.in.: kapilarna elektroforeza strefowa (ang. Capillary Zone Electrophoresis, CZE), kapilarne ogniskowanie izoelektryczne (ang. Capillary Isoelectric Focusing, CIEF), żelowa elektroforeza kapilarna (ang. Capillary Gel Electrophoresis, CGE), izotachoforeza kapilarna (ang. Capillary Isotachophoresis, CITP) czy micelarna elektrokinetyczna chromatografia kapilarna (ang. Micellar Electrokinetic Capillary Chromatography, MECC) [6].
Do najczęściej stosowanych metod detekcji w analizie specjacyjnej należą: spektrometria mas (ang. Mass Spektrometry, MS), oraz spektrometria mas z plazmą indukcyjnie sprzężoną (ang. Inductively Coupled Plasma Mass Spectrometry, ICP-MS). Ponadto można stosować m.in.: płomieniową atomową spektrometrię absorpcyjną (ang. Flame Atomic Absorption Spectrometry, FAAS), elektrotermiczną atomową spektrometrię absorpcyjną (ang. Electrothermal Atomic Absorption Spectrometry, ET AAS), atomową spektrometrię fluorescencyjną (ang. Atomic Fluorescence Spektrometry, AFS), spektrometrię emisji optycznej ze wzbudzeniem w plazmie indukcyjnie sprzężonej (ang. Inductively Coupled Plasma Atomic Emission Spectroscopy, ICP-AES), mikrofalowo indukowaną plazmę z atomową spektrometrią absorpcyjną (ang. Microvawe Inducted Plasma Atomic Emission Spektrometry, MIP AES), spektroskopię w podczerwieni z transformacją Fouriera (ang. Fourier Transform Infrared Spectroscopy, FTIR) czy spektroskopię magnetycznego rezonansu jądrowego (ang. Nuclear Magnetic Resonance, NMR).
Jako źródła jonizacji można stosować: jonizację w polu (ang. Electrospray Ionization, ESI), jonizację chemiczną pod ciśnieniem atmosferycznym (ang. Atmospheric Pressure Chemical Ionization, APCI) lub jonizację fotochemiczną pod ciśnieniem atmosferycznym (ang. Atmospheric Pressure Photochemical Ionization, APPI). Zakres tych zastosowań zależy od polarności i masy analitów oraz natężenia przepływu eluentu. W układach IC-MS jako źródło jonizacji stosuje się wyłącznie jonizację w polu, co w przeciwieństwie do pozostałych metod jonizacji pozwala ona przeprowadzać do fazy gazowej także jony wielowartościowe. Z kolei detekcja MS może być prowadzona w trybie monitorowania wybranego jonu (ang. Selected Ion Monitoring, SIM) lub skanowania (ang. Scan Mode, SM). W pierwszym przypadku otrzymuje się informacje o masie analitu, a metoda ta stosowana jest zazwyczaj do analizy ilościowej. W trybie skanowania uzyskuje się informacje na temat czasów retencji, widm masowych oraz rozkładu mas. Ten tryb stosuje się przede wszystkim do analiz jakościowych. Identyfikacja jest relatywnie prosta w przypadku analitów o niskich masach. Dla dużych cząsteczek trudności z identyfikacją związane są przede wszystkim z większą ilością możliwości uzyskania widm o tych samych stosunkach masy do ładunku.
Na rysunku 1 przestawiono najpopularniejsze metody separacyjne oraz metody detekcji wykorzystywane w technikach łączonych wraz z rodzajem oznaczanych analitów.
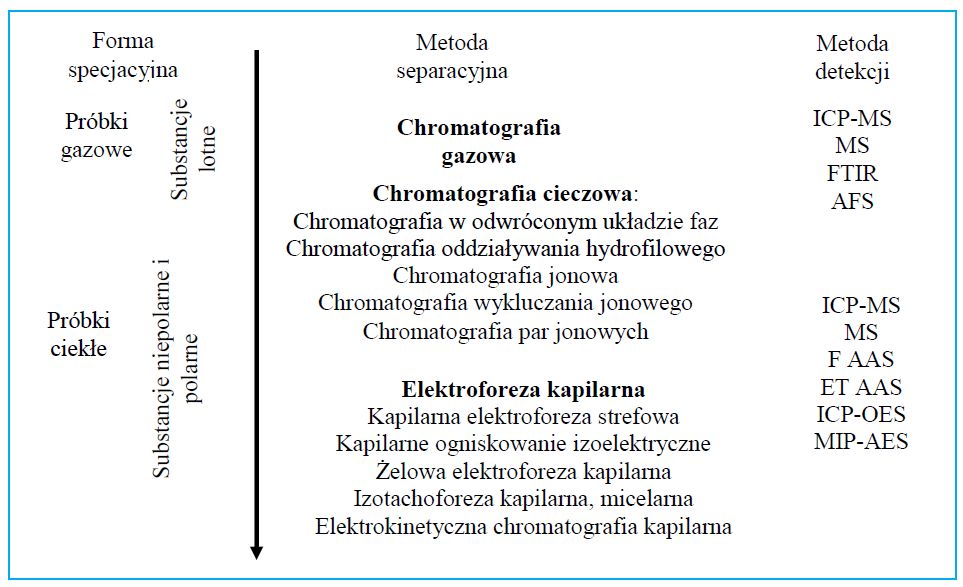
Rys. 1. Przykładowe techniki łączone stosowane w analizie specjacyjnej.
Najpopularniejszą instrumentalną metodą rozdzielania i oznaczania nieorganicznych i orga nicznych anionów i kationów jest chromatografia jonowa [7]. Połączenie chromatografu jonowego z detektorami ICP-MS lub bezpośrednio ze spektrometrem mas daje potężne narzędzie analityczne nie tylko w zakresie analizy specjacyjnej. O ile relatywnie łatwe było połączenie chromatografu gazowego z detektorem spektrometrii mas, w przypadku połączenia chromatografu cieczowego duża objętość eluatu oraz różnice ciśnień w kolumnie chromatograficznej i w spektrometrze stanowiły poważne przeszkody we wprowadzeniu takich układów do praktyki laboratoryjnej. Prace nad technikami łączonymi takimi jak HPLC-MS czy HPLC-ICP-MS trwały już od lat 80-tych minionego wieku, lecz na skalę komercyjną zaczęto je stosować dopiero pod koniec XX wieku.
Tym niemniej rozwój tych technik przybiera na znaczeniu, o czym świadczyć może rosnący zakres ich zastosowań i liczba prac na ten temat [17]. Na rysunku 2 zestawiono liczbę artykułów opublikowanych w międzynarodowych czasopismachnaukowych z lat 1996-2013 zawierających słowa kluczowe takie jak: GC, HPLC, IC, CE w połączeniu z ICP-MS lub MS oraz „speciation”.
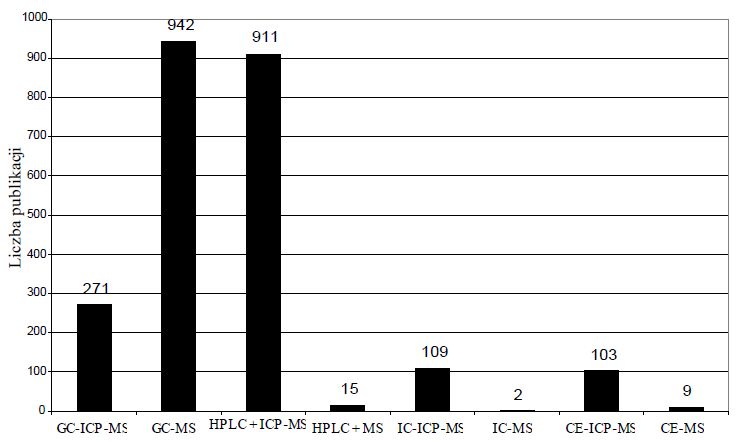
Rys. 2. Liczby artykułów dotyczących wykorzystania różnych technik łączonych w analizie specjacyjnej opublikowanych w latach 1996-2013 w renomowanych czasopismach naukowych (na podstawie słów kluczowych).
Przykłady zastosowań technik łączonych IC-ICP-MS i IC-MS w analizie specjacyjnej
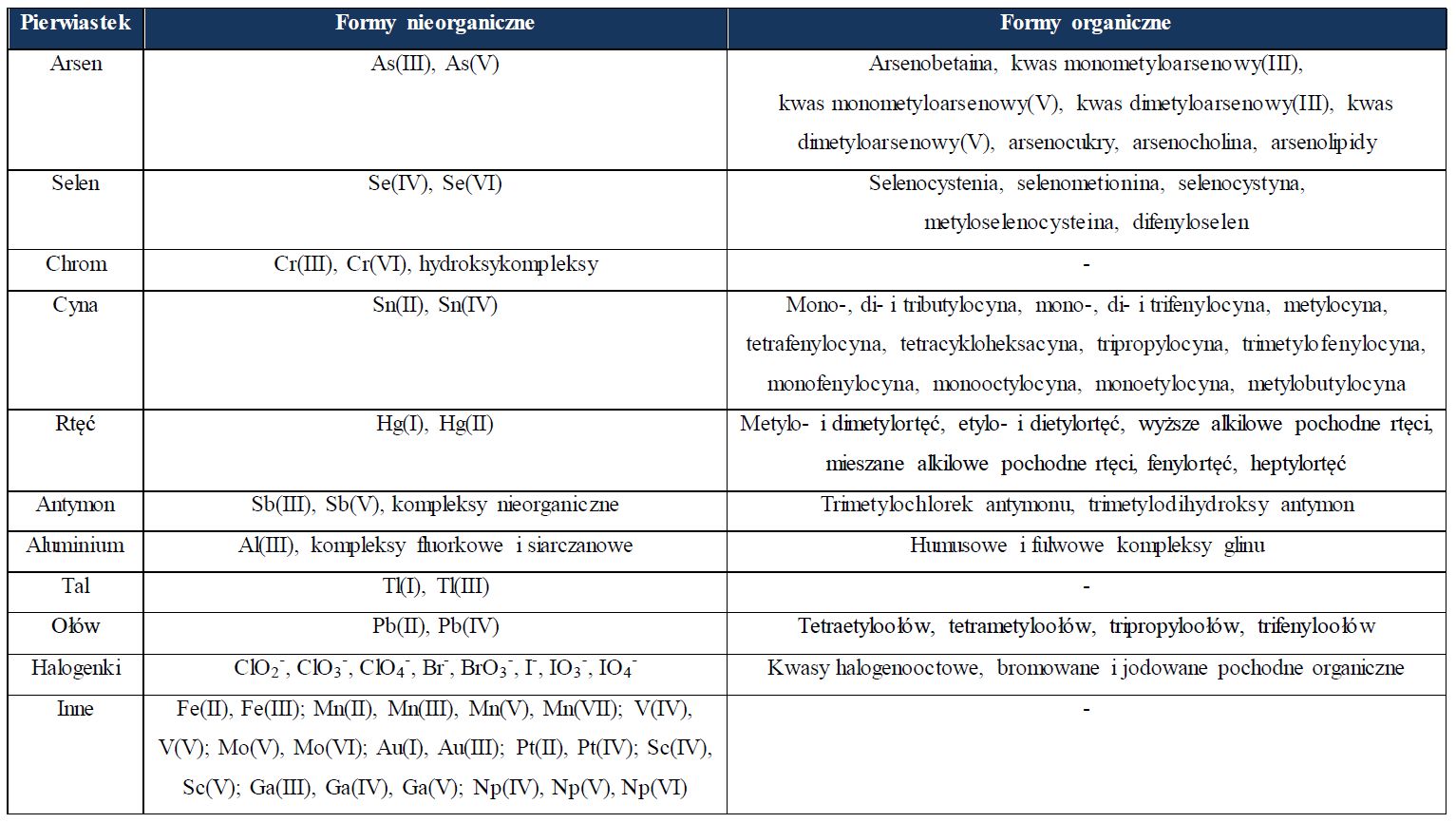
Pierwiastki, które ze względu na właściwości fizyko-chemiczne oraz toksykologiczne swoich różnych form organicznych i nieorganicznych są najczęściej przedmiotem badań w analizie specjacyjnej z wykorzystaniem technik łączonych to: arsen, selen, chrom, cyna, rtęć, antymon, aluminium, tal, ołów, halogenki, platynowce, metale ziem rzadkich i radionuklidy. Ich formy jonowe zarówno organiczne, jak i nieorganiczne mogą być oznaczane metodą chromatografii jonowej w połączeniu z detektorami ICP-MS lub MS [8]. Techniki łączone IC-ICP-MS oraz IC-MS znalazły zastosowania przede wszystkim w analizie specjacyjnej wybranych ubocznych produktów dezynfekcji wód [9] oraz jonów metali i metaloidów [10]. W tabeli 1 podano przykłady analitów oznaczanych różnymi technikami łączonymi, w tym opartymi o chromatografię jonową sprzężoną z detektorami ICP-MS lub MS.
Tab. 1. Przykłady metali i metaloidów oraz ich form specjacyjnych oznaczanych technikami łączonymi.
Analiza specjacyjna z wykorzystaniem technik łączonych (m.in. IC-ICP-MS i IC-MS) pomimo znacznych postępów poczynionych w minionych latach wciąż jest młodą dziedziną chemii analitycznej. Perspektywy jej dalszego rozwoju i popularyzacji uzależnione są od wielu czynników, takich jak m.in.: rozwój nowych metod przygotowania próbek, metod separacyjnych i metod detekcji, oraz dostępności certyfikowanych materiałów referencyjnych. Techniki łączone stwarzają ogromne, nieznane dotychczas możliwości, a ich główne zalety to: ekstremalnie niskie granice wykrywalności i granice oznaczalności oraz bardzo dobra dokładność i powtarzalność oznaczeń [11]. Tak jak wszystkie inne cechują je także określone ograniczenia, takie jak: wysoka cena przyrządów oraz wymagania doskonałego opanowania metodyk analitycznych i szczegółowej znajomości przyrządów przez ich użytkowników. To z kolei powoduje, że nie są one powszechnie dostępne i stosowane rutynowo w laboratoriach. Są to systemy drogie, stosowane raczej do prac naukowych niż do analiz rutynowych.
W Instytucie Podstaw Inżynierii Środowiska PAN od 25 lat prowadzimy badania związane z zastosowaniami chromatografii jonowej w analityce środowiskowej, a od kilku lat także dotyczące technik łączonych [12, 13]. Przykład zastosowania techniki IC-ICP-MS do jednoczesnego oznaczania nieorganicznych form arsenu, antymonu talu przestawiono na rysunku 3.
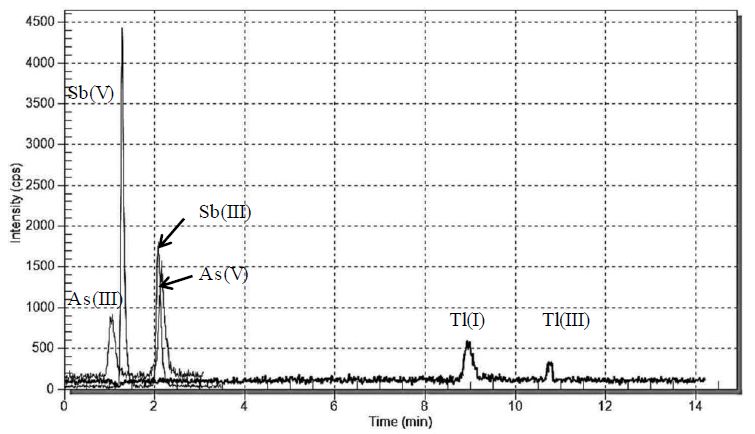
Rys. 3. Chromatogram jednoczesnego rozdzielania jonów As(III), As(V), Sb(III), Sb(V), Tl(I) oraz Tl(III) w próbce wody z rzeki Kłodnica.
Literatura:
[1] T.M. Florence, G.E. Batley, P. Benes, Chemical Speciation in Natural Waters, Crit. Rev. Anal. Chem., 9, 219 (1980).
[2] D.M. Templeton, F. Ariese, R. Cornelis, L.G. Danielsson, H. Muntau, H. Leeuwen, R. Łobiński, Guidelines for Terms Related to Chemical Speciation and Fractionation of Elements. Definitions, Structural Aspects, and Methodological Approaches. (IUPAC Recommendations 2000), Pure Appl. Chem., 72, 1453 (2000).
[3] Specjacja chemiczna - Problemy i możliwości, pod red. D.Barałkiewicz i E.Bulskiej, Wydawnictwo Malamut, Warszawa, (2009).
[4] Analiza śladowa – Zastosowania, pod red. I.Baranowskiej, wydawnictwo Malamut, Warszawa, (2013).
[5] L.A. Ellis, D.J. Roberts, D.J. Chromatographic and Hyphenated Methods for Elemental Speciation Analysis in Environmental Media, J. Chromatogr. A, 774, 3 (1997).
[6] Techniki elektromigracyjne - Teoria i praktyka, pod red. B. Buszewskiego, E. Dziubakiewicz, M. Szumskiego, Wydawnictwo Malamut, Warszawa, (2012).
[7] Michalski R., Chromatografia jonowa. Podstawy i zastosowania, WN-T, Warszawa, 2005.
[8] Michalski R., Application of IC-MS and IC-ICP-MS in environmental research, Current Trends in Mass Spectrometry, LC-GC North America Suppl. S, October 2012, 32-36.
[9] Michalski R., Analysing Inorganic Disinfection By-products by Ion Chromatography, LC GC Europe, May, 2011, 18-23.
[10] Michalski R., Jablonska M., Szopa S., Łyko A., Application of Ion Chromatography with ICP-MS or MS Detection to the Determination of Selected Halides and Metal/Metalloids Species, Crit. Rev. Anal. Chem., 41, 133 (2011).
[11] Michalski R., Jabłońska M., Szopa S., Role and Importance of Hyphenated Techniques in Speciation Analysis [w] Speciation Studies in Soil, Sediment and Environmental Samples, Eds. Sezgin Bakirdere, Science Publishers/CRC Press/Taylor&Francis Group, (2013), pp.242-262.
[12] Michalski R., Jablonska-Czapla M., Szopa S., Łyko A., Hyphenated methods for speciation analysis [w] Encyclopedia of Analytical Chemistry, eds R.A. Meyers, John Wiley: Chichester. DOI: 10.1002/9780470027318.a9291. Published 18th September 2013.
[13] Jabłońska-Czapla M., Szopa S., Grygoyć K., Łyko A., Michalski R., Development and validation of HPLC-ICP-MS method for the determination inorganic Cr, As and Sb speciation forms and its application for Pławniowice reservoir (Poland) water and bottom sediments variability study, Talanta, 120, (2014), 475-483.






