Jarosław Szulfer
Polpharma SA, Badania i Rozwój
strony wersji drukowanej: 40-43
strony wersji drukowanej: 40-43
Fakt, że przemysł chemiczny oddziałuje niekorzystnie na środowisko jest oczywisty, dlatego nieodzowne jest świadome i konsekwentne minimalizowanie tego wpływu. Celem nadrzędnym jest ograniczanie wytwarzania szkodliwych czynników dla zdrowia człowieka. Za ojca „Zielonej chemii” uznaje się amerykańskiego naukowca Paula Anastasa, który jest współtwórcą 12 zasad, których przestrzeganie gwarantuje łagodzenie negatywnych skutków działalności chemicznej. Chemia analityczna podlega tym samym regułom. Pojęcie „zielonej chemii analitycznej” zostało ukute przez profesora Politechniki Gdańskiej Jacka Namieśnika pod koniec lat dziewięćdziesiątych.
Zazwyczaj zadania stawiane przed analitykami same w sobie są dużymi wyzwaniami, stąd często dbałość o wpływ analizy na środowisko wydaje się jednym z ostatnich kryteriów oceny opracowywanej metody. Sojusznikiem zielonej chemii bywa jednak niekiedy ekonomia. Najlepiej uwidocznił to kryzys związany z dostępnością acetonitrylu sprzed kilku lat. W krótkim czasie cena tego rozpuszczalnika wzrosła nawet dziesięciokrotnie, nie mówiąc o tym, że często w ogóle był niedostępny. W wielu laboratoriach zaczęto intensywne prace nad ograniczaniem jego zużycia, bądź zamianą np. na etanol, co idealnie wpisuje się w podstawowe założenia zielonej chemii analitycznej.
Chromatografia cieczowa
W większości nowoczesnych laboratoriów analitycznych, techniki chromatograficzne stanowią podstawę ich funkcjonowania, dlatego ograni-czenie ilości stosowanych odczynników, a co za tym idzie generowanych odpadów wydaje się być kluczowym aspektem. Najpopularniejszym rozpuszczalnikiem stosowanym w chromatografii cieczowej jest acetonitryl. Ze względu na jego właściwości fizykochemiczne (m.in. mała lepkość, niska absorpcja w zakresie UV) wielu analityków preferuje jego użycie jako odczynnika pierwszego wyboru w przygotowywaniu fazy ruchomej. Jak wynika z doświadczenia, w niektórych przypadkach faktycznie próby zastąpienia acetonitrylu innymi rozpuszczalnikami kończą się niepowodzeniem i jedynym rozwiązaniem jest ilościowe ograniczenie jego użycia w danej analizie. Można to uzyskać na dwa sposoby: skrócenie analizy lub zmniejszenie przepływu fazy ruchomej.
Od wielu lat na rynku dostępne są kolumny o mniejszej średnicy wewnętrznej w stosunku do standardowej, tj. 4,6 mm. Przykładem mogą być kolumny o średnicy wewnętrznej 3,0 mm dedykowane dla pracy ze zmniejszonym zużyciem rozpuszczalników. Tak jak z powodzeniem, bez utraty sprawności układu, możliwe jest skalowanie przepływu fazy ruchomej „w górę” np. w celach preparatywnych, tak możliwe jest zmniejszanie średnicy kolumny, a co za tym idzie przepływu. Ekwiwalent przepływu fazy ruchomej dla zmienionych wymiarów kolumny można wyznaczyć posługując się wzorem:
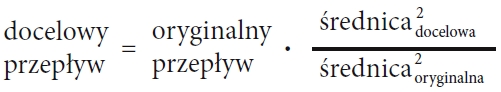
W przypadku kolumny o średnicy wewnętrznej 3,0 mm zużycie fazy ruchomej będzie stanowiło około 40% zużycia obserwowanego dla kolumny o standardowej średnicy 4,6 mm. Niestety nie można pomijać faktu, że kolumna o mniejszej średnicy zawiera mniej złoża, a co powoduje, że można załadować mniej analitu. Może to być krytyczne, szczególnie w przypadku próbek, w których oznacza się substancje na niskim poziomie.
Komercyjnie dostępne są również kolumny o jeszcze mniejszej średnicy np. 2,1 mm, 1,0 mm, a nawet 0,1 mm, ale ich zastosowanie w praktyce ogranicza się przede wszystkim do systemów wyposażonych w detektory MS. W przypadku kolumn o średnicy 1,0 mm i poniżej, systemy powinny być wyposażone w odpowiednie mikro- lub nanolitrowe pompy. Kilka lat temu na rynku pojawiały się kolumny z ziarnem o średnicy poniżej 2 µm, dzisiaj oferowane praktycznie przez wszystkich producentów. Posiadają one znacznie wyższą sprawność niż konwencjonalne kolumny z ziarnem 5 µm, dlatego możliwe było ograniczenie ich wymiarów tak średnicy, jak i długości bez pogorszeni rozdziału. W konsekwencji, przy zachowaniu stałego przepływu liniowego standardowy współczynnik przepływu dla kolumn o średnicy 4,6 mm wynoszący 1 ml/min, dla kolumny o średnicy 2,1 mm, będzie wynosił 0,21 ml/min, co już daje 5-krotne ograniczenie zużycia rozpuszczalników. Dodatkowo, dzięki efektowi podniesienia sprawność kolumny przez zmniejszenie średnicy ziarna złoża, możliwe staje się skrócenie długości kolumny przy zachowaniu odpowiedniej rozdzielczości układu. Skrócenie długości kolumny przy danym przepływie fazy ruchomej powoduje proporcjonalne skrócenie czasów retencji, a co za tym idzie czasu analizy i ilości zużytych odczynników. Na ryc.1 przedstawiono oszczędności jakie można osiągnąć transferując przykładową analizę z klasycznych warunków HPLC do UHPLC.
Chromatogram 1
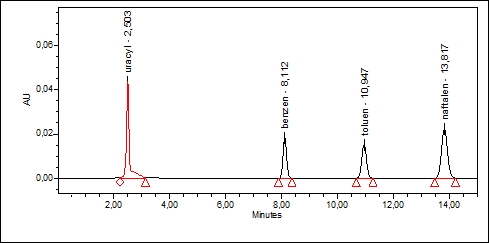
Waters Alliance 2695
kolumna: Atlantis T3
250x4,6 mm 5 µm
faza: H2O:ACN (40:60)
przepływ: 1,0 ml/min
temperatura kolumny: 25°C
detekcja: 254 nm
objętość nastrzyku: 10 µl
Nnaftalen= 19553
Rtoluen-naftalen= 8,1
Chromatogram 2
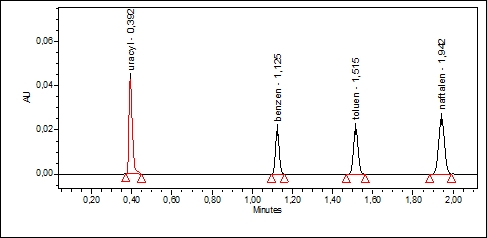
Waters ACQUITY UPLC
kolumna: Acquity HSS T3
100x2,1 mm 1,8 µm
faza: H2O:ACN (40:60)
przepływ: 0,525 ml/min
temperatura kolumny: 25°C
detekcja: 254 nm
objętość nastrzyku: 0,8 µl
Nnaftalen= 19950
Rtoluen-naftalen= 8,7
Ryc. 1. oszczędności jakie można osiągnąć transferując przykładową analizę z klasycznych warunków HPLC do UHPLC.
Należy zwrócić uwagę, że bez straty sprawności czas analizy skrócono około siedmiokrotnie, a zużycie odczynników około 15-krotnie!
Przy okazji kolumn ze zmniejszoną średnicą ziaren warto wspomnieć o kolumnach z ziarnem o nieporowatym rdzeniu, które, podobnie jak kolumny z ziarnem o średnicy poniżej 2 µm, dzięki zwiększonej sprawności umożliwiają efektywną pracę na krótkich kolumnach, co daje pozytywny efekt ograniczenia zużycia rozpuszczalników. Kolumny tego typu, dzięki wąskiej dystrybucji wielkości ziaren, generują stosunkowo niskie ciśnienie wsteczne, przez co, bez większych problemów, można je stosować w klasycznych systemach HPLC. Niestety w takim przypadku ogromny wpływ na ostateczną sprawność układów wyposażonych w kolumny z nieporowatym rdzeniem mają efekty pozakolumnowe, dlatego przed ich użyciem należałoby zoptymalizować układ poprzez minimalizację objętości martwych (wymiana kapilar, miksera, nastrzykiwacza, celi detektora).
Z punktu widzenia zielonej chemii analitycznej w przypadku chromatografii cieczowej nie tylko zmniejszenie zapotrzebowania na rozpuszczalniki organiczne przynosi pozytywne efekty. Zamiana acetonitrylu na inne, bardziej przyjazne dla środowiska rozpuszczalniki jak np. etanol, wydaje się również korzystne, ze względu tak na jego pozyskiwanie jak i degradację.
Niestety do tej pory etanol, ze względu na swoją wysoką lepkość, nie jest rozpuszczalnikiem powszechnie stosowanym w chromatografii. Sytuacja ta może jednak ulec zmianie, ponieważ obecnie większość producentów systemów chromatograficznych oferuje sprzęt zdolny pracować przy ciśnieniu ponad 1000 barów, więc wspomniana lepkość wydaje się nie być już takim problemem. Z doświadczenia wynika, że w wielu przypadkach zamiana acetonitrylu na metanol w składzie fazy ruchomej zmienia selektywność układu. Podobnie sprawa wygląda w przypadku etanolu.
Chromatografia gazowa
Chromatografia gazowa, w porównaniu do cieczowej, ze względu na fakt, że ewentualne użycie rozpuszczalników ogranicza się jedynie do etapu przygotowania próbek, już w założeniu posiada bardziej zielony charakter. Jak wiadomo technika ta wykorzystywana jest do badania substancji lotnych i półlotnych.
Oczywiście, możliwe jest również upochodnianie nielotnych substancji nadające im lotny charakter. Jednak w tym ostatnim przypadku z punktu widzenia zielonej chemii, korzystniejsze byłoby bezpośrednie oznaczanie np. przy użyciu techniki LC/MS.
Istotnym zagadnieniem w chromatografii gazowej, z punktu widzenia zielonej chemii, jest wybór gazu nośnego. Obecnie najpopularniejszym gazem nośnym jest hel, jednak jego pozyskanie jest znacznie droższe od pozyskania wodoru, który nie ustępuje helowi w jakości rozdziałów chromatograficznych. Co więcej, ze względu na właściwości wodoru, w porównaniu do analizy wykonanej przy użyciu helu, uzyskując te same rozdzielczości, analiza wykonana przy użyciu wodoru będzie o około 30% krótsza. Ze względów bezpieczeństwa, w większości laboratoriów, nadal używa się helu jako gazu nośnego, chociaż nowoczesne generatory wodoru gwarantują bezpieczeństwo, a dodatkowo, co jest bardzo korzystne z punktu widzenia zielonej chemii, do produkcji wodoru potrzebują jedynie wody i energii elektrycznej. Dodatkowo, używanie generatora eliminuje potrzebę transportu zbiorników, co nie jest bez znaczenia dla środowiska naturalnego. Inny z gazów – azot, mimo, iż porównywalnie tani jak wodór, w większości przypadków nie jest alternatywą dla w/w gazów z powodu powolnego transportu masy przez co analizy stają się znacznie dłuższe.
Podobnie, jak w przypadku chromatografii cieczowej, dzięki zmniejszeniu średnicy wewnętrznej kolumny GC można uzyskać krótsze czasy analizy. Zważywszy na fakt, że konsumpcja energii elektrycznej w trakcie analiz GC jest znacząca, to ograniczenie jej trwania korzystnie wpływa na zielony wymiar tej techniki. Dodatkowo, w odróżnieniu do chromatografii cieczowej, w przypadku GC zmniejszenie średnicy wewnętrznej kolumny powoduje zwiększenie sprawności układu, dzięki czemu możliwe jest użycie krótszej kolumny oraz skrócenie czasu analizy bez straty rozdzielczości. Co więcej, zmniejszając średnicę kolumny optymalna prędkość liniowa przepływu gazu zwiększa się, co daje kolejną możliwość skrócenia czasu analizy.
Chromatografia z fazą ruchomą w stanie nadkrytycznym
Chromatografia z fazą ruchomą w stanie nadkrytycznym (SFC) to technika znana od ponad 25 lat, ale dopiero od kilku lat na rynku dostępne są systemy, które spełniają ostre wymagania stawiane między innymi przez przemysł farmaceutyczny. Zasadniczą zaletą tej techniki jest fakt, że jako faza ruchoma w większości przypadków stosowany jest CO2 w stanie nadkrytycznym, a rozpuszczalniki organiczne stanowią wyłącznie rolę modyfikatorów fazy. Oczywiście, naturalną obawą, jeśli chodzi o zgodność tej techniki z zasadami zielonej chemii jest fakt, że CO2 jest gazem powodującym efekt cieplarniany, ale w rzeczywistości gaz stosowany w analizie odzyskiwany jest z procesów przemysłowych, więc ogólna jego pula się nie zwiększa. Co więcej, możliwa jest praca w obiegu zamkniętym, gdzie po analizie gaz jest odzyskiwany i ponownie sprężany, choć opłacalne jest to dopiero w skali półpreparatywnej i preparatywnej. Obecnie SFC stosowana jest głównie do oznaczeń związków chiralnych, jak alternatywa dla wyjątkowo toksycznych faz normalnych (heksan, heptan, octan etylu, chlorowcopochodne). Dodatkowo, dzięki właściwościom CO2 w stanie nadkrytycznym, sprawność układu na tej samej kolumnie jest wyższa, co pozwala na skrócenie czasu analizy. Kilka miesięcy temu firma Waters zaprezentowała nowy system tj. UPSFC (UltraPerformance SFC).Wykorzystano w nim zdobycze technologii UHPLC tj. kolumny z ziarnem o średnicy poniżej 2 µm i zoptymalizowany układ chromatograficznym pod kątem minimalizacji objętości martwych. Tak jak w przypadku chromatografii cieczowej pozwala on na kilkakrotne skrócenie czasu analizy i zmniejszenie zużycia odczynników. Zużycie najczęściej stosowanego modyfikatora fazy ruchomej – metanolu, na jedną analizę nie przekracza 1 ml.
Kolejną ważną zaletą stosowania CO2 jest łatwość usuwania fazy ruchomej w przypadku chromatografii preparatywnej, w porównaniu do klasycznej chromatografii cieczowej, a szczególnie z zastosowaniem faz odwróconych. Ograniczony został czas oraz ilość energii potrzebnej na odparowanie rozpuszczalników. Wszystkie te czynniki pozwalają nadać technice SFC miano przyjaznej dla środowiska.
Przygotowywanie próbek
Na etap przygotowania próbek przeważnie zużywa się największe ilości rozpuszczalników, a do tego najczęściej są to substancje najniebezpieczniejsze z punktu widzenia ekologii (w tym chlorowcopochodne), dlatego każda oszczędność w ich zużyciu jest korzystna. Obecnie coraz popularniejsze są techniki, w których zmniejszono lub całkowicie wyeliminowano potrzebę używania rozpuszczalników na etapie przygotowania próbek. Do takich technik zaliczyć można m.in.: ekstrakcję do fazy stałej (SPE), mikroekstrakcję do fazy stałej (SPME), dynamiczną ekstrakcję do fazy stałej (SPDE), ekstrakcję z użyciem ultradźwięków (UE), ekstrakcję płynem w stanie nadkrytycznym (SFE), mikroekstrakcję z wykorzystaniem włókna z osadzoną fazą ciekłą (LPME), mikroekstrakcję do fazy ciekłej wspomagana promieniowaniem mikrofalowym oraz wiele innych.
Podsumowanie
Zielona chemia stara się ograniczyć, a najlepiej wyeliminować zanieczyszczenia u źródła w celu ochrony zdrowia ludzkiego i środowiska naturalnego.
W artykule zaprezentowano kilka najnowszych proekologicznych zdobyczy w dziedzinie chemii analitycznej, ale niestety rzeczywistość pracy analityka jest zazwyczaj odmienna. Dysponuje on najczęściej podstawowym wyposażeniem i wspomniane wyżej techniki pozostają jedynie w sferze marzeń. Jakkolwiek także on może uczynić krok w stronę zielonej chemii podejmując kilka prostych działań. Chodzi przede wszystkim o świadome planowanie i prowadzenie eksperymentów, np. przygotowywanie odpowiedniej ilości faz ruchomych, jeśli kolejne serie próbek badane są w dłuższych odstępach czasu (np. co kilka godzin) zmniejszanie przepływu fazy ruchomej, racjonalne czasy płukania i kondycjonowania aparatów. Ale chyba najważniejsza jest zasada, aby badania wykonywać raz a dobrze, kontrolować przebieg analizy na bieżąco by móc jak najszybciej interweniować.





