Wojciech Mrozik
Katedra i Zakład Chemii Nieorganicznej, Gdański Uniwersytet Medyczny
strony wersji drukowanej: 31-35
strony wersji drukowanej: 31-35
Produkcja przemysłowa oraz zastosowanie konwencjonalnych rozpuszczalników organicznych
w różnych gałęziach gospodarki prowadzi do istotnego zanieczyszczania środowiska naturalnego. Stosowane w przemyśle jako wszelkiego rodzaju media reakcji chemicznych, a także występujące jako odpady produkcyjne stałe czy ciekłe, zwykle charakteryzują się wysoką prężnością par, co bezpośrednio przekłada się na ich emisje do atmosfery. Tego typu zanieczyszczenia mogą migrować na bardzo dalekie odległości i powodować skażenia w miejscach gdzie ich, teoretycznie, w ogóle nie powinno być. Oprócz mobilności, konwencjonalne rozpuszczalniki organiczne zwykle cechują się dużą toksycznością, a często także mutagennością i rakotwórczością. Wymienione cechy sprawiają, że związki te stanowią duże zagrożenie dla życia i zdrowia ludzkiego, ale także dla środowiska naturalnego. Dlatego też w ostatnich latach podejmuje się próby projektowania oraz tworzenia alternatywnych rozpuszczalników, które charakteryzowałyby się przede wszystkim niską lotnością, stabilnością chemiczną i fizyczną oraz szerokim zastosowaniem i możliwością wielokrotnego wykorzystania. Tego typu myślenie charakteryzuje tzw. „zieloną chemię” (ang. green chemistry)1, czyli nowe podejście do zagadnienia syntezy i wykorzystania związków chemicznych, co ma na celu zmniejszenie zagrożenia dla środowiska i zdrowia człowieka. Filozofia ta zakłada m.in. obniżenie toksyczności oraz zwiększenie podatności na degradację wytwarzanych związków chemicznych w naturalnych systemach.
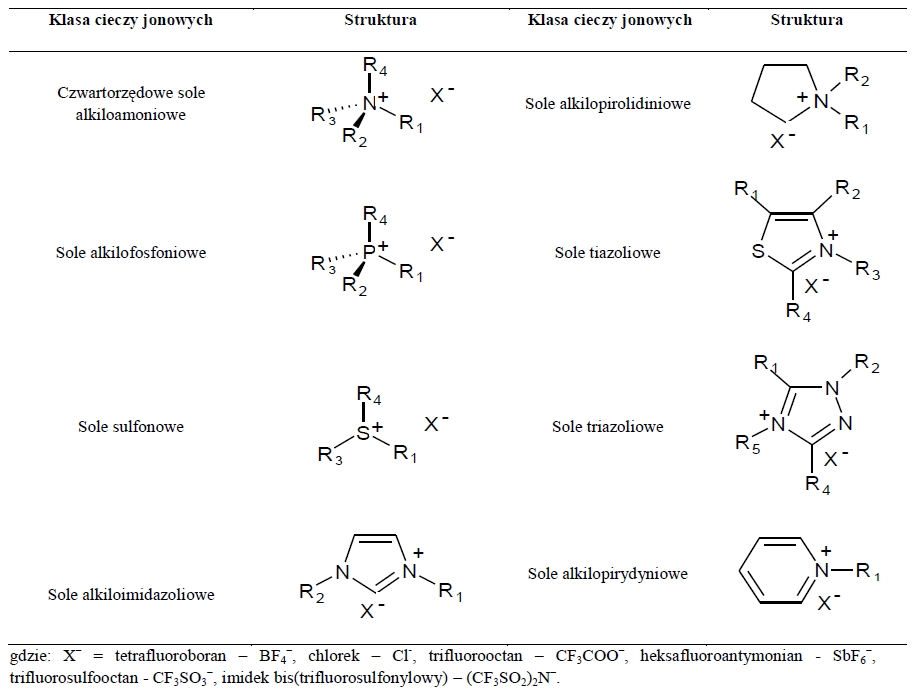
Tabela 1. Najczęściej spotykane klasy cieczy jonowych3.
Ciecze jonowe (ang. ionic liquids) to nazwa soli, których temperatury topnienia są niższe od 100oC, a duża część przedstawicieli tej klasy wykazuje stan ciekły już w temperaturze pokojowej. Ze względu na swoje bardzo zróżnicowane i unikalne właściwości fizyko-chemiczne, związki te postrzegane są w ostatnich latach jako bardzo obiecująca alternatywa dla konwencjonalnych rozpuszczalników organicznych. Ponieważ jedną z ich cech jest zaniedbywalna prężność par, niska palność oraz wysoka stabilność termiczna, bardzo szybko nadano im miano „przyjaznych środowisku”2. Jednak najważniejszą zaletą tych związków, z punktu widzenia przemysłu, jest możliwość „dostrajania” ich do potrzeb konkretnej reakcji chemicznej czy procesu separacyjnego.
Ciecze jonowe zbudowane są z dużych i niesymetrycznych kationów alkiloimidazoliowych, alkilopirydyniowych lub alkilofosfoniowych oraz mniejszych anionów nieorganicznych, a także organicznych często zawierających atom fluoru (np. tetrafluoroboran, heksafluorofosforan, imidek bis(trifluorometylosulfonylowy) i inne3,4. Coraz częściej fragmenty alkilowe kationów cieczy jonowych są dodatkowo podstawiane różnymi grupami funkcyjnymi w celu uzyskania wysokiej specyficzności powstałego związku dla potrzeb konkretnej reakcji chemicznej czy procesu technologicznego, a także np. w celu obniżenia toksyczności związku. W chwili obecnej komercyjnie dostępnych jest ponad 300 związków5, teoretycznie jednak liczba możliwych kombinacji kation-anion o właściwościach typowych dla tej grupy substancji może sięgnąć nawet 1018 6. Liczba potencjalnych zastosowań cieczy jonowych rośnie bardzo szybko. Głównym kierunkiem aplikacyjnym stanie się synteza organiczna, a zwłaszcza reakcje katalizowane przez metale przejściowe. Do tej pory potwierdzono przydatność cieczy jonowych dla przeprowa-dzenia reakcji: Friedela-Craftsa, Dielsa-Aldera, dimeryzacji, oligomeryzacji, polimeryzacji olefin, depolimeryzacji, nitrowania, oksydacji, katalitycznego uwodornienia, redukcji wodorkami metali, jonowych redukcji, reakcji Heck’a, Suzuki, izomeryzacji i krakingu, epoksydacji, oraz cyklopropanacji i halogenowania. Z chemicznego punktu widzenia, zasadnicze korzyści wynikające ze stosowania cieczy jonowych to przede wszystkim wysokie wydajności reakcji, a także lepsza chemo-, regio-, stereo- i enancjoselektywność w stosunku do rozpuszczalników konwencjonalnych. Dzięki zastosowaniu tych soli uzyskujemy selektywne wydzielanie produktów reakcji i łatwe oddzielenie od zastosowanego katalizatora7.
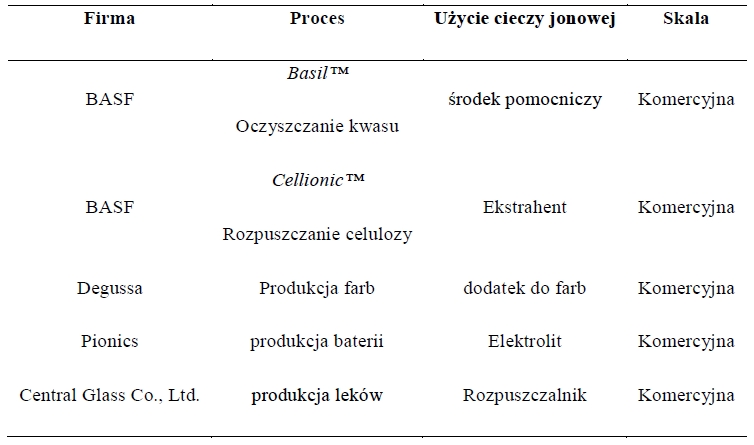
Tabela 2. Przykładowe zastosowania cieczy jonowych na skalę przemysłową5,8.
Ciecze jonowe znalazły także zastosowanie w procesach biokatalityznych. Dzięki swoim właściwościom można je stosować w układach jako czyste rozpuszczalniki, mieszaninę rozpuszczalników czy jako osobną fazę. Główną ich zaletą w tego typu reakcjach jest brak lub niewielka dezaktywacja stosowanych enzymów lub komórek. Stwierdzono także, iż szereg hydrolaz i oksydoreduktaz pozostaje aktywny w wybranych cieczach jonowych. Hydrofobowe ciecze jonowe, mogą być z powodzeniem wykorzystane jednocześnie jako rozpuszczalnik i elektrolit, wykazując szeroki zakres stabilności elektrochemicznej, dobre przewodnictwo, termiczną stabilność oraz trwałość8. Są także bardzo wydajnym i bezpiecznym elektrolitem w bateriach litowych7, a także można je wykorzystać jako superprzewodniki9. Kolejnym polem zastosowań cieczy jonowych jest wszelkiego rodzaju analityka. Wykazano przydatność tych związków elektrolitów w elektroforezie kapilarnej, modyfikatorów faz stałych w chromatografii gazowej, cieczowej czy elektroforezie5,8.
Tak naprawdę możliwości zastosowania cieczy jonowych właściwie są nieograniczone. Dzięki swoim unikalnym właściwościom sole te powoli wchodzą do użycia na skalę przemysłową. Można się więc spodziewać, że w niedalekiej przyszłości trafią one również do środowiska naturalnego. Spowodowane to może być niekontrolowanymi wyciekami podczas ich przemysłowego wykorzystania i produkcji, transportu czy np. awarii i wypadków. Pomimo swoich niewątpliwych zalet okazało się, że ciecze jonowe nie są tak „przyjazne środowisku” jak to się na początku wydawało. W związku z zaniedbywalną prężnością par, ich emisja do atmosfery nie będzie stanowić żadnego zagrożenia, jednakże tak wody, jak i środowisko glebowe mogą ulec zanieczyszczeniu. Dodatkowo Rozporządzenie UE w sprawie rejestracji, oceny, udzielania zezwoleń i stosowanych ograniczeń w zakresie chemikaliów (REACH), spowodowało konieczność określania ryzyka dla środowiska i zdrowia człowieka oraz badań właściwości wszystkich związków chemicznych, znajdujących się w obrocie handlowym na terenie Wspólnoty.
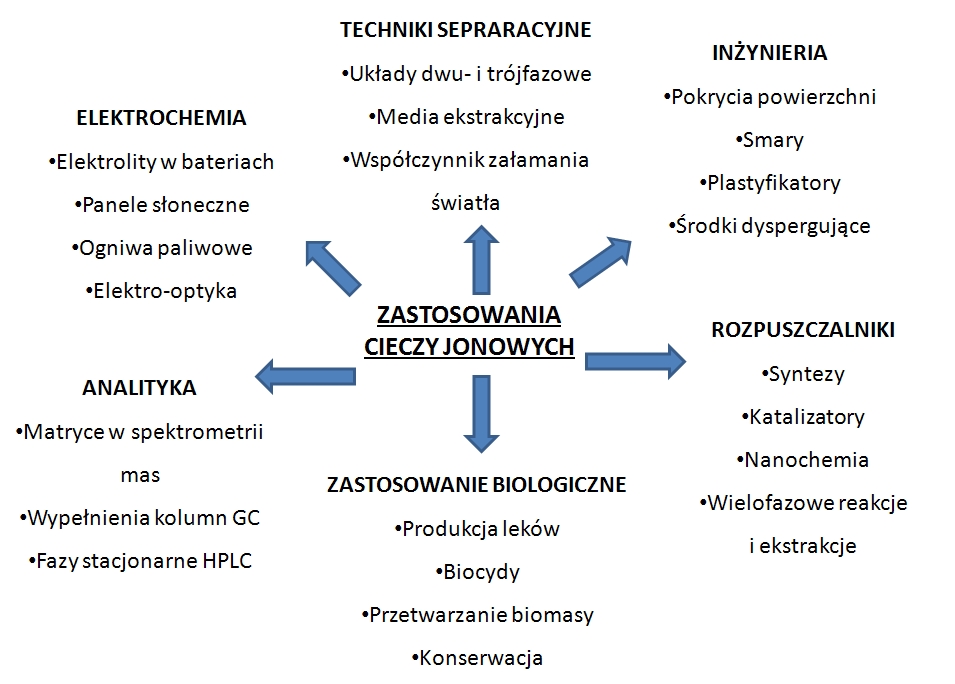
Rysunek 1. Obecne i przyszłe zastosowania cieczy jonowych.
Prospektywne badania wykazały, że ciecze jonowe, po ewentualnej emisji do środowiska, będą zachowywać się podobnie do niektórych trwałych zanieczyszczeń organicznych (np. herbicydy parakwatowe)10. W zależności od struktury, stwierdzono silną sorpcję do gleb11 lub możliwość infiltracji do wód gruntowych12, potencjalnie wysoką bioakumulację, ekotoksyczność wobec roślin i mikroorganizmów13,15 czy bardzo niski potencjał biodegradacji16,17. Dodatkowo wykazano, że związki te mogą także wykazywać cytotoksyczność wyższą niż konwencjonalne rozpuszczalniki organiczne18.
Czy to oznacza koniec kariery cieczy jonowych, zanim tak na dobre się rozpoczęła? Absolutnie nie! Dzięki takim właśnie prospektywnym badaniom udało się wyeliminować związki, które mogłyby stanowić największe obciążenie dla środowiska naturalnego. Zaczęto też modyfikować ciecze jonowe tak aby byłyby łatwiej biodegradowalne19-20, a jednocześnie nadal wykazywały przydatność w procesach przemysłowych. Unikalne właściwości tych związków, a także praktycznie nieograniczona możliwość kombinacji kation-anion pozwalają na poszukiwania struktur, które będą mogły być z powodzeniem zastosowane w przemyśle, a jednocześnie nie będą stanowiły obciążenia dla środowiska naturalnego. Powstają nowe generacje cieczy jonowych21,22, które rzeczywiście można zacząć nazywać „przyjaznymi” środowisku. Tak naprawdę, nowoczesna „zielona chemia” oparta na tych fascynujących związkach zaczyna powstawać właśnie teraz, na naszych oczach.
Literatura:
1. P.T. Anastas, J.C. Warner Green Chemistry: Theory and Practice. Oxford University Press, New York (1998)
2. Eds. J.F. Brennecke, R.D. Rogers, K.R. Seddon, Ionic Li-quids: Not Just Solvents Anymore, American Chemical Society, 2007.
3. A. Stark, K.R. Seddon, Kirk-Othmer Encyklopaedia of Chemical Technology,
4. Ed. A. Seidel, J. Wiley and Sons, Inc., Hoboken, 2007, 26, 836.
5. H. Olivier- Bourbigou, L. Magna, J Mol Catalysis A: Che-mical, 2002, 182, 419.
6. N.V. Plechkova, K.R. Seddon, Chem. Soc. Rev., 2008, 37, 123.
7. M.J Earle, K.R. Seddon, Pure Appl. Chem., 2000, 72, 1391.
8. Ed. P. Wasserscheid, T. Welton, Ionic Liquids in Synthesis, WILEY-VCH, Weinheim, 2008.
9. N. Papagergiou, Y. Athanassov, M. Armand, P. Bonhote, H. Patterson, A. Azam, M. Gratzel, J. Electrochem. Soc., 1996, 143, 3099.
10. R. Hagiwara, Electrochem., 2002, 70, 130.
11. Jastorff, R. Störmann, J. Ranke, K. Mölter, F. Stock, B. Oberheitmann, W. Hoffman, J. Hoffmann, M. Nüchter, B. Ondruschka and J. Filser, Green Chem. 5 (2003) 136.
12. P. Stepnowski, Aust. J. Chem. 58 (2005) 170.
13. W. Mrozik, C. Jungnickel, T. Ciborowski, W.R. Pitner, J. Kumirska, Z. Kaczyński, P. Stepnowski, J. Soil Sediment, 2009, 9, 237.
14. K. Docherty, S.Z. Hebbeler, C.F. Kulpa Jr., Green Chem., 2006, 8, 560.
15. A. Latała, P. Stepnowski, M. Nędzi, W. Mrozik Aquatic Toxicol., 2005,73, 91.
16. S. Stolte, J. Arning, U. Bottin-Webber, A. Muller, W.-R. Pitner, U. Welz-Bierman, B. Jastorff, J. Ranke, Green Chem., 2007, 9, 760.
17. E.M. Siedlecka, W. Mrozik, Z. Kaczyński, P. Stepnowski, J. Hazard. Mater., 2007, 154, 893.
18. K. Docherty, Ch.F. Kulpa Jr., Green Chem., 2005, 7, 185.
19. A.C. Składanowski, P. Stepnowski, K. Kleszczyński, B. Dmochowska, Environ. Toxicol. Pharmacol., 2005, 19, 291.
20. N. Gathergood, M.T. Garcia, P.J. Scammells, Green Chem., 2004, 3, 166.
21. N. Gathergood, P.J. Scammells, Austr. J. Chem., 2002, 55, 557.
22. H. Ohno, O. Fukumoto, Acc. Chem. Res., 2007, 40, 1122.
23. Y. Fukaya, Y. Iizuka, K. Sekikawa, H. Ohno, Green Chem., 2007, 9, 1155.





