Hubert Cieśliński
Katedra Mikrobiologii, Wydział Chemiczny, Politechnika Gdańska
strony wersji drukowanej: 23-26
strony wersji drukowanej: 23-26
Enzymy produkowane przez wybrane gatunki bakterii, drożdży lub pleśni pełnią kluczową rolę w produkcji dóbr konsumpcyjnych w przemyśle spożywczym, chemicznym, farmaceutycznym, tekstylnym, kosmetycznym oraz agrochemicznym. Według opublikowanej w 2010 roku prognozy, światowy rynek enzymów, głównie stosowanych jako przemysłowe biokatalizatory, osiągnie w roku 2013 wartość 7 mld dolarów amerykańskich. Ogromną większość stosowanych w tym celu enzymów stanowią hydrolazy, enzymy przeprowadzające reakcję rozcinania wiązań chemicznych z zaangażowaniem cząsteczek wody. Do tej grupy enzymów należą m.in. takie hydrolazy jak: lipazy, proteazy, celulazy, ksylanazy, β-D-glukozydazy, β-D-galaktozydazy, α-amylazy. Przykłady konkretnych zastosowań wybranych hydrolaz w poszczególnych gałęziach przemysłu zostały przedstawione w tabeli 1.
Tabela 1. Przykłady wybranych zastosowań enzymów w produkcji przemysłowej.
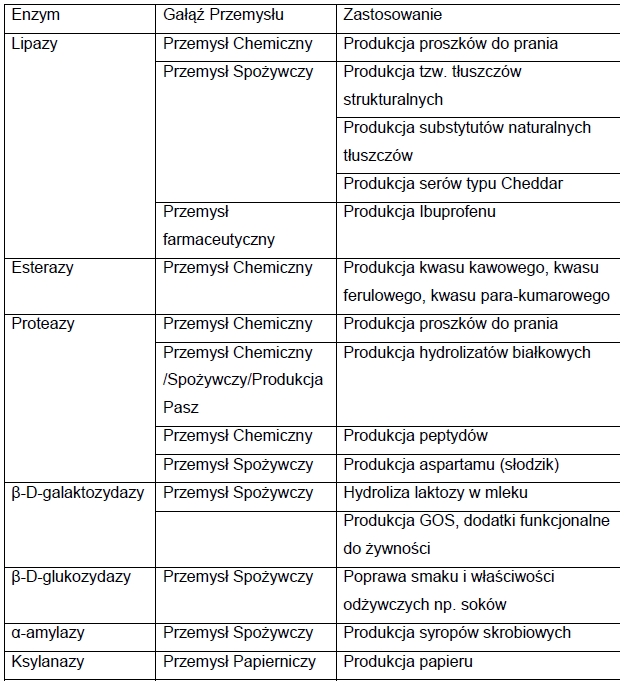
O powszechnym wykorzystaniu enzymów jako przemysłowe biokatalizatory decyduje m. in.: (a) wysoka sprawność katalityczna pozwalającą na używanie bardzo małych ilości enzymów do przerobu znacznie większej ilości substratu katalizowanej reakcji chemicznej, (b) wysoka specyficzność substratowa połączona ze zdolnością enzymów do syntezy związków chemicznych w postaci jednego z możliwych enancjomerów oraz (c) reakcje chemiczne katalizowane przez enzymy na ogół przebiegają w warunkach fizykochemicznych tj. temperatury, pH, ciśnienia, które można określić jako „łagodne” w porównaniu z warunkami prowadzenia wielu reakcji chemicznych z wykorzystaniem katalizatorów nieenzymatycznych.
Na dzień dzisiejszy źródłem większości komercyjnie dostępnych enzymów, wykorzystywanych w przemyśle, są organizmy mezofilne. Optymalna temperatura wzrostu i rozwoju tych organizmów mieści się w granicach od 30°C do 40°C. W praktyce oznacza to, że enzymy wyizolowane z organizmów mezofilnych wykazują maksymalną aktywność enzymatyczną w temperaturach mieszczących się w zakresie pomiędzy 45-55oC, natomiast w temperaturach poniżej 30oC ich sprawność katalityczna jest znacząco ograniczona. Efektem tej zależności jest zastosowanie enzymów mezofili w biotechnologiach gdzie temperatura procesów jednostkowych wykorzystujących enzymy wynosi od 30oC do 60oC. Oczywiście, enzymy te też mogą być stosowane do katalizowania reakcji chemicznych w niższych temperaturach, jednak wiąże się to z wydłużeniem procesu produkcyjnego, wzrostem kosztów procesu produkcji, a w przypadku biotechnologii przemysłu spożywczego zwiększeniem ryzyka zanieczyszczenia niepożądaną mikroflorą potencjalnie chorobotwórczą. Stąd w ostatniej dekadzie, nastąpił wzrost liczby projektów badawczych oceniających możliwość wykorzystania w przemyśle psychrozymów. Psychrozymy to enzymy wykazujące wysoką sprawność katalityczną w zakresie temperatur powyżej 10-15oC, a maksymalną aktywność enzymatyczną w zakresie temperatur pomiędzy 30oC a 40oC. Enzymy te są produkowane przez organizmy należące do grupy psychrofili i psychrotrofów, powszechnie występujących w glebach i wodzie regionów polarnych i wysokogórskich Ziemi oraz wodach mórz i oceanów. W zastosowaniu w przemyśle adaptowanych do zimna hydrolaz upatruje się następujących korzyści:
• wysoka aktywność enzymatyczna w stosunkowo niskich temperaturach (15-20oC) pozwala ograniczyć koszty procesu dzięki unikaniu potrzeby grzania bioreaktorów (energooszczędność),
• w niższej temperaturze spada szybkość reakcji chemicznych przebiegających bez udziału enzymu, prowadzących do niepożądanych produktów ubocznych (lepsze wykorzystanie substratu),
• niska temperatura pozwala na ograniczenie strat powstałych na skutek degradacji termolabilnych substratów i/lub produktów reakcji,
• psychrozymy na ogół ulegają szybkiej denaturacji termicznej po podniesieniu temperatury o 10oC powyżej temperatury zapewniającej maksymalną aktywność,
• enzymatyczną psychrozymu – pozwala to na kontrolowanie czasu trwania reakcji enzymatycznej,
• w przemyśle spożywczym dzięki stosowaniu psychrozymów obniżamy ryzyko rozwoju mezofilnej flory bakteryjnej (patogennej lub mogącej zepsuć właściwości organoleptyczne produktu), której źródłem np. mogą być pracownicy zatrudnieni przy produkcji.
Na dzień dzisiejszy, adaptowane do zimna lipazy i proteazy są powszechnie stosowane jako dodatek enzymatyczny w proszkach do prania i w środkach do czyszczenia powierzchni. Proszki do prania z zastosowaniem psychrozymów pozwalają na efektywne usuwanie zanieczyszczeń w niskiej temperaturze, co ogranicza zużycie energii (grzanie wody) oraz ogranicza tempo zużycia włókien materiałów stosowanych do produkcji odzieży. Prowadzi się także badania nad możliwością zastosowania innych psychrozymów w przemyśle. Szczególnie dużo projektów badawczych skupia się nad zastosowaniem adaptowanych do zimna β-D-galaktozydaz do usuwania laktozy z mleka. Obecna w mleku i niektórych produktach jego przetwarzania laktoza jest częstą przyczyną „alergii” pokarmowej u spożywających ją osób dorosłych, wywołanych utratą przez komórki jelita cienkiego zdolności do produkcji endogennej β-D-galaktozydazy. Obecnie do usuwania laktozy z mleka na etapie jego przechowywania i transportu w chłodniach stosuje się mezofilną β-D-galaktozydazę drożdży Kluyveromyces lactis. Zastosowaniem w tym samym celu enzymu adaptowanego do zimna pozwoli na ograniczenie czasu trwania procesu hydrolizy w warunkach chłodniczych oraz zmniejszy ryzyko kontaminacji niepożądaną mezofilną florą bakteryjną. Intensywne badania mające na celu znalezienie odpowiedniego do tego celu psychrozymu były jak dotąd prowadzone m.in. w USA, Japonii, Belgii, Chinach, a także w Polsce w Instytucie Biochemii Technicznej Politechniki Łódzkiej i w Katedrze Mikrobiologii Politechniki Gdańskiej gdzie do dnia dzisiejszego wyizolowano i scharakteryzowano przydatność adaptowanych do zimna β-D-galaktozydaz wyizolowanych z bakterii z rodzaju Pseudoalteromonas sp. oraz Arthrobacter sp. Wyniki uzyskane przez różne ośrodki naukowe wskazują na znaczne różnice we właściwościach enzymatycznych β-D-galaktozydaz izolowanych z różnych gatunków psychrofili i psychrotrofów. Niestety, żaden z tych psychrozymów nie spełnia wszystkich wymogów stawianych przed idealnym biokatalizatorem przydatnym do zastosowania w przemysłowym procesie usuwania laktozy z mleka. Najczęściej występujące problemy to inhibicja enzymu jonami Ca2+ lub produktami hydrolizy laktozy (D-glukoza i D-galaktoza), albo zbyt niska wydajność produkcji enzymu w komórkach natywnego gospodarza, co czyni produkcję psychrozymu nieopłacalną na dużą skalę wymaganą dla zaspokojenia potrzeb przemysłu. Rozwiązania napotkanych problemów upatruje się w zastosowaniu metody „ewolucji in vitro” oraz doborze właściwego organizmu gospodarza pozwalającego na wydajną produkcję rekombinantowej wersji psychrozymu. Obiecującym gospodarzem dla wydajnej produkcji rekombinowanych β-D-galaktozydaz są drożdże gatunku Pichia pastoris, co potwierdzają wyniki uzyskane dla rekombinowanej adaptowanej do zimna β-D-galaktozydazy Artrobacter sp. 32 c. Wspomniana powyżej, metoda „ewolucji in vitro” pozwala na modyfikacje sekwencji genów znanych psychrozymów. Następnie na drodze racjonalnej selekcji możliwe jest wybranie biokatalizatora spełniającego wymagania stawiane przez biotechnologię hydrolizy laktozy w mleku. Warto zaznaczyć, że dzięki zastosowaniu tej metody uzyskano adaptowane do zimna hydrolazy odporne na denaturujące działanie detergentów obecnych w proszkach. Uważa się, że to rozwiązanie w niedalekiej przyszłości zaowocuje stworzeniem konkurencyjnego do obecnie stosowanego w przemyśle mezofilnego enzymu, β-D-galaktozydazy Kluyveromyces lactis. Podsumowując, psychrozymy stanowią grupę enzymów będących nowym i ważnym źródłem unikalnych biokatalizatorów. Dlatego też, poszerzanie wiedzy na temat tej grupy biokatalizatorów jest istotne dla dalszego rozwoju współczesnej biotechnologii.





