Wojciech Kamysz
Laboratorium Syntezy Peptydów, Lipopharm.pl
strony wersji drukowanej: 36-39
strony wersji drukowanej: 36-39
Otrzymywanie peptydów jest drogie z definicji. Zużywa się litry rozpuszczalników organicznych, a otrzymuje się zaledwie kilka miligramów czystego peptydu. Nie jest to ani ekonomiczne, ani zbyt przyjazne dla środowiska naturalnego. Czy istnieje możliwość bardziej proekologicznej metody pozyskiwania tej grupy związków?
Peptydy należą do substancji o bardzo dużej aktywności biologicznej. Zwykle do wywołania spodziewanego efektu leczniczego wystarczą ilości miligramowe a w zastosowaniach diagnostycznych nawet mikrogramowe. Powoduje to, że przemysłowe otrzymywanie tych substancji równoważne jest ze stosowaniem skali gramowej, maksymalnie kilogramowej w skali świata.
Chemiczna synteza peptydów z powodzeniem udaje się naukowcom od ponad stu lat. Pierwsze polimery złożone z 3 reszt glicyny (Gly-Gly-Gly) otrzymał już w roku 1902 Emil Fisher. Od tego czasu z różnym powodzeniem otrzymuje się peptydy trzema niezależnymi sposobami. Jest to izolacja ze źródeł naturalnych, jako pierwszy etap otrzymania biologicznie aktywnego związku chemicznego. Typowa synteza chemiczna oraz metody biologiczne, stosujące techniki inżynierii genetycznej to jednak jedne z najprężniej rozwijających się sposobów pozyskiwania peptydów. W związkach peptydowych postrzega się kandydatów na leki dla szerokiego wachlarza schorzeń. Do chwili obecnej największy sukces zdobyły leki hormonalne. W trakcie badań klinicznych jest jednak kilkadziesiąt nowych molekuł o znaczeniu aplikacyjnym.
Metody otrzymywania peptydów
Izolacja ze źródeł naturalnych, synteza chemiczna (synteza w roztworze, synteza na nośniku stałym) oraz synteza enzymatyczna to trzy główne sposoby pozyskiwania peptydów.
Trwająca już ponad pół wieku era sukcesów, ale i pasmo niespełnionych oczekiwań, otworzyło syntetyczne otrzymanie oksytocyny i wazopresyny przez Vincent du Vigneaud’a w roku 1954. Dzięki temu wzrosło ogromnie zainteresowanie chemią peptydów. Krokiem milowym okazały się jednak próby kotwiczenia pierwszych aminokwasów na stałym nośniku. W roku 1955 Nicholls z powodzeniem otrzymał kilka pochodnych dipeptydów przyłączając N-chronione aminokwasy do aminokwasów zakotwiczonych na wymieniaczu jonowym Dowex. Rozwinięciem tego podejścia było kotwiczenie pierwszego aminokwasu w sposób kowalencyjny. Kluczowym osiągnięciem okazał się sposób Merrifileda, polegający przyłączeniu C-terminalnego aminokwasu do nierozpuszczalnego nośnika. Metoda ta, zwana później od nazwiska twórcy, metodą Merrifielda została uznana po dwudziestu latach od opracowania na tyle ważna, iż twórca jej otrzymał w roku 1984 nagrodę Nobla. Właśnie metodą syntezy na nośniku stałym otrzymuje się współcześnie peptydy w laboratoriach naukowych, ale i coraz chętniej w procesach typowo przemysłowych. Idea przyłączenia jednego z substratów do nierozpuszczalnego nośnika została zaadoptowana powszechnie przez laboratoria syntetyczne i jest coraz częściej postrzegana jako jedna z najbardziej proekologicznych metod syntezy. Synteza na nośniku pozwala na miniaturyzacje syntezy, czy stosowanie nadmiarów reagentów (jeśli trzeba). Nie bez znaczenia jest też możliwość ograniczenia do minimum kontaktu z odczynnikami. Najbardziej toksyczne związki można w sposób bezpieczny podawać np. mikropipetą lub zastosować automatyczne syntezatory peptydów. Urządzenia te, choć stosunkowo drogie, zapewniają jednak bezpieczeństwo oraz powtarzalność wyników w przypadku syntez cyklicznych.
Najważniejszą zaletą jest jednak uniknięcie etapów pośrednich, zwykle przeprowadzanych z użyciem ekstrakcji ciecz-ciecz. Podczas syntezy na nośniku nieprzereagowane reagenty oraz produkty uboczne usuwa się podczas zwykłego sączenia z użyciem naczyń ze spiekiem szklanym bez niepotrzebnej izolacji produktów pośrednich. Stopień acylowania bada się kolorymetrycznie z użyciem dostępnych testów na obecność wolnych grup aminowych. W przypadku testu pozytywnego reakcję prowadzi się dalej, w przypadku reakcji negatywnej przechodzi się do następnego etapu.
W ostatnich latach na syntezę na nośniku przeszedł też przemysł. Pomimo, że jest to proces odczynnikowo droższy niż synteza w roztworze, to daje wymierne efekty w zmniejszeniu kosztów pracy.
Synteza peptydów na nośniku stałym
Syntetyczne otrzymywanie peptydów jest zwykle trudne dla niewprawionych chemików. Problemy pojawiają się zarówno na etapie syntezy, odczepienia od nośnika, ale przede wszystkim podczas oczyszczania surowych produktów. Sama synteza polega na chemicznym przyłączeniu pierwszego aminokwasu do nie-rozpuszczalnego polimeru oraz cyklicznym przyłączaniu kolejnych elementów (tj. aminokwasów) i każdorazowej deprotekcji grupy ochronnej blokującej budowany łańcuch peptydowy. Wszystkie reakcje związane z przyłączaniem kolejnych pochodnych aminokwasowych, deprotekcji osłon ochronnych grupy N-α-aminowych oraz finalnej deprotekcji prowadzi się w środowisku rozpuszczalników organicznych. W trakcie acylowania oraz przemywań stosuje się przeważnie dichlorometan oraz dimetyloformamid. Podczas odszczepiania peptydu od nośnika wraz z odczepieniem osłon łańcuchów bocznych wykorzystuje się rożne stężenia kwasu trifluorooctowego, często w obecności tioli. Wszystkie wspomniane rozpuszczalniki stanowią duże zagrożenia dla środowiska naturalnego i należy je utylizować w wyspecjalizowanych firmach, a związki lotne absorbować na właściwych pochłaniaczach. Wysokie ceny unieszkodliwiania odpadów postsyntetycznych są związane głównie z obecnością rozpuszczalników chlorowcopochodnych. Około 1/10 kosztów używanych do syntezy odczynników to właśnie utylizacja.
Alternatywą dla tych problemów jest możliwość syntezy w roztworach wodnych, a pierwsze doniesienia na ten temat pojawiły się już ponad 10 lat temu. Na chwilę obecną pozostaje racjonalna gospodarka odczynnikami oraz próba optymalizacji każdego z procesów wchodzących w skład całej, często kilkudziesięcioetapowej syntezy.
Zmniejszenie nakładu energii związanej z mieszaniem żywicy (nośnika) i mieszaniny reakcyjnej, ale i potrzebnego czasu można zmniejszyć poprzez wykorzystanie wynalazku ostatnich lat jakim są nowoczesne syntezatory. Dużym udogodnieniem jest bowiem prowadzenie etapów acylowania w reaktorach mikrofalowych. Dzięki wykorzystaniu promieniowania mikrofalowego można przyspieszyć reakcje nawet dziesięciokrotnie.
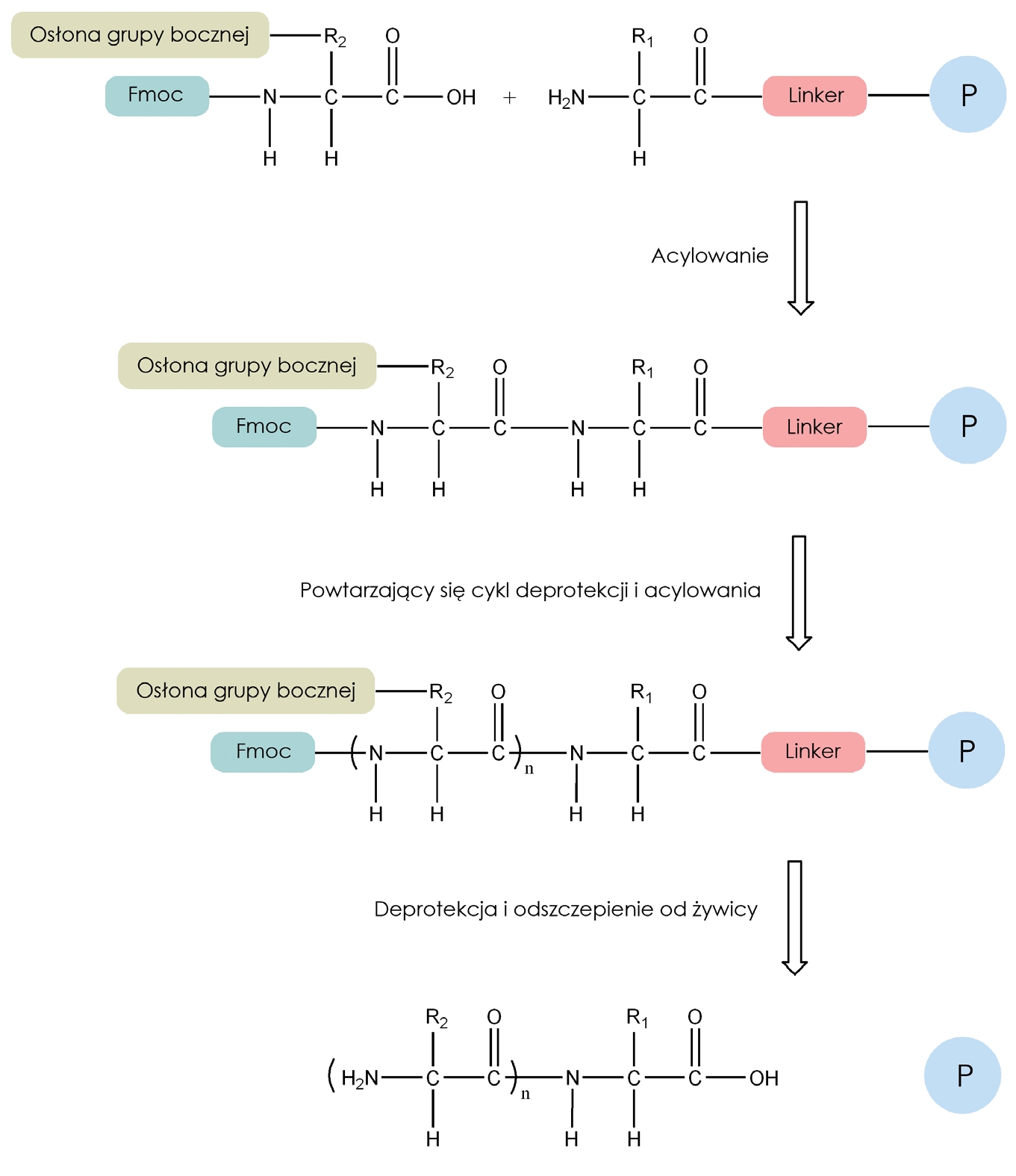
Rys. 2. Schemat syntezy peptydów na stałym nośniku polimerowym (P – polimer/nośnik, R1, R2 – łańcuchy boczne aminokwasów, Fmoc – osłona grupy α-aminowej aminokwasów).
Oczyszczanie peptydów
Otrzymanie peptydów w postaci oczyszczonej jest procesem często bardzo trudnym. Zanieczyszczenia wchodzące w skład próbki to często bardzo podobne związki chemiczne. Dlatego wyodrębnienie czystego produktu pochłania więcej czasu i funduszy niż sama synteza. Obecnie najpopularniejszą metodą oczyszczania peptydów jest wysokosprawna chromatografia cieczowa w układzie faz odwróconych (RP-HPLC). Jako fazę stacjonarna stosuje się kolumny wypełnione krzemionką modyfikowana łańcuchami alkilowymi (C8 lub C18). Jako eluent podaje się wodę oraz acetonitryl z dodatkiem 0,1% kwasu trifluorooctowego. Proces oczyszczania prowadzi się gradientowo stopniowo zwiększając udział acetonitrylu w fazie ruchomej. W skali laboratoryjnej, z wykorzystaniem typowego sprzętu analitycznego (HPLC z przepływem do 10ml/min), ale kolumną semipreparatywną można z powodzeniem oczyszczać jednorazowo ilości nawet do 200-500mg substancji. Odpowiednie frakcje analizuje się, a następnie po odparowaniu acetonitrylu suszy sublimacyjnie z użyciem liofilizatora. Zarówno zlewki po oczyszczaniu jak i odparowywaniu frakcji z acetonitrylu powinny być utylizowane (kiedyś były powszechnie wylewane do kanalizacji!). Otrzymywanie peptydów w przemyśle niewiele różni się od skali laboratoryjnej. Stosuje się większe średnice kolumn (a więc i większe przepływy), a acetonitryl zastępuje się etanolem lub izopropanolem. Należy tutaj wspomnieć, że roczne potrzeby niektórych peptydów (np. oktreotydu, despopresyny) w skali świata wynoszą zaledwie 50-200kg.
Analiza peptydów
Peptydy zarówno w laboratoriach naukowych jak i przemysłowych analizuje się ten sam sposób. Czystość próbki określa się chromatograficznie, tożsamość potwierdza z użyciem spektrometrii mas. W analityce dominuje chromatografia cieczowa RP-HPLC w układzie gradientowym woda-acetonitryl z detekcją UV, zwykle przy długości fali 214 lub 220m. Stosowanie wypełnień kolumn o klasycznej średnicy porów uziarnienia (100A) w zupełności wystarcza aby analizować nawet małe białka (do 5-6kDa). Często w trudnych przypadkach wykorzystuje się też detektor masowy, który daje informacje o zawartych zanieczyszczeniach oraz jednocześnie potwierdza masę cząsteczkowa kluczowego składnika.
W latach 90-tych próbowano wykorzystywać elektroforezę kapilarną (CE), jednak bez większych sukcesów. Obecnie CE, podobnie jak chromatografię jonową stosuje się do oznaczania przeciwjonów w peptydach.
Duże zasługi w określaniu struktury przestrzennej większych polipeptydów wnosi dwuwymiarowy rezonans magnetyczny (NMR) oraz badania dichroizmu kołowego (CD). W praktyce przemysłowej jednak te analizy dotyczą peptydów zawierających więcej niż 20-30 reszt i nie są wymagane obligatoryjnie.
Przemysłowe podejście w syntezie
Zgodnie z powszechnie panującym trendem dotyczącym proekologii, przemysł daje wiele rozwiązań jak syntezować ekologicznie a zarazem skutecznie.
Osadzenie na stosowanych nośnikach powinno być maksymalne, w przypadku oligopeptydów nawet 3mmol/g. Same nośniki powinny być odzyskiwane, co możliwe jest w przypadku nośnika 2-chlorotritylowego. Zużycie rozpuszczalników chlorowcopochodnych ogranicza się do minimum.
Wszelkie etapy syntezy powinny być zoptymalizowane, a pod uwagę powinny być tez brane takie czynniki jak zużycie energii elektrycznej oraz pracochłonność etapów (gdyż pracownik też kosztuje). W oczyszczaniu jako eluent powinno stosować się etanol, co pozostaje też w zgodzie z wytycznymi Amerykańskiej Agencji ds. Żywności i Leków (FDA). Niestety stosowanie tego eluentu nie pozostaje bez wpływu na wzrost ciśnień podczas rozdziałów. Dużą rolę w oczyszczaniu przemysłowym odgrywa bardzo tania chromatografia jonowymienna oraz chromatografia metalopowinowactwa. Umożliwia ona ograniczenie do minimum zastosowania rozpuszczalników organicznych, a ilości oczyszczane jednorazowo na kolumnie są nawet 2-5 krotnie większe niż na kolumnie HPLC. Sama elucja z kolumny następuje w gradiencie soli nieorganicznej lub gradiencie pH.
Wielu ekspertów do niedawna skłaniało się ku poszukiwaniu metod biologicznych wykorzystujących zdobyte osiągnięcia inżynierii genetycznej. Pozyskiwanie peptydów niesie jednak za sobą duże niebezpieczeństwa dla produktów farmaceutycznych, gdyż otrzymywane substancje zwykle zawierają ślady fragmentów drobnoustrojów, w których następowała nadekspresja, co wiąże się z opowiedzą układu odpornościowego w trakcie stosowania takich leków. W obecności zawartych też proteaz dodatkowo obniża się trwałość preparatów peptydowych. Jedyne co może zostać po syntezie chemicznej i klasycznym oczyszczaniu to ślady rozpuszczalników oraz eluentów, które w sposób bardzo prosty można kontrolować chromatografią gazową.





