Wojciech Kamysz
Laboratorium Badawczo-Rozwojowe, Lipopharm.pl
strony wersji drukowanej: 29-36
strony wersji drukowanej: 29-36

Chemiczna synteza na nośniku stałym, zwana też powszechnie syntezą na fazie stałej ma ponad 50 lat. Pomimo dojrzałości idei znajduje jednak ciągle nowe zastosowania. Pierwotnie stworzona w celu syntezy peptydów oraz kwasów nukleinowych do dziś dnia stanowi doskonałe narzędzie znajdujące zastosowanie w wielu laboratoriach naukowych oraz przemysłowych. Metoda opracowana pierwotnie przez Bruce’a Merrifield’a w 1963 roku została doceniona Nagrodą Nobla w dziedzinie chemii co udowadnia wagę tego opracowania. Należy jednak zauważyć, że wiązanie reagentów z nośnikiem było znane 8 lat wcześniej. Nicholls opisał bowiem metodę z wykorzystaniem wymieniacza jonowego. Nowość podejścia Merrifield’a polegała jednak na wiązaniu kowalencyjnym substratów do złoża.
Olbrzymi rozwój tego podejścia nastąpił jednak w latach osiemdziesiątych wraz zastosowaniem nośników do otrzymywania związków niskocząsteczkowych oraz wprowadzeniem do użycia nowych linkerów, czyli ugrupowań chemicznych pozwalających na selektywne przyłączenie do nośnika określonych struktur chemicznych.
Do niewątpliwych zalet syntezy w fazie stałej należą szybkość procesów chemicznych, co związane jest z możliwością stosowania nadmiarów i łatwość ich odmywania od złoża po danych etapach oraz brak potrzeby izolowania produktów pośrednich ogranicza pracochłonność, a tym samym skraca cykl produkcji, co jest szczególnie ważne w przemyśle. Synteza w fazie stałej umożliwia też automatyzację, również w trakcie izolacji i oczyszczania produktów reakcji. Koszt nośników stosowanych w tych procesach często jest w końcowym bilansie niższy aniżeli wartość wszystkich pracochłonnych etapów w syntezie w roztworze.
Idea syntezy w fazie stałej
Synteza na nośnikach stałych rozwija się od ponad pół wieku, głównie dzięki powszechnemu stosowaniu tej metody w syntezie peptydów (więcej w artykułach „Pół wieku syntezy peptydów, Laborant 2/2010 oraz „Proekologia w peptydach” Laborant 3/2011). Polega ona na zastosowaniu nierozpuszczalnego nośnika (zwykle w postaci polimerowych ziaren), na którym za pomocą linkera umieszcza się pierwszy element budowanego związku. Nośnik po zadaniu odpowiednim rozpuszczalnikiem umieszcza się w specjalnym naczyniu, posiadającym filtr zapobiegający przed opuszczaniem ziaren podczas przemywania. Przykłady naczyń do syntezy przedstawia rys. 1.

Rys. 1. Typowe naczynia do syntezy na nośniku stałym (www.tech-lab.pl).
Drugi reagent lub mieszaninę reagentów dodaje się w postaci roztworu. Po zakończonej reakcji nośnik filtruje się oraz przemywa rozpuszczalnikami usuwając w ten sposób nadmiar użytych reagentów. Nie izolując produktu pośredniego nośnik można poddać działaniu kolejnego odczynnika, uzyskując w ten sposób kolejne struktury bez potrzeby uwalniania produktów pośrednich. Pozwala to na ominięcie procesów krystalizacji czy ekstrakcji jaka jest wymagana w syntezie w fazie ciekłej. Synteza na nośniku stałym umożliwia również stosowanie dużych nadmiarów dodawanych reagentów, co w znaczący sposób przyspiesza przebieg reakcji. Nadmiary te w trakcie odsączania są usuwane. Miniaturyzacja skali syntezy z kolei umożliwia automatyzację procesu oraz uniknięcie kontaktu z często toksycznymi substancjami chemicznymi stosowanymi podczas syntez organicznych.
Rodzaje nośników i linkerów
Wybór odpowiedniego nośnika podyktowany jest w głównej mierze warunkami późniejszych reakcji. Z założenia nośnik powinien być bierny chemicznie (z wyjątkiem linkera), posiadać odpowiedni linker zdolny do przyłączenia pierwszego reagenta, być odpornym mechanicznie, a także dobrze pęcznieć w stosowanych rozpuszczalnikach. Pęcznienie nośnika stałego jest bardzo ważne ze względu na to, że syntezowany związek o masie często nawet kilku kilodaltonów stanowi ponad połowę masy stosowanego złoża. Zwykle używa się nośników o uziarnieniu 50-400 mesh oraz maksymalnym osadzeniu 0,5-1,5 mmol/g nośnika.
Na przełomie lat próbowano syntezować związki chemiczne na prętach polietylenowych (metoda Geysena, 1984 r.), krążkach celulozowych SPOT (metoda Franka), szkle (metoda Fodora) czy zwykłej krzemionce. Ostatnio duże nadzieje wiąże się z immobilizacją związków na kulkach magnetycznych czy powierzchni złota.
Jednak to stosunkowo tanie złoże polistyrenowe sieciowane diwinylobenzenem cały czas stanowi prawie ¾ wszystkich nośników stosowanych w różnych aplikacjach laboratoryjnych. Rzadziej stosuje się nośniki (żywice) na bazie polietylenoglikoli (PEG) czy poliakryloamidu (PA). Na rynku dominują głównie trzy nośniki: żywica Wanga (przykład użycia na rys. 1), żywica Rink amide oraz nośnik z linkerem 2-chlorotritylowym (żywica Barlosa).
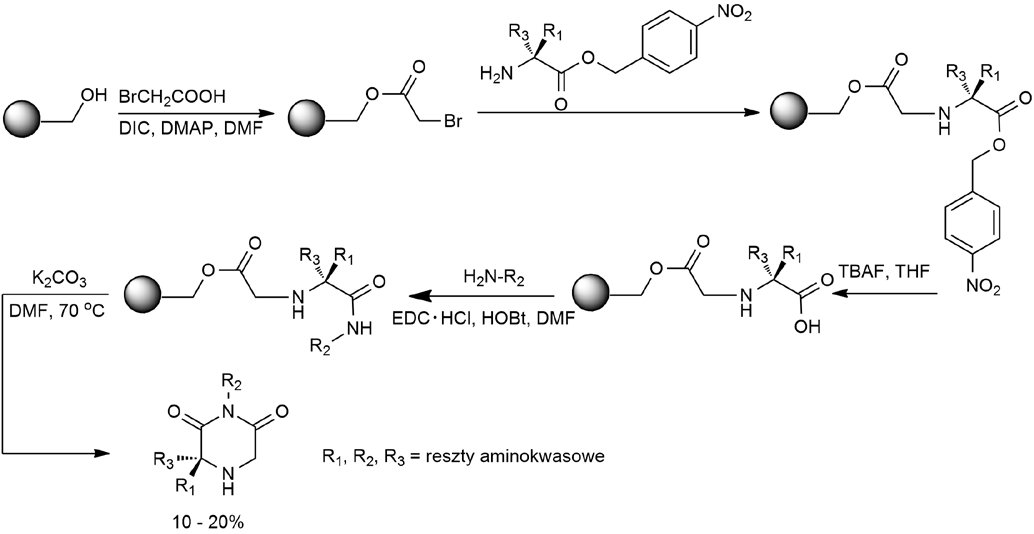
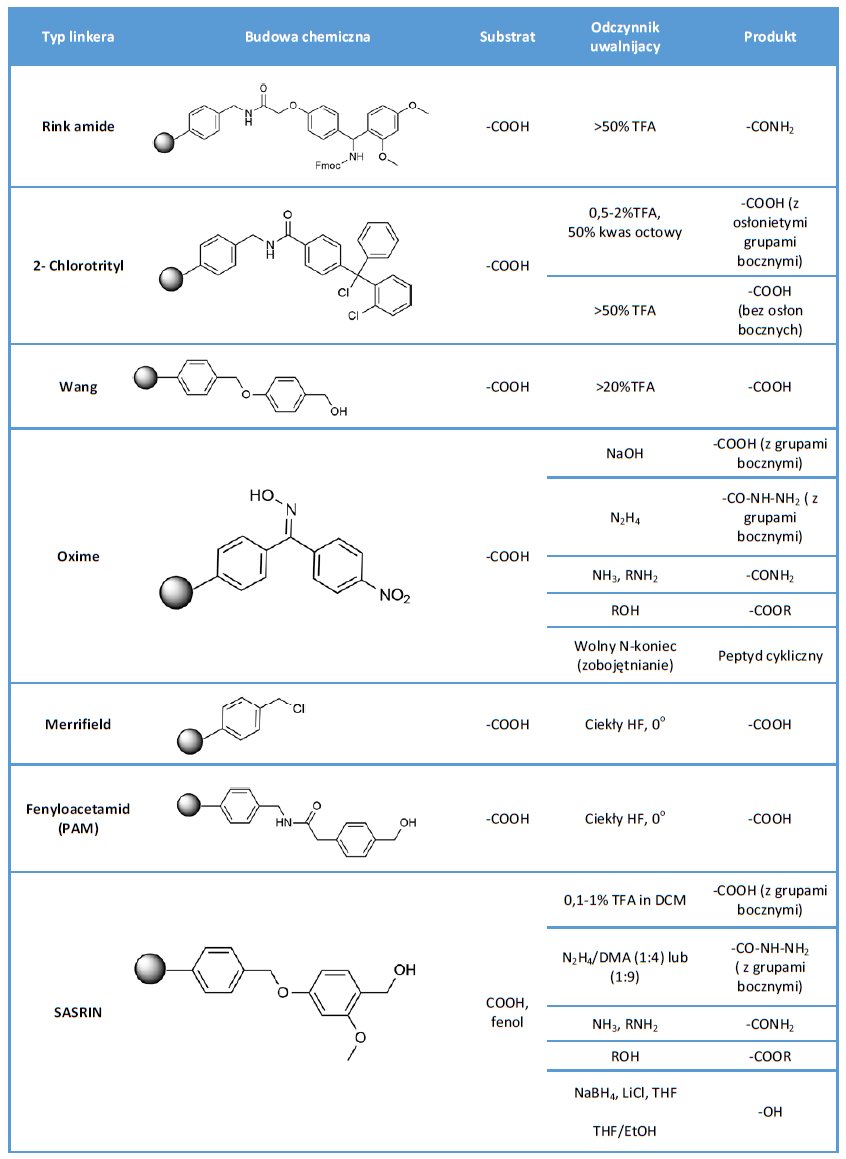
Tabela 1. Rodzaje linkerów uwalnianych w środowisku kwaśnym.

Rys 2. Synteza 1,3 podstawionej pochodnej diketopiperazyny z użyciem żywicy Wanga (Perotta E. i wsp, J Comp Chem, 2001).
Tabela 1. Rodzaje linkerów uwalnianych w środowisku kwaśnym.

Zakotwiczone reagenty
Dużym powodzeniem cieszy się również synteza w roztworze wykorzystująca nośniki z reaktywnymi grupami funkcyjnymi. Cały proces syntezy w tym przypadku odbywa się w roztworze. Metoda ta jest wykorzystywana przy odczynnikach stosowanych zwykle w małych ilościach. Należą do nich głównie katalizatory reakcji. Do innych, rzadszych zastosowań należą środki kondensujące, czynniki utleniające. Przykłady takich produktów przedstawia rysunek 2.
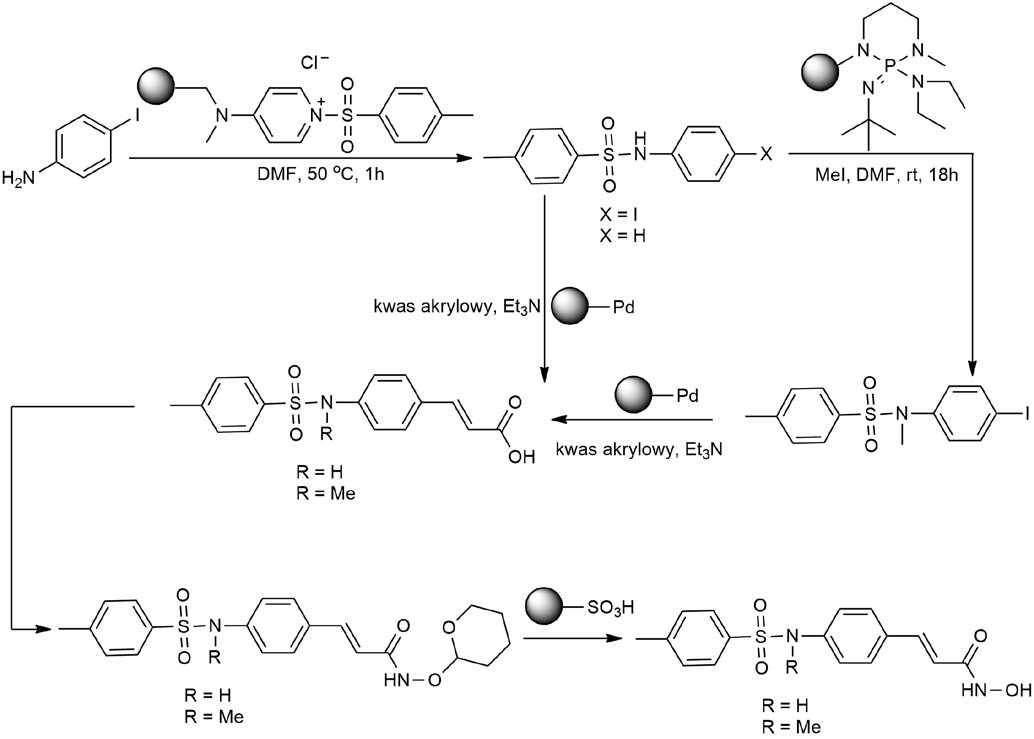
Rys. 3. Przykład wykorzystania nośników w syntezie w fazie ciekłej, syntezie inhibitorów deacetylazy histonów, (A. Bapna i wsp, Org. Biomol. Chem., 2004).

Rys. 3. Przykład wykorzystania nośników w syntezie w fazie ciekłej, syntezie inhibitorów deacetylazy histonów, (A. Bapna i wsp, Org. Biomol. Chem., 2004).
Zaletą syntezy w roztworze z użyciem reagentów na złożach jest możliwość analizy postępu reakcji w czasie rzeczywistym bez potrzeby odszczepiania produktu lub półproduktu od nośnika. Stosowane reagenty usuwa się przez filtrację.
Nośniki-skawendżery
Nośniki z przyłączonymi skawendżerami stanowią obecnie jedno z ważniejszych narzędzi dla syntezy chemicznej w roztworze. Umożliwiają one bezproblemowe (zwykła filtracja) usuwanie określonych związków chemicznych z mieszanin poreakcyjnych, przez co synteza może przebiegać z nadmiarze jednego z reagentów. Ponieważ reakcje przebiegają w roztworze, późniejsze skalowanie wszystkich procesów nie jest tak kłopotliwe jak dla syntezy przeprowadzanej w fazie stałej. Drugą olbrzymią zaletą jest możliwość zastosowania w toku reakcji różnych nośników, usuwających tylko określone półprodukty bądź substraty. Przykłady zastosowań takich nośników oraz struktur chemicznych ich linkerów przedstawia tabela 2.
Nośniki-skwawendżery stosowane są już powszechnie od lat 90-tych. Jonity zawarte w systemach oczyszczania wody, to właśnie złoża o takich właściwościach.
Tabela 2. Przykłady nośników-skawendżerów.
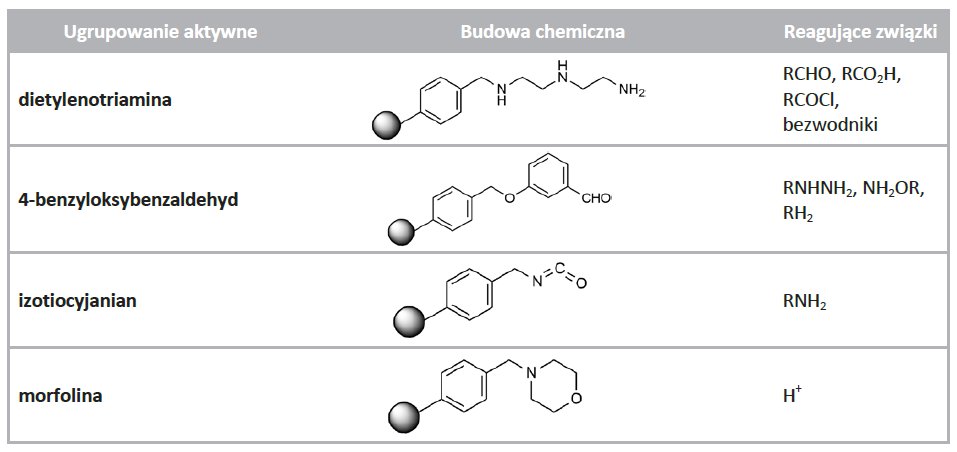
Tabela 2. Przykłady nośników-skawendżerów.

Chemia równoległa i kombinatoryczna
Synteza równoległa na nośniku może być prowadzona na wiele sposobów. Zwykle nośniki są umieszczone w osobnych naczyniach połączonych wspólnym kanałem służącym do pozbywania się nadmiaru reagentów, bądź rozpuszczalników stosowanych do przemywań. W tej konwencji jest opracowany tzw. Domino Block. Zbudowany jest on z szeregu połączonych ze sobą rezerwuarów (strzykawek z filtrem) umieszczonych na miniplatformie stanowiącej wspólne ujście roztworów upuszczających te naczynia.
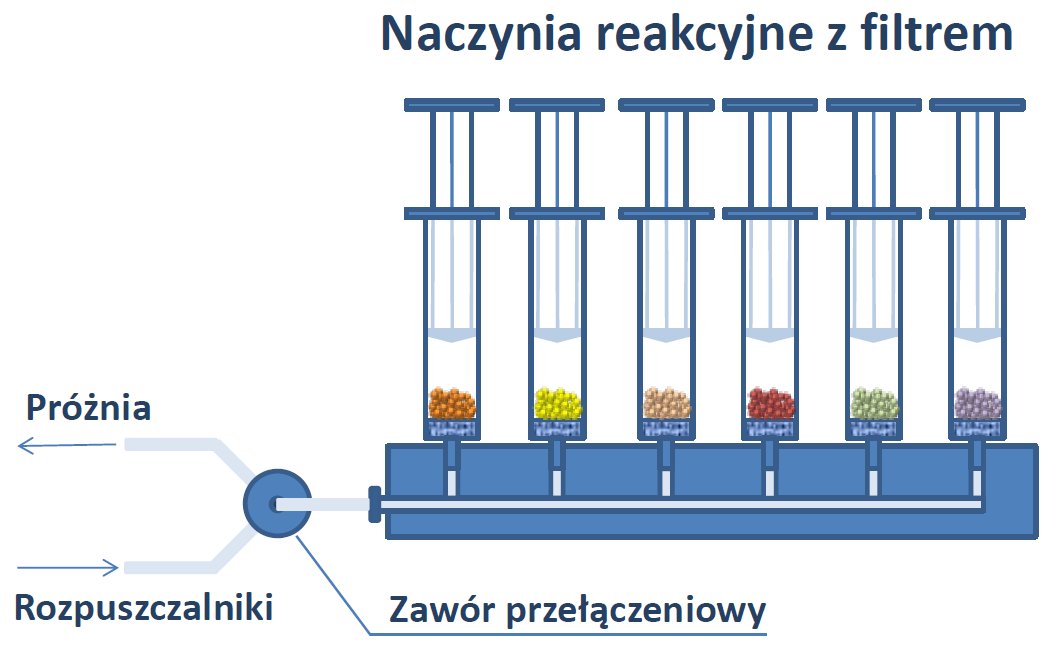
Rys 4. Schemat bloku Domino wraz z naczyniami do syntezy.
Jednym z ciekawych podejść jest metoda opisana przez Houghtena polegająca na umieszczeniu nośnika w woreczkach z perforowanego polipropylenu. Woreczki takie można wykonać samodzielnie z użyciem zgrzewarki do folii.
Zastosowanie woreczków z nośnikiem pozwala na jednoczesne poddawanie pewnym procesom dużej ilości nośników. Określone procesy w takim podejściu można wykonywać w jednym naczyniu (np. deprotekcję osłon, czy przemywanie nośników). Metoda ta jest szczególnie użyteczna w przypadku, gdy otrzymuje się analogi modyfikowane w określonej pozycji. Zapewnia to ciągłą kontrolę, gdzie (w którym woreczku) znajduje się określony związek chemiczny.
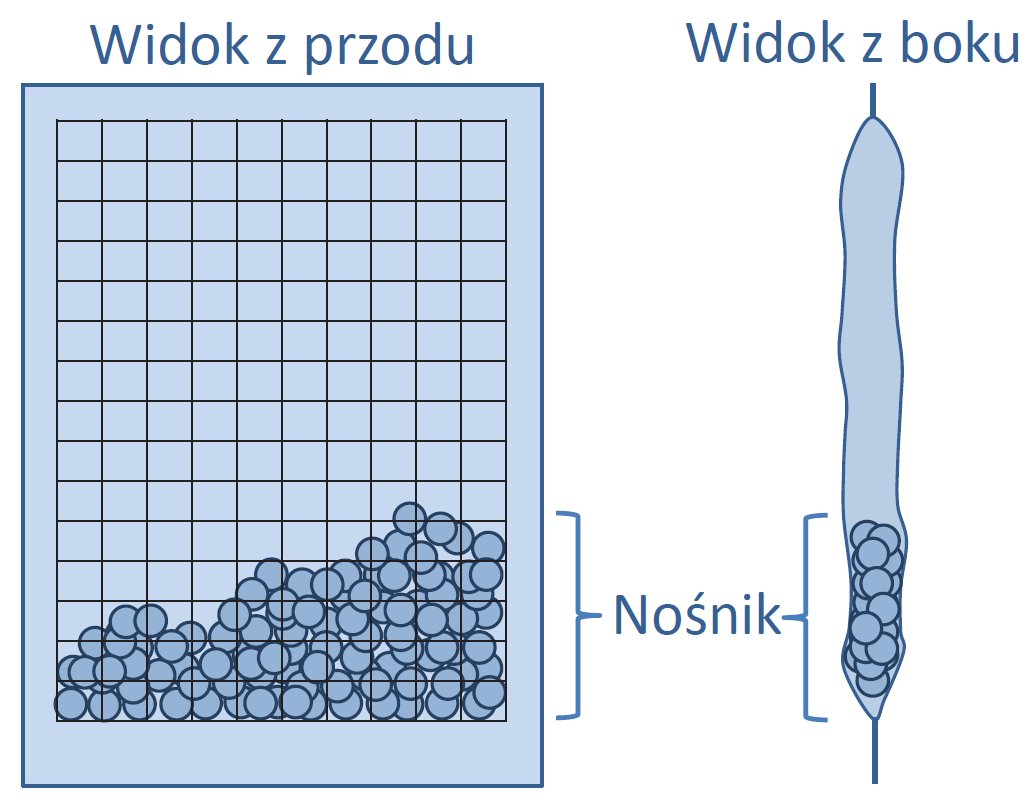

Rys. 5a. Woreczek polipropylenowy z nośnikiem (Tea-bag).

Rys. 5b. Schemat sposobu postępowania podczas syntezy peptydów w technice tzw. torebek herbacianych (Tea-bag).
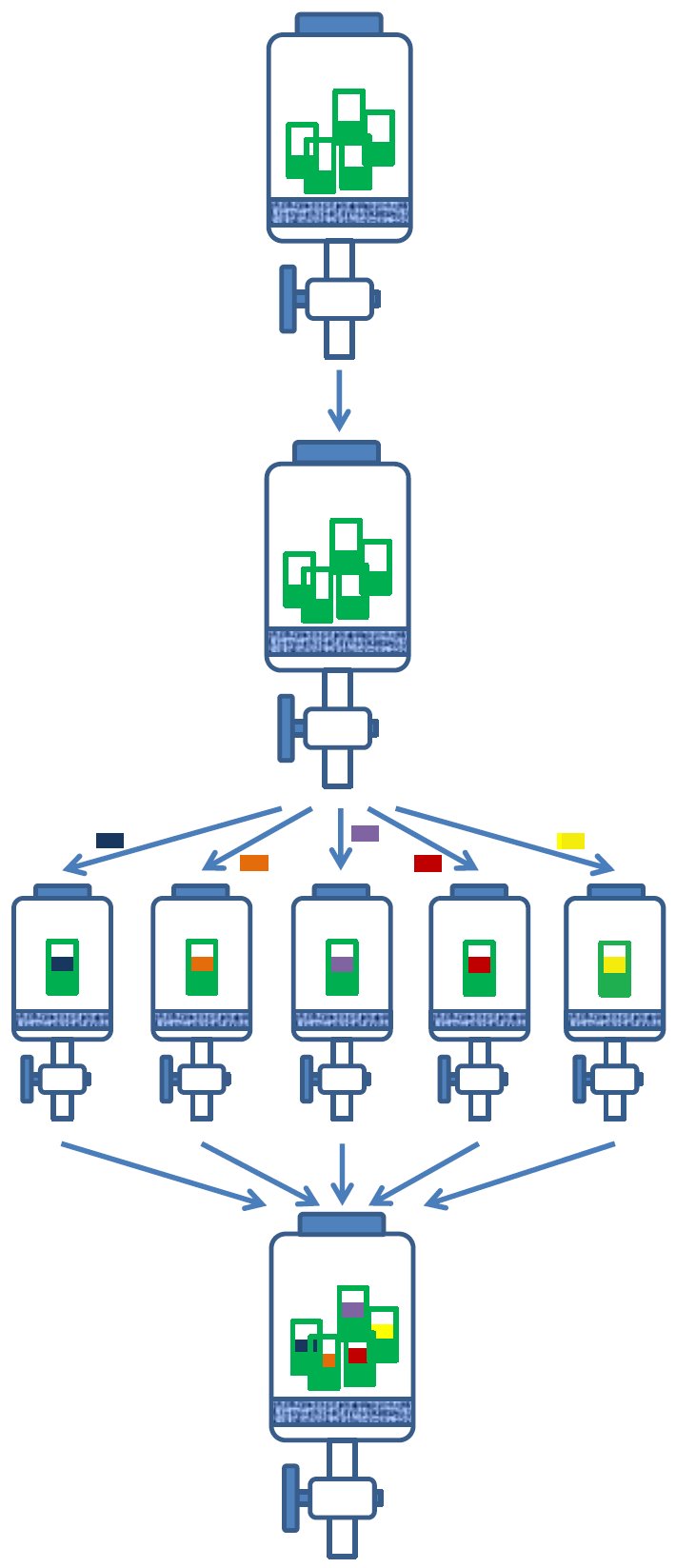
Krokiem milowym w wykorzystaniu nośników stałych było zaprezentowanie w 1988 roku przez Arpada Furke metody mieszaj-dziel stanowiącej podwaliny nowoczesnej chemii kombinatorycznej. Sposób podejścia naukowca polegał na naprzemiennym poddawaniu nośników acylowaniu aminokwasami, mieszaniu ich w jednym naczyniu oraz ponownym dzieleniu. Ideę pomysłu przedstawia rysunek 6.
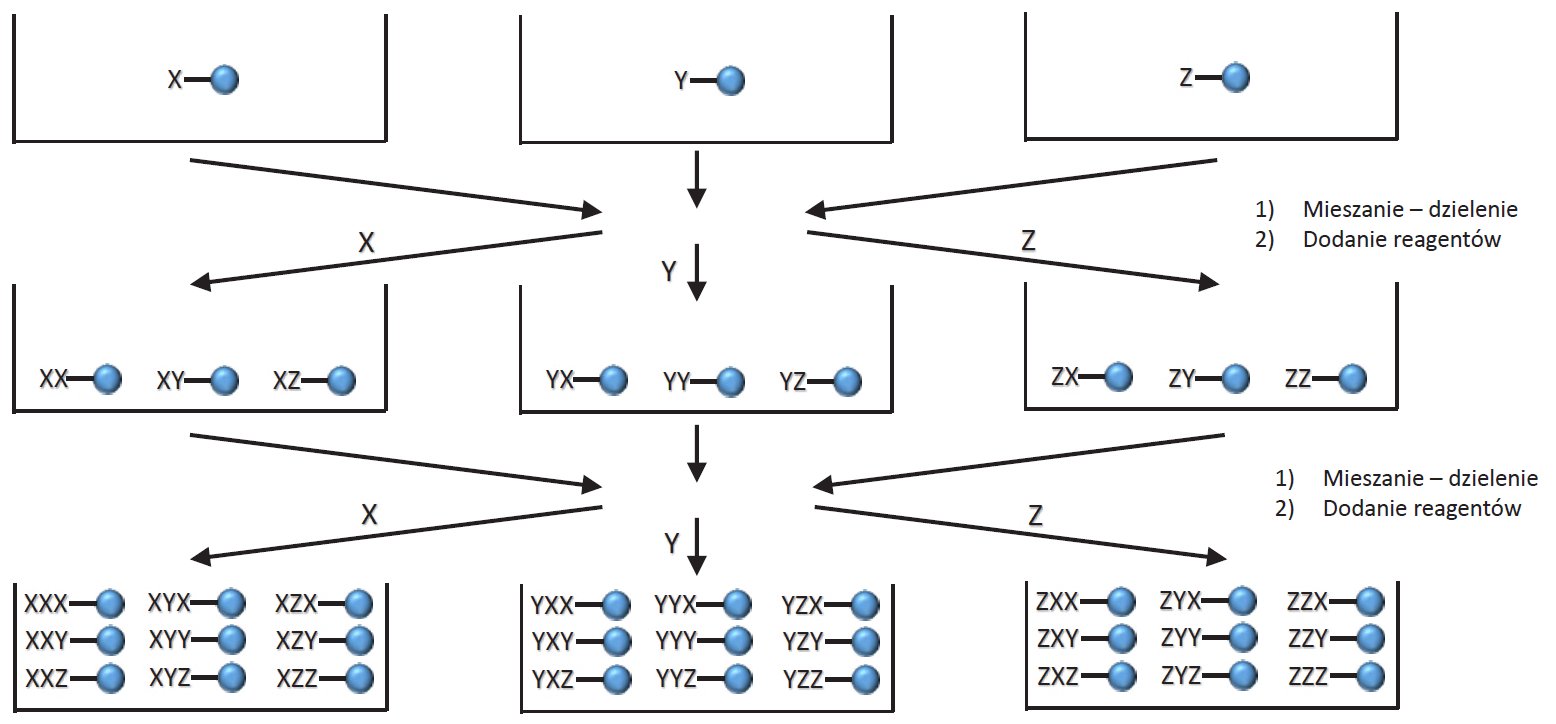
Rys 6. Schemat postępowania w metodzie mieszaj-dziel.
W wyniku tego otrzymuje się tzw. biblioteki związków chemicznych. W przypadku wykorzystania wszystkich możliwości łączenia 20 białkowych aminokwasów można otrzymać np. 400 różnych dipeptydów, 8000 tripepdydów a ilość potencjalnych pentapeptydów wynosi już 3,2 mln (205). Aktywne struktury poddaje się potem dekonwolucji celem wyodrębnienia najaktywniejszych struktur chemicznych. I ten etap wydaje się najtrudniejszy w całym procesie otrzymywania bibliotek związków. Należy wziąć bowiem pod uwagę, że podczas procesu otrzymywania bibliotek eksperymentator jest praktycznie pozbawiony możliwości bieżącej kontroli procesów, nie izoluje, nie oczyszcza ani nie analizuje produktów pośrednich. W podobny sposób jak dla syntez peptydów można otrzymywać biblioteki kwasów) nukleinowych czy związków niskocząsteczkowych o potencjalnym zastosowaniu farmakologicznym (fluorochinolony, benzodiazepiny i inne).
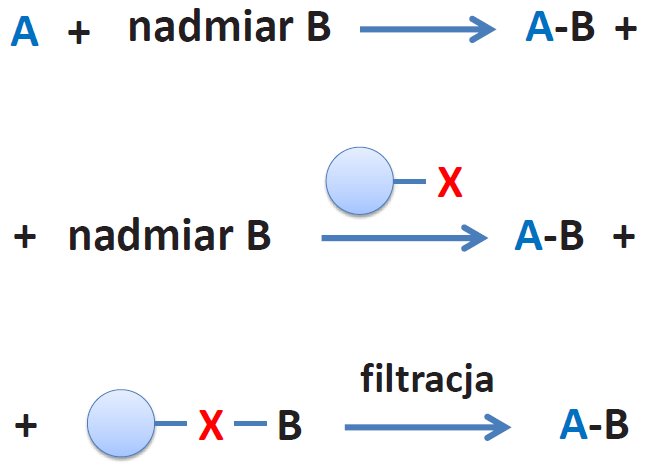
Rys. 7. Schemat wykorzystania nośnika stałego do usuwania nadmiaru jednego z reagentów.
Automatyzacja w syntezie
Aktualnie na rynku jest obecnie ponad 50 firm specjalizujących się w automatycznych syntezatorach i robotach dedykowanych do pracy w fazie stałej. Syntezy w fazie stałej znalazły zastosowanie głównie w poszukiwaniu nowych związków organicznych o potencjalnym zastosowaniu w przemyśle farmaceutycznym. Nowością ostatnich lat z wykorzystaniem syntezy na nośnikach stałych jest synteza w reaktorach na bazie chipów. W podejściu tym nośnik umieszcza się wewnątrz minikomory/kanału zabezpieczając przed ich wymyciem. Natomiast rozpuszczalniki wraz z reagentami doprowadza się stosując odpowiednie pompy perystaltyczne lub strzykawkowe. Mikrosystemy tego typu pozwalają na monitorowanie przebiegu reakcji w czasie rzeczywistym metodami spektrofotometrycznymi. Miniaturyzacja w znacznym stopniu obniża ilość zużywanych substancji oraz umożliwia szybsze i wydajniejsze prowadzenie procesu syntezy.





