- Nowe generacje protez wewnątrznaczyniowych w leczeniu choroby wieńcowej
Magdalena Maciejewska
Laboratorium Farmaceutyczne AVENA Sokulska-Dura i Palmowski s.j.
strony wersji drukowanej: 22-28
strony wersji drukowanej: 22-28
Choroby układu krążenia rozwijające się głównie na skutek miażdżycy naczyń wieńcowych stanowią jeden z ważniejszych problemów współczesnej medycyny i są najczęstszą przyczyną zgonów i hospitalizacji w krajach uprzemysłowionych.
Przełomem w walce z chorobą niedokrwienną serca był rok 1986, kiedy Puel i Sigwart umieścili po raz pierwszy stent naczyniowy w organizmie ludzkim, tym samym rozpoczynając nowy rozdział w kardiologii interwencyjnej.
Stent to rodzaj cewki w kształcie walca o strukturze cienkiej siateczki pełniącej funkcję wewnątrznaczyniowej protezy. Początkowo zabieg stentowania przeprowadzany był w przypadku powikłań angioplastyki balonowej, a już dziesięć lat po pierwszej implantacji stanowił szeroko rozpowszechnioną samodzielną technikę poszerzania naczyń wieńcowych w celu przywrócenia prawidłowego ukrwienia mięśnia sercowego. Wskazaniem do przeprowadzenia zabiegu angioplastyki jest obecność w tętnicy wieńcowej co najmniej jednej, angiograficznie istotnej (> 70% średnicy naczynia) zmiany miażdżycowej, z uwzględnieniem występowania objawów klinicznych oraz wyników dodatkowych nieinwazyjnych badań potwierdzających niedokrwienie w danym obszarze mięśniasercowego. Według danych Polskiego Towarzystwa Kardiologicznego obecnie w Polsce ponad 80% zabiegów angioplastyki wieńcowej przebiega z implantacją stentu.
Implantację wykonuje się poprzez przezskórne wprowadzenie stentu przez specjalnie ukształtowane cewniki angioplastyczne umieszczone w ujściach tętnic wieńcowych. Umieszczony na cewniku stent wprowadza się do miejsca zwężenia tętnicy gdzie następuje jego rozprężenie i implantacja w ścianie naczynia. Dostęp uzyskuje się poprzez wprowadzenie koszulki naczyniowej do tętnic obwodowych: udowej (najczęściej), ramiennej lub promieniowej. W przypadku zwapnień lub wyjątkowo krętych odcinków naczyń zaleca się wykonanie w pierwszej kolejności angioplastyki balonowej. Predylatacja umożliwia optymalne rozprężenie protezy wewnątrznaczyniowej w miejscu wystąpienia zmiany, zapobiegając jednocześnie zsunięciu się stentu z balonu i embolizacji. Szacuje się, że w 92-98% implantacji uzyskuje się pozytywny wynik PCI – przezskórnych interwencji wieńcowych (Percutaneous Coronary Interventions) określany jako prawidłowy przepływ kontrastu przez naczynie. Stosowanie stentów przyczyniło się do redukcji częstości występowania nawrotu zwężenia i liczby ponownych rewaskularyzacji.
Obecnie protezy wewnątrznaczyniowe stanowią ważne narzędzie w kardiologii inwazyjnej. Intensywny postęp technologiczny w tej dziedzinie wiąże się głównie z minimalizowaniem ryzyka powikłań. Istnieje wiele rodzajów wewnątrznaczyniowych protez oraz wiele kryteriów ich klasyfikacji. Najpowszechniej używaną klasyfikacją jest podział na stenty klasyczne – metalowe (BMS – Bare Metal Stent) oraz stenty powlekane lekiem (DES – Drug Eluting Stent). Immobilizacja leku na stentach naczyniowych (stenty typu DES) okazała się przełomem w kardiologii interwencyjnej. Połączenie funkcji podporowej rusztowania wraz z lokalnym efektem terapeutycznym substancji leczniczej w miejscu występowania zmiany stanowi skuteczne narzędzie w zapobieganiu restenozie. Kliniczne zastosowanie znalazły m.in. stenty pokryte sirolimusem, paklitakselem, ewerolimusem, takrolimusem. Przeprowadzone badania wykazały, że kliniczne zastosowanie stentów uwalniających leki w istotny sposób obniżyły odsetek nawrotnego zwężenia wieńcowego w porównaniu do klasycznych metalowych stentów BMS. Zmniejszenie ryzyka wystąpienia restenozy następuje jednak kosztem stosowania długotrwałej terapii przeciwpłytkowej zapobiegającej wystąpieniu późnej zakrzepicy w stencie.
Znaczny rozwój w dziedzinie protez naczyniowych przyniosło zastosowanie powłok polimerowych będących matrycą do uwalniania substancji leczniczych. Stenty z polimerową powłoką w odróżnieniu od klasycznych metalowych wykazują dużą plastyczność, ułatwiając transfer protezy w miejsce docelowej implantacji, a powłoka polimerowa stanowi dobrą matrycę do immobilizacji i uwalniania w kontrolowany sposób leków antyproliferacyjnych. Implanty tego typu stanowią więc ciekawą alternatywę w leczeniu choroby wieńcowej. Pojawiło się wiele publikacji o wskazujących na pozytywne wyniki badań klinicznych po zastosowaniu stentów DES o biodegradowalnych powłokach na bazie kwasu polimlekowego, poliglikolowego i kopolimeru blokowego glikolu z poli(tereftalenem etylu). Trwają badania z wykorzystaniem kolejnych biodegradowalnych powłok na bazie poli(ε-kaprolaktonu) - PCL i poli(ε-dekalaktonu).

Rycina 1. Stent w 100-krotnym powiększeniu.
Stenty biodegradowalne
Obecnie najbardziej obiecującym kierunkiem rozwoju stentów jest potencjalne zastosowanie w praktyce klinicznej implantów całkowicie biodegradowalnych będących kombinacją różnych biokompatybilnych polimerów i uwalnianych leków antyproliferacyjnych. W odróżnieniu od stentów typu DES, stenty bioabsorbowalne mają całkowicie biodegradowalną konstrukcję zapewniającą tymczasowe podparcie ściany naczyniowej po angioplastyce. Wprowadzenie stentów typu DES nowej generacji pozwoliło na znaczące ograniczenie odsetek restenoz i ponownych rewaskularyzacji w trudnych klinicznie przypadkach, tj. wielonaczyniowa choroba wieńcowa, cukrzyca czy niewydolność nerek. Stenty bioresorbowalne ulegają całkowitemu rozpuszczeniu po kilku lub kilkudziesięciu miesiącach po implantacji. Po tym okresie leczony segment naczynia odzyskuje funkcję fizjologiczną. Potencjalną korzyścią zastosowania stentów biodegradowalnych jest więc perspektywa długotrwałego przywrócenia reaktywności śródbłonka naczyń oraz odbudowy naczyń w ciągu zaledwie kilku miesięcy. Niewątpliwą zaletą stosowania tego typu stentów jest ich biokompatybilność (szybkie i właściwe formowanie neointimy) bez konieczności stosowania przedłużonej, podwójnej terapii przeciwpłytkowej. Jednocześnie zastosowanie technologii bioresorbowalnej w razie potrzeby daje możliwość reinterwencji w zakresie leczonego fragmentu oraz umożliwia nieinwazyjną kontrolę chorych z wykorzystaniem nieinwazyjnych metod obrazowania. Całkowita biodegradacja eliminuje ryzyko późnych niepożądanych incydentów wieńcowych związanych z obecnością ciał obcych w naczyniu.
Do najważniejszych wyzwań rozwijającej się technologii należą więc: zoptymalizowanie czasu bioresporpcji, właściwości mechanicznych protezy (elastyczność, wystarczająca siła radialna), właściwości fizykochemicznych (nieinwazyjne obrazowanie) i ich biokompatybilność (brak reakcji zapalnej, szybka endotelializacja, powrót fizjologicznej funkcji zmienionego segmentu naczynia).
Pierwsze badania związane z zastosowaniem biodegradowalnych protez wewnątrznaczyniowych rozpoczęto na wiele lat przed wdrożeniem w 1994 r. stentów metalowych. Istotny wkład w tym zakresie stanowiła publikacja z 1988 r. Stack’a w i wsp. o stworzeniu pierwszego biodegradowalnego stentu i przeprowadzeniu udanej implantacji u zwierząt. Lincoff i wsp. opublikowali obiecujące wyniki implantacji stentów pokrytych polimerem kwasu mlekowego (PLLA, poly L-lactic acid) o dużej masie cząsteczkowej w tętnicach wieńcowych świń. Kolejnym znaczącym doniesieniem było opublikowanie wyników badań Yamawaki i wsp.. Bioresorbowalne stenty pokryte inhibitorem kinazy tyrozynowej, wykonane z PLLA skutecznie ograniczyły hiperplazję neointimy w modelu tętnicy wieńcowej świń.
Pomimo obiecujących wyników badań przedklinicznych trudności technologiczne w produkcji biokompatybilnych polimerów oraz duże zainteresowanie stentami BMS w praktyce klinicznej wstrzymało na kilka lat rozwój technologii biodegradowalnych stentów.
Stent Igaki-Tamai
Pierwszą implantację stentu bioabsorbowalnego u człowieka przeprowadzono w 2000 r. przez Tamai i wsp. Był to stent wykonany z PLLA, którego średni czas degradacji wynosił 18-24 miesięcy. Na podstawie wyników pierwszego badania klinicznego FIM stwierdzono, że częstość występowania pożądanych zdarzeń sercowo-naczyniowych była porównywalna do wyników badań z wykorzystaniem stentów BMS. Wykonane po 3 latach badanie ultrasonografii wewnątrznaczyniowej (IVUS, Intravascular ultrasound) potwierdziło całkowitą wchłanialność przęseł stentu w leczonym segmencie naczynia. Stent Igaki-Tamai w listopadzie 2007 r. został zarejestrowany jako pierwszy stent bioresorbowalny w leczeniu zmian naczyń obwodowych.
Stent ABSORB – Stent BVS (Bioabsorbable vascular solutions)
Przełomem w kardiologii interwencyjnej było wprowadzenie jesienią 2012 roku do użytku klinicznego stentów bioabsorbowalnych ABSORB (Producent: Abbott Vascular, Santa Clara - USA). Szkielet stentu ABSORB został wykonany z polimeru na bazie kwasu mlekowego (PLLA) pokrytego warstwą poli-D-laktydu (PDLLA, poly-DL-lactic acid) uwalniającą inhibitor proliferacji komórek – ewerolimus. Biodegradacja rusztowania wynosi ok. 24 miesiące i polega na hydrolizie wiązań estrowych PLLA i PDLLA. Powstałe w wyniku hydrolizy cząsteczki kwasu mlekowego są fagocytowane przez makrofagi i końcowym etapie dochodzi do powstania dwutlenku węgla i wody. W badaniu klinicznym ABSORB prowadzonym od 2006 r. w celu klinicznej oceny bioabsorbowalnego rusztowania naczyniowego (BVS- Bioresorbable Vascular Scaffold) potwierdzono bezpieczeństwo stosowania tego typu stentów w leczeniu zmian typu de novo w natywnych naczyniach wieńcowych. Po 2 latachobserwacji wykazano, że stosowanie stentów biodegradowalnych uwalniających ewerolimus jest związane z niskim odsetkiem niepożądanych zdarzeń sercowo-naczyniowych, akceptowalną, późną utratą światła naczynia, stosunkowo niewielką proliferacją neointimy oraz całkowitym powrotem funkcji wazomotorycznej naczynia w zakresie leczonych fragmentów. W 2009 r. rozpoczęto drugą fazę badania. W kryteriach włączenia pacjentów uwzględniono chorych ze zmianami de novo w co najmniej dwóch tętnicach wieńcowych. W celu zwiększenia siły radialnej stentu z jednoczesnym opóźnieniem pierwszej fazy degradacji, zmianie uległa jedynie konstrukcja rusztowania – wprowadzono jednolity rozkład przęseł w celu lepszego podparcia ściany naczynia. Lek antyproliferacyjny oraz polimer tworzący rusztowanie i regulujący uwalnianie substancji leczniczej nie uległy zmianie. Obecnie producent rozszerzył zakres badania (ABSORB EXTEND) oceniającego grupę pacjentów z długimi zmianami zlokalizowanymi w tętnicach o małych średnicach. Stent typu BVS otrzymał certyfikat CE i jest komercyjnie dostępny w Polsce. Pierwsza implantacja stentu bioabsorbowalnego firmy Abbott Vascular w Polsce miała miejsce 8 czerwca 2006 r. w ramach zainicjowanego w Krakowie - jako jednym z sześciu na świecie ośrodków - programu badawczego ABSORB-FIM.
Stent DESolve
Kolejnym bioabsorbowalnym stentem, którego szkielet stanowi kwas poli-L-mlekowy jest stent DESolve (Elixir Medical, USA). Polimer uwalnia jako substancje antyproliferacyjne pochodne sirolimusa – miolimus oraz nowolimus. W pierwszejfazie badań z użyciem stentów DESolve uwalniających miolimus wykazano obecność cienkiej warstwy neointimy oraz brak zjawiska zapadania się światła naczynia i stentu. Obecnie trwa kliniczne badanie DESolve NX, w którym implantowane są stenty uwalniające nowolimus.
Stent DREAMS
W 2012 r. opublikowano wyniki prospektywnego badania oceniającego skuteczność i bezpieczeństwo stentu biodegradowalnego: DREAMS, firmy Biotronik. W odróżnieniu od klasycznej technologii bioresobowalnej, podstawą stentu nie jest polimer, ale stop magnezu z dodatkiem metali ziem rzadkich (mniej niż 5%). Powłokę zewnętrzną stanowi mikrometrowa warstwa klasycznego polimeru bioresorbowalnego uwalniającego paklitaksel.
Badania potwierdziły ich przydatność w leczeniu stabilnej i niestabilnej choroby wieńcowej. W pierwszym kwartale po implantacji stentu DREAMS następuje stopniowe, kontrolowane uwalnianie leku z jednoczesną degradacją magnezu, podczas gdy warstwa polimerowa zostaje stabilna. Po upływie 6 miesięcy proces degradacji magnezu zostaje zakończony, a trwa degradacja warstwy polimerowej. Całkowita degradacja warstwy polimerowej następuje po upływie 9 miesięcy.
Stent ReZolve
Kolejną interesującą bioresorbowalną protezą jest stent ReZolve (REVA Medical, San Diego, USA). Postawę stentu stanowi poliwęglan i pochodna tyrozyny (zawierająca jod). Zawartość jodu warunkuje dobrą widoczność w badaniu angiograficznym.
W badaniach przedklinicznych wykazano, że siła radialna jest porównywalna do stentów ze stali nierdzewnej, przy zachowaniu dużej elastyczności. Pomimo pierwszych obiecujących wyników w badaniu klinicznym RESORB odnotowano znaczący duży odsetek ponownych rewaskularyzacji. W nowej udoskonalonej generacji stentu usprawniono działanie mechanizmu zatrzaskowego, wzmocniono siłę radialną stentu oraz dodano substancję antyproliferacyjną – sirolimus. Obecnie trwa zrandomizowane badanie kliniczne w celu oceny przydatności tej protezy w leczeniu choroby wieńcowej.
Stent Ideal
Innym stentem ocenianym obecnie w badaniach klinicznych jest stent Ideal (Xenogenics Corp, USA) uwalniający sirolimus. Podstawę rusztowania stanowi polimer bezwodnikowy (poly-anhydride ester) w połączeniu z kwasem salicylowym. W założeniach niepożądane incydenty zakrzepowe miały zostać znacząco zredukowane poprzez specyficzną kombinację właściwości sirolimusu (właściwości antyproliferacyjne) i kwasu salicylowego (właściwości przeciwzapalne i przeciwzakrzepowe). Wstępna analiza histopatologiczna leczonego segmentu naczynia potwierdziła prawidłową odbudowę ściany naczynia. Jednocześnie odnotowano niewystarczające hamowanie proliferacji neointimy. Stent poddano więc modyfikacji poprzez zwiększenie dawki leku antyproliferacyjnego. Udoskonalona wersja protezy przechodzi kolejny etap badań klinicznych.
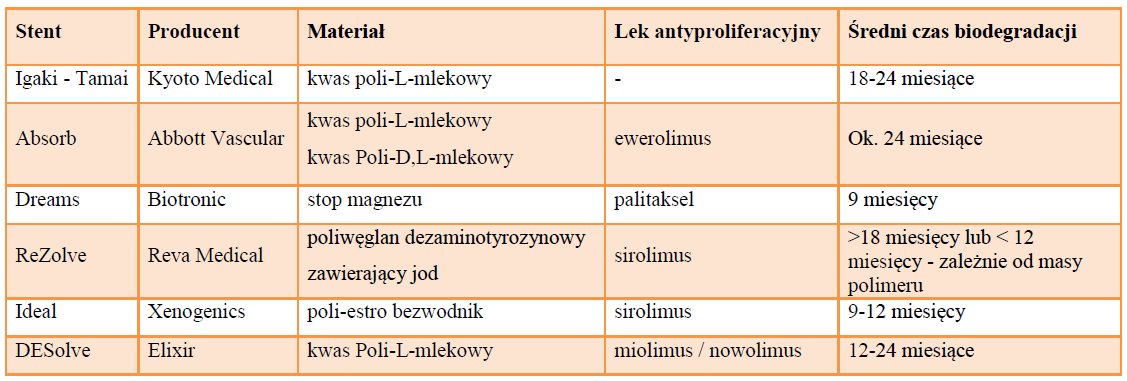
Tab. 1. Przykłady aktualnie testowanych stentów bioresorbowalnych.
Stenty bioabsorbowalne uwalniające biolimus
W ostatnich latach do użytku klinicznego w terapii STEMI (zawał serca z uniesieniem odcinka ST) wprowadzono stenty z biodegradowalną powłoką uwalniającą lek, która po depozycji czynnika antyproliferacyjnego odsłania powierzchnię zbliżoną budową do stentu BMS. W 2012 roku ogłoszono wyniki badania COMFORTABLE AMI szacującego przydatność i bezpieczeństwo implantacji stentu z biodegradowalnym polimerem uwalniającym biolimus (analog sirolimusu) w porównaniu z klasycznym stentem BMS u chorych ze STEMI. Opublikowane wyniki badań wykazały, że u chorych ze STEMI implantacja stentu z biodegradowalnym polimerem uwalniającym biolimus, w porównaniu z BMS, zmniejszała ryzyko powtórnego zawałuoraz zmniejszała liczbę ponownych rewaskularyzacji uprzednio leczonych zmian. W rocznej obserwacji odnotowano niski odsetek zakrzepicy w stenach włączonych do badania oraz nie stwierdzono istotnej różnicy pod względem śmiertelności.
Stenty wykonane ze stopów żelaza
Interesującą alternatywą dla klasycznej technologii stanowi bioresorbowany stent NOR-I wykonany z żelaza. Peuster i wsp. przeprowadzili eksperymentalne badanie implantując stent NOR-I w aortach królików. W 18-miesięcznej obserwacji nie odnotowano niepożądanych zdarzeń zakrzepowych ani nadmiernej reakcji zapalnej. Zaobserwowano jednak znaczne uszkodzenia wewnętrznej błony elastycznej naczynia prowadzące w konsekwencji do zmian struktury błony mięśniowej. Otrzymane wyniki były podstawą do wstrzymania rozwoju tej technologii.
Podsumowanie
Technologia biodegradowalnych stentów w świetle dotychczasowo uzyskanych wyników jest obiecującą koncepcją w leczeniu choroby niedokrwiennej serca. Dotychczas przeprowadzone badania z użyciem stentów biodegradowalnych dotyczyły jednak wąskiej grupy pacjentów i mimo obiecujących wyników badań, producenci zalecają stosowanie tego typu stentów do ściśle określonych zmianach w naczyniu. Wykazano, jednak że zastosowanie kliniczne stentów całkowicie biodegradowalnych ułatwia przeprowadzenie późniejszych zabiegów rewaskularyzacyjnych. Otrzymane wyniki są więc podstawą do kontynuowania badań w celu lepszego określenia skuteczności i bezpieczeństwa stosowania stentów bioabsorbowalnych. Technologia oparta na bioabsorbowalnych polimerach zwłaszcza w połączeniu z lekami antyproliferacyjnymi jest obiecującym kierunkiem rozwoju stentów nowej generacji.
Literatura:
1. Alfonso F.: New Drug-eluting Stents: Polymer-free, Biodegradable Polymers or Bioabsorbable Scaffolds?. Rev Esp Cardiol. 2013 Jun;66(6):423-426.
2. Gil R., J.: Komentarz redakcyjny. Zwężenie zwężeniu nierówne. Kardiol. Pol., 2009, 67, 1054-1056.
3. Guzik Ł., Nasternak M., Maciejewski M.: Stenty powlekane lekiem jako kierunek rozwoju wewnątrznaczyniowych protez naczyniowych. Pol Merkur Lekarski. 2010 Apr;28(166):297-301.
4. Haude M., Erbel R., Erne P. i wsp.: Safety and performance of the drug eluting absorbable metal scaffold (DREAMS) in patients with de novo coronary lesions: 12 month results of the prospective, multicentre, first in man BIOSOLVE 1 trial. Lancet (Early Online Publication, 15 January 2013), doi:10.1016/S0140-6736(12)61 765–6.
5. Itagaki B.K, Brar S.S: Controversies in the use & implementation of drug-eluting stent technology. Indian J Med Res. 2012 December; 136(6): 926–941.
6. Milewski K., Tajstra M.: Stenty bioabsorbowalne – aktulany stan wiedzy. Folia Cardiologica Excerpta 2012, tom 7, nr 4, 213-219.
7. Depukat R., Dudek D.: Biodegradowalne stenty wieńcowe czwartą rewolucją w kardiologii inwazyjnej. Post Kardiol Interw 2009; 5, 3 (17), 144-147.
8. Ilnicka M., Wawrzyńska M., Biały D.: Biodegradowalne stenty wieńcowe – przegląd. Acta Bio-Optica et Informatica Medica 2009, 4, vol.15, 369-372.
9. Kuehler M., De ScheerderI.: Drug delivery coatings. (w) Serruys, P.W., Gershlick, A.H., (red): Handbook of Drug-eluting stents. Taylor@Francis, London, 2005, 65-74.
10. Lesiak M., Grajek S. Kliniczne znaczenie restenozy. Folia Cardiol. 2000; 7,supl.C, 17–21.
11. Lowe H., Oesterle S., Khachigian L.: Coronary instent restenosis: Current status and future strategies. J. Am. Coll. Cardiol., 2002; 39: 183-193.
12. Mehilli J., Dibra A., Kastrati A.: A randomized comparison of a sirolimus-eluting stent with a standard stent. Advances in Interventional Cardiology 3/2006; 295: 895-904.
13. Raber L., Kelbaek H., Ostojic M. i wsp.: Effect of biolimus eluting stents with biodegradable polymer vs bare metal stents on cardiovascular events among patients with acute myocardial infarction. The COMFORTABLE AMI Randomized Trial. JAMA, 2012; 308: 777–787.
2. Gil R., J.: Komentarz redakcyjny. Zwężenie zwężeniu nierówne. Kardiol. Pol., 2009, 67, 1054-1056.
3. Guzik Ł., Nasternak M., Maciejewski M.: Stenty powlekane lekiem jako kierunek rozwoju wewnątrznaczyniowych protez naczyniowych. Pol Merkur Lekarski. 2010 Apr;28(166):297-301.
4. Haude M., Erbel R., Erne P. i wsp.: Safety and performance of the drug eluting absorbable metal scaffold (DREAMS) in patients with de novo coronary lesions: 12 month results of the prospective, multicentre, first in man BIOSOLVE 1 trial. Lancet (Early Online Publication, 15 January 2013), doi:10.1016/S0140-6736(12)61 765–6.
5. Itagaki B.K, Brar S.S: Controversies in the use & implementation of drug-eluting stent technology. Indian J Med Res. 2012 December; 136(6): 926–941.
6. Milewski K., Tajstra M.: Stenty bioabsorbowalne – aktulany stan wiedzy. Folia Cardiologica Excerpta 2012, tom 7, nr 4, 213-219.
7. Depukat R., Dudek D.: Biodegradowalne stenty wieńcowe czwartą rewolucją w kardiologii inwazyjnej. Post Kardiol Interw 2009; 5, 3 (17), 144-147.
8. Ilnicka M., Wawrzyńska M., Biały D.: Biodegradowalne stenty wieńcowe – przegląd. Acta Bio-Optica et Informatica Medica 2009, 4, vol.15, 369-372.
9. Kuehler M., De ScheerderI.: Drug delivery coatings. (w) Serruys, P.W., Gershlick, A.H., (red): Handbook of Drug-eluting stents. Taylor@Francis, London, 2005, 65-74.
10. Lesiak M., Grajek S. Kliniczne znaczenie restenozy. Folia Cardiol. 2000; 7,supl.C, 17–21.
11. Lowe H., Oesterle S., Khachigian L.: Coronary instent restenosis: Current status and future strategies. J. Am. Coll. Cardiol., 2002; 39: 183-193.
12. Mehilli J., Dibra A., Kastrati A.: A randomized comparison of a sirolimus-eluting stent with a standard stent. Advances in Interventional Cardiology 3/2006; 295: 895-904.
13. Raber L., Kelbaek H., Ostojic M. i wsp.: Effect of biolimus eluting stents with biodegradable polymer vs bare metal stents on cardiovascular events among patients with acute myocardial infarction. The COMFORTABLE AMI Randomized Trial. JAMA, 2012; 308: 777–787.





