Maciej Jaśkiewicz
Gdański Uniwersytet Medyczny
strony wersji drukowanej: 38-41

strony wersji drukowanej: 38-41

Jakość mikrobiologiczna produktów kosmetycznych jest jednym z kluczowych elementów bezpieczeństwa ich stosowania. Zakażenie kosmetyku jest groźne nie tylko dla konsumenta lecz również dla wytwórcy. Producent, by zapewnić odpowiednią jakość swoich produktów musi nie tylko zachowywać określone procedury i standardy wytwarzania, lecz również stale prowadzić weryfikację czystości mikrobiologicznej. Stanowią one gwarancję, że gotowy produkt jest wolny od niepożądanych patogenów oraz że użytkowanie go w sposób zdefiniowany nie stanowi zagrożenia dla zdrowia. Rozporządzenie Parlamentu Europejskiego i Rade (WE) z dnia 30 listopada 2009 r. dotyczące produktów kosmetycznych nakłada na producentów konieczność posiadania raportu bezpieczeństwa produktu [1]. Jednym z kluczowych elementów tego raportu jest jakość mikrobiologiczna kosmetyku. Musi on zawierać szczegółową specyfikację produktu oraz wyniki badania obciążeniowego – testu konserwacji.
Testy Konserwacji
Testy konserwacji (ang. challenge test) są gwarantem, że zastosowane środki konserwujące zabezpieczają produkt kosmetyczny przed rozwojem niebezpiecznych drobnoustrojów oraz chronią przed rozwojem wtórnych zakażeń w trakcie użytkowania. Należy jednak zwrócić szczególną uwagę na fakt, że rolą użytych konserwantów nie jest eliminacja efektów nieprawidłowego procesu technologicznego. Ważne jest by kosmetyk posiadał odpowiednią recepturę, a także by był wytwarzany i przechowywany w sposób uniemożliwiający zakażenie. Powyższe elementy mogą być modyfikowane i weryfikowane na etapie projektowania kosmetyku. Niemniej jednak ważna jest również kontrola jakości, która powinna być składową każdego stadium procesu technologicznego. Testy konserwacji przeprowadza się na różnych etapach badawczo-wdrożeniowych oraz produkcji. Polegają one na zaszczepieniu próbki wybranymi referencyjnymi szczepami bakterii, drożdżaków oraz pleśni i inkubacji w odpowiednich warunkach wzrostu (Tabela 1).
Tabela 1. Drobnoustroje wykorzystywane w testach konserwacji.
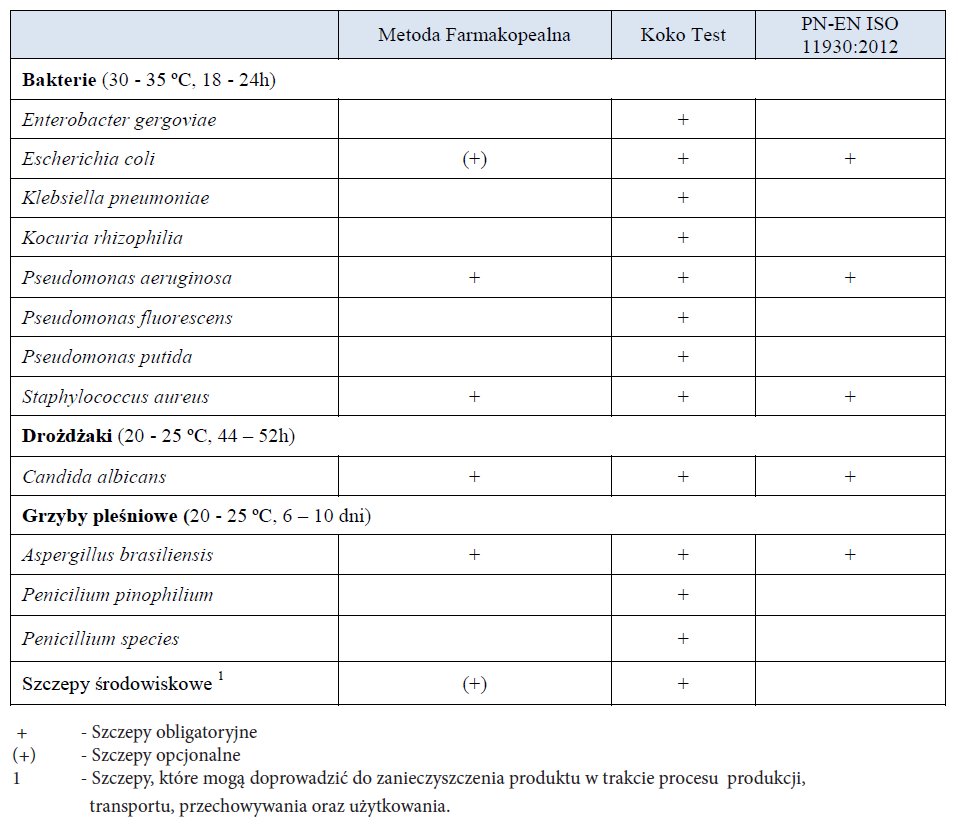
Następnie w wyszczególnionych odstępach czasu przeprowadza się posiewy w celu określenia stopnia redukcji drobnoustrojów. Istotne jest, by w teście konserwacji wszystkie odczynniki, podłoża oraz szczepy pochodziły z certyfikowanych i oryginalnych źródeł. O skuteczności zastosowanego układu konserwującego możemy powiedzieć, gdy następuje wymagany spadek lub brak wzrostu mikroorganizmów. Na tę chwilę w obecnym ustawodawstwie nie ma szczegółowych wytycznych co do rodzaju używanego testu konserwacji produktów kosmetycznych. Do najczęściej stosowanych metod w Polsce należą:
- Metoda Farmakopealna
- Metoda Koko Test
- Norma PN-EN ISO 11930:2012
METODA FARMAKOPEALNA
Metoda ta, polega na wprowadzeniu do zakonserwowanej próbki produktu referencyjnych szczepów: Pseudomonas aeruginosa, Staphylococcus aureus, Candida albicans oraz Aspergillus brasiliensis (dawniej Aspergillus niger). Gęstość użytej zawiesiny (inokulum) drobnoustrojów jest jednakowa dla wszystkich badanych mikroorganizmów. Każdy szczep bada się oddzielnie, próbki kontaminowane są jednokrotnie i pozostawia się je na określony czas działania. Test uznawany jest za zaliczony, jeśli spełnione zostaną kryteria akceptacji (Tabela 2.)
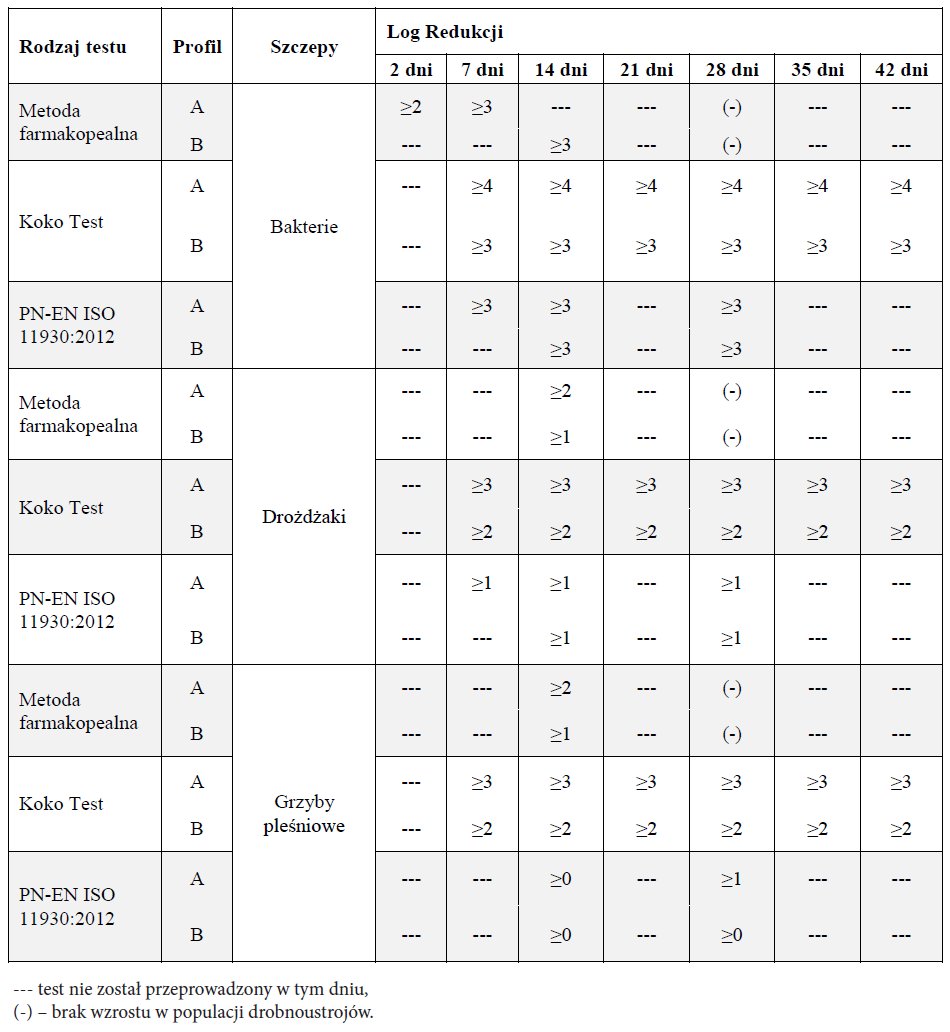
Ponadto wyróżniamy 2 profile kryteriów akceptacji: A oraz B. W kryterium A produkt kosmetyczny wysiewamy po 48 godzinach, 7 oraz 28 dniach dla bakterii oraz 14 i 28 dniach dla grzybów (drożdży oraz grzybów pleśniowych). W przypadku gdy kryterium to nie może być spełnione - ze względu na możliwość ryzyka wystąpienia działań niepożądanych u konsumenta, które wynikają ze zwiększonego stężenia środka konserwującego, przyjmuje się kryterium B. Zawiera ono akceptowalne i bezpieczne stężenie konserwantu. Uwzględniając jego założenia, posiewy wykonuje się w 14 i 28 dniu inkubacji zarówno dla bakterii jak i grzybów.
Tabela 2. Kryteria akceptacji dla wybranych testów.

Ponadto wyróżniamy 2 profile kryteriów akceptacji: A oraz B. W kryterium A produkt kosmetyczny wysiewamy po 48 godzinach, 7 oraz 28 dniach dla bakterii oraz 14 i 28 dniach dla grzybów (drożdży oraz grzybów pleśniowych). W przypadku gdy kryterium to nie może być spełnione - ze względu na możliwość ryzyka wystąpienia działań niepożądanych u konsumenta, które wynikają ze zwiększonego stężenia środka konserwującego, przyjmuje się kryterium B. Zawiera ono akceptowalne i bezpieczne stężenie konserwantu. Uwzględniając jego założenia, posiewy wykonuje się w 14 i 28 dniu inkubacji zarówno dla bakterii jak i grzybów.
METODA KOKO TEST
W metodzie tej punktem odniesienia jest niezakonserwowana próbka badanego produktu – próbka kontrolna. Do zakonserwowanych próbek oraz kontroli wprowadza się mieszaninę wszystkich dedykowanych, referencyjnych drobnoustrojów (bakterii oraz grzybów) i wysiewa co 7 dni. Bezpośrednio po wykonaniu posiewu próbki te są kolejny raz kontaminowane tą samą mieszaniną mikroorganizmów. Proces ten powtarza się 6-krotnie, a więc ostatnia kontrola przeprowadzana jest na próbce mającej 6 tygodni. Czas ten jest odpowiedni do określenia jakości mikrobiologicznej i potwierdzony został licznymi badaniami laboratoryjnymi. Odczytu wyniku dokonuje się wizualnie, a wynik interpretowany jest wg skali. Kryteria akceptacji, tak jak w przypadku metody farmakopealnej również zostały podzielone na A i B (Tabela 2). Natomiast wskaźnikiem dobrej konserwacji jest obserwowany brak wzrostu drobnoustrojów po 6 cyklach kontaminacji badanej próbki.
NORMA PN-EN ISO 11930:2012
W przypadku metody określonej w PN-EN ISO 11930:2012 do badanej próbki wprowadza się drobnoustroje Escherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus, Candida albicans oraz Aspergillus brasiliensis. Gęstość użytej zawiesiny mikroorganizmów jest inna dla bakterii, drożdżaków oraz grzybów pleśniowych oraz badanie wykonywane jest na oddzielnie dla każdego szczepu. Zanieczyszczoną próbkę wysiewa się po 7, 14 oraz 28 dniach dla bakterii i drożdżaków, natomiast dla grzybów pleśniowych po 14 i 28 dniach. Ocenę skuteczności układu konserwującego dokonuje się liczbowo i tak jak w pozostałych przypadkach również z uwzględnieniem dwóch profili – A i B (Tabela 2).
PODSUMOWANIE
Przeprowadzenie testu konserwacji jest niezwykle ważne dla potwierdzenia bezpieczeństwa stosowania produktu kosmetycznego, tym samym zdrowia konsumenta. Stanowi on gwarancję, że użyte środki konserwujące zabezpieczają przed rozwojem niebezpiecznych patogenów i eliminują możliwość wtórnego zakażenia próbki w trakcie użytkowania. W tym artykule przedstawione zostały trzy najczęściej stosowane w Polsce testy konserwacji produktów kosmetycznych. Różnią się one sposobem zanieczyszczania próbki, jak również czasem odczytu wyników. Jednak we wszystkich przypadkach obrazują właściwości użytych środków konserwujących. Dobór odpowiedniego testu powinien być podyktowany rodzajem produktu, jego składem i procesem technologicznym. Jego wybór powinien zostać określony na etapie projektowania produktu, w porozumieniu z laboratorium mikrobiologicznym. Dzięki temu mamy pewność, że użyty test w pełni odzwierciedli bezpieczeństwo stosowania gotowego kosmetyku.
Bibliografia:
1. ROZPORZĄDZENIE PARLAMENTU EUROPEJSKIEGO I RADY (WE) NR 1223/2009 z dnia 30 listopada 2009 r. dotyczące produktów kosmetycznych, Dziennik Urzędowy Unii Europejskiej, L 342/59.
2. European Pharmacopeia 7th Main edition.
3. Siegert W.: Comparison of microbial challenge testing methods for cosmetics, Household and Personal Care Today, Vol. 8(2) 2013.
4. Polska Norma PN-EN ISO 11930:2012, Kosmetyki – Mikrobiologia – Test skuteczności i ocena zakonserwowania produktów kosmetycznych.
5. Kurszewska M.: Jakość należy wyprodukować. „Przemysł Kosmetyczny” nr 1/2012.





